Co энергетическая диаграмма. Основные положения метода молекулярных орбиталей
Предпосылки возникновения метода
Хронологически метод молекулярных орбиталей появился позже метода валентных связей, поскольку оставались в теории ковалентной связи вопросы, которые не могли получить объяснение методом валентных связей. Рассмотрим некоторые из них.
Основное положение метода валентных связей состоит в том, что связь между атомами осуществляется за счет электронных пар (связующих двух-электронных облаков). Но это не всегда так. В ряде случаев в образовании химической связи участвуют отдельные электроны. Так, в молекулярном ионе Н 2+ одноэлектронная связь. Метод валентных связей образование одноэлектронной связи объяснить не может, она противоречит его основному положению.
Метод валентных связей не объясняет также роли неспаренных электронов в молекуле. Молекулы, имеющие неспаренные электроны, парамагнитны, т.е. втягиваются в магнитное поле, так как неспаренный электрон создает постоянный магнитный момент. Если в молекулах нет неспаренных электронов, то они диамагнитны - выталкиваются из магнитного поля. Молекула кислорода парамагнитна, в ней имеется два электрона с параллельной ориентацией спинов, что противоречит методу валентных связей. Необходимо также отметить, что метод валентных связей не смог объяснить ряд свойств комплексных соединений - их цветность и др.
Чтобы объяснить эти факты, был предложен метод молекулярных орбиталей.
Основные положения метода
Согласно методу молекулярных орбиталей электроны в молекулах распределены по молекулярным орбиталям, которые подобно атомным орбиталям характеризуются определенной энергией (энергетическим уровнем) и формой. В отличие от атомных орбиталей молекулярные орбитали охватывают не один атом, а всю молекулу, т.е. являются двух- или многоцентровыми. Если в методе валентных связей атомы молекул сохраняют определенную индивидуальность, то в методе молекулярных орбиталей молекула рассматривается как единая система.
Наиболее широко в методе молекулярных орбиталей используется линейная комбинация атомных орбиталей. При этом соблюдается несколько правил:
Уравнение Шредингера для молекулярной системы должно состоять из члена кинетической энергии и члена потенциальной энергии сразу для всех электронов. Но решение одного уравнения с таким большим количеством переменных (индексы и координаты всех электронов) невозможно, поэтому вводится понятие одноэлектронного приближения .
Одноэлектронное приближение предполагает, что можно рассматривать каждый электрон движущимся в поле ядер и усредненном поле остальных электронов молекулы. Это означает, что каждый i -й электрон в молекуле описывается своей собственной функцией ψ i и имеет свою собственную энергию E i . В соответствии с этим, для каждого электрона в молекуле можно составить свое уравнение Шредингера. Тогда для n электронов необходимо решить n уравнений. Это осуществляется методами матричного исчисления с помощью компьютеров.
При решении уравнения Шредингера для многоцентровой и многоэлектронной системы получаются решения в виде одноэлектронных волновых функций - молекулярных орбиталей, их энергий и электронной энергии всей молекулярной системы как целого.
Линейная комбинация атомных орбиталей
В одноэлектронном приближении метод молекулярных орбиталей описывает каждый электрон своей орбиталью. Как в атоме есть атомные орбитали, так и в молекуле есть молекулярные орбитали. Различие заключается в том, что молекулярные орбитали - многоцентровые.
Рассмотрим электрон, расположенный на молекулярной орбитали ψ i нейтральной молекулы, в тот момент времени, когда он находится вблизи ядра некоторого атома m . В этой области пространства потенциальное поле создается, в основном, ядром атома m и находящимися вблизи электронами. Поскольку молекула в целом нейтральна, притяжение между рассматриваемым электроном и каким-либо другим ядром n приблизительно компенсируется отталкиванием между рассматриваемым электроном и электронами, находящимися вблизи ядра n . Значит, вблизи ядра движение электрона будет приближенно таким же, как и в отсутствие остальных атомов. Поэтому в орбитальном приближении молекулярная орбиталь ψ i вблизи ядра m должна быть похожа на одну из атомных орбиталей этого атома. Поскольку атомная орбиталь имеют существенные значения только вблизи своих ядер, можно приблизительно представить молекулярную орбиталь ψ i в виде линейной комбинации атомных орбиталей отдельных атомов.
Для простейшей молекулярной системы, состоящей из двух ядер атомов водорода, учитывая 1s -атомные орбитали, описывающие движение электрона в атоме Н , молекулярная орбиталь представляется в виде:
Величины c 1i и c 2i - численные коэффициенты, которые и находятся решением уравнения Шредингера . Они показывают вклад каждой атомной орбитали в конкретную молекулярную орбиталь. В общем случае коэффициенты принимают значения, лежащие в интервале от -1 до +1. Если в выражении для конкретной молекулярной орбитали один из коэффициентов преобладает, то это отвечает тому, что электрон, находясь на данной молекулярной орбитали, в основном находится вблизи того ядра и описывается в основном именно той атомной орбиталью, чей коэффициент больше. Если коэффициент перед атомной орбиталью близок к нулю, то это означает, что пребывание электрона в области, описываемой данной атомной орбиталью маловероятно. По физическому смыслу квадраты данных коэффициентов определяют вероятность нахождения электрона в области пространства и энергий, описываемых данной атомной орбиталью.
В методе ЛКАО для образования устойчивой молекулярной орбитали необходимо, чтобы энергии атомных орбиталей были близки друг к другу. Кроме того, нужно, чтобы их симметрия не сильно отличалась. При выполнении этих двух требований коэффициенты должны быть близкими по своим значениям, а это, в свою очередь, обеспечивает максимальное перекрывание электронных облаков. При сложении атомных орбиталей образуется молекулярная орбиталь, энергия которой понижается относительно энергий атомных орбиталей. Такая молекулярная орбиталь называется связывающей . Волновая функция, соответствующая связывающей орбитали, получается в результате сложения волновых функций с одинаковым знаком. Электронная плотность при этом концентрируется между ядрами, и волновая функция принимает положительное значение. При вычитании атомных орбиталей энергия молекулярной орбитали повышается. Эта орбиталь называется разрыхляющей . Электронная плотность в этом случае располагается за ядрами, а между ними равна нулю. Волновая функция в двух образовавшихся электронных облаках имеет противоположные знаки, что хорошо видно из схемы образования связывающей и разрыхляющей орбиталей.
Когда атомная орбиталь одного из атомов вследствие большой разницы в энергии или симметрии не может взаимодействовать с атомной орбиталью другого атома, она переходит в энергетическую схему молекулярных орбиталей молекулы с энергией, соответствующей ей в атоме. Орбиталь этого типа называется несвязывающей .
Классификация орбиталей
Классификация орбиталей на σ или π производится в соответствии с симметрией их электронных облаков. σ -орбиталь имеет такую симметрию электронного облака, при которой поворот ее вокруг оси, соединяющей ядра, на 180° приводит к орбитали, по форме не отличимой от первоначальной. Знак волновой функции при этом не меняется. В случае π -орбитали при повороте ее на 180° знак волновой функции меняется на противоположный. Отсюда следует, что s -электроны атомов при взаимодействии между собой могут образовывать только σ -орбитали, а три (шесть) p -орбитали атома - одну σ- и две π -орбитали, причем σ -орбиталь возникает при взаимодействии р х атомных орбиталей, а π -орбиталь - при взаимодействии р y и р z . Молекулярные π -орбитали повернуты относительно межьядерной оси на 90°.
Для того чтобы отличать связывающие и разрыхляющие орбитали друг от друга, а также их происхождение, принята следующая система обозначений. Связывающая орбиталь обозначается сокращением «св» , располагающимся справа вверху после греческой буквы, обозначающей орбиталь, а разрыхляющая - соответственно «разр» . Принято еще одно обозначение: звездочкой помечаются разрыхляющие орбитали, а без звездочки - связывающие. После обозначения молекулярной орбитали пишется обозначение атомной орбитали, которой молекулярная обязана своим происхождением, например, π разр 2p y . Это означает, что молекулярная орбиталь π -типа, разрыхляющая, образовалась при взаимодействии 2р y - атомных орбиталей.
Положение атомной орбитали на шкале энергий определяется значением энергии ионизации атома, отвечающей удалению электрона, описываемого данной орбиталью, на бесконечно большое расстояние. Такая энергия ионизации называется орбитальной энергией ионизации . Так, для атома кислорода возможны типы ионизации, когда удаляется электрон с 2р - или с 2s -электронной подоболочки.
Положение молекулярной орбитали энергетических диаграммах также определяется на основании квантово-химических расчетов электронной структуры молекул. Для сложных молекул число энергетических уровней молекулярных орбиталей на энергетических диаграммах велико, однако для конкретных химических задач часто важно знать энергии и состав не всех молекулярных орбиталей, а только наиболее «чувствительных» к внешним воздействиям. Такими орбиталями являются молекулярные орбитали, на которых размещены электроны самых высоких энергий. Эти электроны могут легко взаимодействовать с электронами других молекул, удаляться с данной молекулярной орбитали, а молекула будет переходить в ионизированное состояние или видоизменяться вследствие разрушения одних или образования других связей. Такой молекулярной орбиталью является высшая занятая молекулярная орбиталь. Зная число молекулярных орбиталей (равно суммарному числу всех атомных орбиталей) и число электронов, нетрудно определить порядковый номер ВЗМО и, соответственно, из данных расчета - ее энергию и состав. Также наиболее важной для изучения химических задач является низшая свободная молекулярная орбиталь, т.е. следующая по очереди за ВЗМО на шкале энергий, но вакантная молекулярная орбиталь. Важны и другие орбитали, прилегающие по энергии к ВЗМО и НСМО.
Молекулярные орбитали в молекулах, как и атомные орбитали в атомах, характеризуются не только относительной энергией, но и определенной суммарной формой электронного облака. Аналогично тому, как в атомах имеются s -, р -, d -, ... орбитали, самая простая молекулярная орбиталь, обеспечивающая связь между только двумя центрами (двухцентровая молекулярная орбиталь), может быть σ -, π -, δ -, ... типа. Молекулярные орбитали разделяются на типы в зависимости от того, какой симметрией они обладают относительно линии, соединяющей ядра атомов относительно плоскости, проходящей через ядра молекулы и др. Это приводит к тому, что электронное облако молекулярной орбитали различным образом распределяется в пространстве.
| σ -орбитали - это молекулярные орбитали, симметричные относительно вращения вокруг межъядерной оси. Область повышенной электронной плотности σ -молекулярной орбитали распределена вдоль данной оси. Такие молекулярные орбитали могут быть образованны любыми атомными орбиталями атомных орбиталей любой симметрии. На рисунке заливкой помечены участки волновых функций, имеющие отрицательный знак; остальные участки имеют положительный знак. | π -орбитали - это молекулярные орбитали, антисимметричные относительно вращения вокруг межъядерной оси. Область повышенной электронной плотности π -молекулярных орбиталей распределена вне межъядерной оси. Молекулярные орбитали π -симметрии образуются при особом перекрывании р -, d - и f -атомных орбиталей. | δ -орбитали - это молекулярные орбитали, антисимметричные относительно отражения в двух взаимно перпендикулярных плоскостях, проходящих через межъядерную ось. δ -молекулярная орбиталь образуется при особом перекрывании d - и f -атомных орбиталей. Электронное облако данных молекулярных орбиталей распределено, главным образом, вне межъядерной оси. |
Физический смысл метода
Для любой другой системы, включающей k атомных орбиталей, молекулярная орбиталь в приближении метода ЛКАО запишется в общем виде следующим образом:
Для уяснения физического смысла такого подхода вспомним, что волновая функция Ψ соответствует амплитуде волнового процесса, характеризующего состояние электрона. Как известно, при взаимодействии, например, звуковых или электромагнитных волн их амплитуды складываются. Как видно, приведенное уравнение разложения молеклярной орбитали на составляющие атомные орбитали равносильно предположению, что амплитуды молекулярной «электронной волны» (т. е. молекулярная волновая функция) тоже образуются сложением амплитуд взаимодействующих атомных «электронных волн» (т. е. сложением атомных волновых функций). При этом, однако, под влиянием силовых полей ядер и электронов соседних атомов волновая функция каждого атомного электрона изменяется по сравнению с исходной волновой функцией этого электрона в изолированном атоме. В методе ЛКАО эти изменения учитываются путем введения коэффициентов c iμ , где индекс i определяет конкретную молекулярную орбиталь, а индекс cμ - конкретную атомную орбиталь. Так что при нахождении молекулярной волновой функции складываются не исходные, а измененные амплитуды - c iμ ·ψ μ .
Выясним, какой вид будет иметь молекулярная волновая функция Ψ 1 , образованная в результате взаимодействия волновых функций ψ 1 и ψ 2 - 1s -орбиталей двух одинаковых атомов. Для этого найдем сумму c 11 ·ψ 1 + c 12 ·ψ 2 . В данном случае оба рассматриваемых атома одинаковы, так что коэффициенты c 11 и c 12 равны по величине (c 11 = c 12 = c 1 ) и задача сводится к определению суммы c 1 ·(ψ 1 + ψ 2) . Поскольку постоянный коэффициент c 1 не влияет на вид искомой молекулярной волновой функции, а только изменяет ее абсолютные значения, ограничимся нахождением суммы (ψ 1 + ψ 2) . Для этого расположим ядра взаимодействующих атомов на том расстоянии друг от друга (r) , на котором они находятся в молекуле, и изобразим волновые функции 1s -орбиталей этих атомов (рисунок а ).
Чтобы найти молекулярную волновую функцию Ψ 1 , сложим величины ψ 1 и ψ 2 : в результате получится кривая, изображенная на (рисунке б ). Как видно, в пространстве между ядрами значения молекулярной волновой функции Ψ 1 больше, чем значения исходных атомных волновых функций. Но квадрат волновой функции характеризует вероятность нахождения электрона в соответствующей области пространства, т. е. плотность электронного облака. Значит, возрастание Ψ 1 в сравнении с ψ 1 и ψ 2 означает, что при образовании молекулярной орбиталли плотность электронного облака в межъядерном пространстве увеличивается. В результате образуется химическая связь. Поэтому молекулярная орбиталь рассматриваемого типа называется связывающей .
В данном случае область повышенной электронной плотности находится вблизи оси связи, так что образовавшаяся молекулярная орбиталь относится к σ -типу. В соответствии с этим, связывающая молекулярная орбиталь, полученная в результате взаимодействия двух атомных 1s -орбиталей, обозначается σ 1s св .
Электроны, находящиеся на связывающей молекулярной орбитали, называются связывающими электронами .
Рассмотрим другую молекулярную орбиталь Ψ 2 . По причине симметрии системы следует предположить, что коэффициенты перед атомными орбиталями в выражении для молекулярной орбитали Ψ 2 = c 21 ·ψ 1 + c 22 ·ψ 2 должны быть равны по модулю. Но тогда они должны отличаться друг от друга знаком: c 21 = - c 22 = c 2 .
Значит, кроме случая где знаки вкладов обеих волновых функции одинаковы, возможен и случай, когда знаки вкладов 1s -атомных орбиталей различны. В таком случае (рисунок (а) )вклад 1s -атомной орбитали одного атома положителен, а другого - отрицателен. При сложении этих волновых функций получится кривая, показанная на рисунке (б) . Молекулярная орбиталь, образующаяся при подобном взаимодействии, характеризуется уменьщением абсолютной величины волновой функции в межъядерном пространстве по сравнению с ее значением в исходных атомах: на оси связи появляется даже узловая точка, в которой значение волновой функции, а, следовательно, и ее квадрата, обращается в нуль. Это означает, что в рассматриваемом случае уменьшится и плотность электронного облака в пространстве между атомами. В результате притяжение каждого атомного ядра в направлении к межъядерной области пространства окажется более слабым, чем в противоположном направлении, т.е. возникнут силы, приводящие к взаимному отталкиванию ядер. Здесь, следовательно, химическая связь не возникает; образовавшаяся в этом случае молекулярная орбиталь называется разрыхляющей σ 1s * , а находящиеся на ней электроны - разрыхляющими электронами .
Переход электронов с атомных 1s -орбиталей на связывающую молекулярную орбиталь, приводящий к возникновению химической связи, сопровождается выделением энергии. Напротив, переход электронов с атомных 1s -орбиталей на разрыхляющую молекулярную орбиталь требует затраты энергии. Следовательно, энергия электронов на орбитали σ 1s св ниже, а на орбитали σ 1s * выше, чем на атомных 1s -орбиталях. Приближенно можно считать, что при переходе 1s -электрона на связывающую молекулярную орбиталь выделяется столько же энергии, сколько необходимо затратить для его перевода на разрыхляющую молекулярную орбиталь.
Порядок связи
В методе молекулярных орбиталей для характеристики электронной плотности, ответственной за связывание атомов в молекулу вводится величина - порядок связи . Порядок связи, в отличие от кратности связи, может принимать нецелочисленные значения. Порядок связи в двухатомных молекулах принято определять по числу связывающих электронов, участвующих в ее образовании: два связывающих электрона соответствуют простой связи, четыре связывающих электрона - двойной связи и т. д. При этом разрыхляющие электроны компенсируют действие соответствующего числа связывающих электронов. Так, если в молекуле имеются 6 связывающих и 2 разрыхляющих электрона, то избыток числа связывающих электронов над числом разрыхляющих равен четырем, что соответствует образованию двойной связи. Следовательно, с позиции метода молекулярных орбиталей химическую связь в молекуле водорода, образованную двумя связывающими электронами, следует рассматривать как простую связь.
У элементов первого периода валентной орбиталью является 1s -орбиталь. Эти две атомных орбитали образуют две σ -молекулярные орбитали - связывающую и разрыхляющую. Рассмотрим электронное строение молекулярного иона H 2 + . Он имеет один электрон, который будет занимать более энергетически выгодную s -связывающую орбиталь. В соответствии с правилом подсчета кратности связи она будет равна 0,5, а так как в ионе имеется один неспаренный электрон, H 2 + будет обладать парамагнитными свойствами. Электронное строение этого иона запишется по аналогии с электронным строением атома так: σ 1s св . Появление второго электрона на s -связывающей орбитали приведет к энергетической диаграмме, описывающей молекулу водорода, возрастанию кратности связи до единицы и диамагнитным свойствам. Возрастание кратности связи повлечет за собой и увеличение энергии диссоциации молекулы H 2 и более короткому межъядерному расстоянию по сравнению с аналогичной величиной у иона водорода.
Двухатомная молекула Не 2 существовать не будет, так как имеющиеся у двух атомов гелия четыре электрона расположатся на связывающей и разрыхляющей орбиталях, что приводит к нулевой кратности связи. Но в тоже время ион He 2 + будет устойчив и кратность связи в нем равна 0,5. Так же, как и ион водорода, этот ион будет обладать парамагнитными свойствами.
У элементов второго периода появляются еще четыре атомных орбитали: 2s, 2р х, 2р у, 2р z , которые будут принимать участие в образовании молекулярных орбиталей. Различие в энергиях 2s - и 2p -орбиталей велико, и они не будут взаимодействовать между собой с образованием молекулярных орбиталей. Эта разница в энергиях при переходе от первого элемента к последнему будет увеличиваться. В связи с этим обстоятельством электронное строение двухатомных гомоядерных молекул элементов второго периода будет описываться двумя энергетическими диаграммами, отличающимися порядком расположения на них σ св 2p x и π св 2p y,z . При относительной энергетической близости 2s - и 2p -орбиталей, наблюдаемой в начале периода, включая атом азота, электроны, находящиеся на σ разр 2s и σ св 2p x -орбиталях, взаимно отталкиваются. Поэтому π св 2p y - и π св 2p z -орбитали оказываются энергетически более выгодными, чем σ св 2p x -орбиталь. На рисунке представлены обе диаграммы. Так как участие 1s -электронов в образовании химической связи незначительно, их можно не учитывать при электронном описании строения молекул, образованных элементами второго периода.
Второй период системы открывают литий и бериллий, у которых внешний энергетический уровень содержит лишь s -электроны. Для этих элементов схема молекулярных орбиталей ничем не будет отличаться от энергетических диаграмм молекул и ионов водорода и гелия, с той лишь разницей, что у последних она построена из 1s -электронов, а у Li 2 и Ве 2 - из 2s -электронов. 1s -электроны лития и бериллия можно рассматривать как несвязывающие, т.е. принадлежащие отдельным атомам. Здесь будут наблюдаться те же закономерности в изменении порядка связи, энергии диссоциации и магнитных свойств. Ион Li 2 + имеет один неспаренный электрон, расположенный на σ св 2s -орбитали - ион парамагнитен. Появление второго электрона на этой орбитали приведет к увеличению энергии диссоциации молекулы Li 2 и возрастанию кратности связи с 0,5 до 1. Магнитные свойства приобретут диамагнитный характер. Третий s -электрон расположится на σ разр -орбитали, что будет способствовать уменьшению кратности связи до 0,5 и, как следствие этого, понижению энергии диссоциации. Такое электронное строение имеет парамагнитный ион Be 2 + . Молекула Ве 2 , так же как и Hе 2 , существовать не может из-за нулевого порядка связи. У этих молекул число связывающих электронов равно числу разрыхляющих.
Как видно из рисунка, по мере заполнения связывающих орбиталей энергия диссоциации молекул увеличивается, а с появлением электронов на разрыхляющих орбиталях уменьшается. Ряд заканчивается нестабильной молекулой Ne 2 . Из рисунка также видно, что удаление электрона с разрыхляющей орбитали приводит к повышению кратности связи и, как следствие этого, увеличению энергии диссоциации и уменьшению межъядерного расстояния. Ионизация молекулы, сопровождаемая удалением связывающего электрона дает прямо противоположный эффект.
Метод ВС широко используется химиками. В рамках этого метода большая и сложная молекула рассматривается как состоящая из отдельных двухцентровых и двухэлектронных связей. Принимается, что электроны, обусловливающие химическую связь, локализованы (расположены) между двумя атомами. К большинству молекул метод ВС может быть применен с успехом. Однако имеется ряд молекул, к которым этот метод неприменим или его выводы находятся в противоречии с опытом.
Установлено, что в ряде случаев определяющую роль в образовании химической связи играют не электронные пары, а отдельные электроны. На возможность химической связи при помощи одного электрона указывает существование иона H 2 + . При образовании этого иона из атома водорода и иона водорода выделяется энергия в
255 кДж (61 ккал). Таким образом, химическая связь в ионе H 2 + довольно прочная.
Если попробовать описать химическую связь в молекуле кислорода по методу ВС, то придем к заключению, что, во-первых, она должна быть двойной (σ- и p-связи), во-вторых, в молекуле кислорода все электроны должны быть спарены, т.е. молекула О 2 должна быть диамагнитна (у диамагнитных веществ атомы не обладают постоянным магнитным моментом и вещество выталкивается из магнитного поля). Парамагнитным веществом называется то, атомы которого или молекулы обладают магнитным моментом, и оно обладает свойством втягиваться в магнитное поле. Экспериментальные данные показывают, что по энергии связь в молекуле кислорода действительно двойная, но молекула является не диамагнитной, а парамагнитной. В ней имеется два неспаренных электрона. Метод ВС бессилен объяснить это факт.
Метод молекулярных орбиталей (МО) наиболее нагляден в его графической модели линейной комбинации атомных орбиталей (ЛКАО). Метод МО ЛКАО основан на следующих правилах.
1) При сближении атомов до расстояний химических связей из атомных орбиталей (АО) образуются молекулярные.
2) Число полученных молекулярных орбиталей равно числу исходных атомных.
3) Перекрываются атомные орбитали, близкие по энергии. В результате перекрывания двух атомных орбиталей образуются две молекулярные. Одна из них имеет меньшую энергию по сравнению с исходными атомными и называется связывающей , а вторая молекулярная орбиталь обладает большей энергией, чем исходные атомные орбитали, и называется разрыхляющей .
4) При перекрывании атомных орбиталей возможно образование и σ-связи (перекрывание по оси химической связи), и π-связи (перекрывание по обе стороны от оси химической связи).
5) Молекулярная орбиталь, не участвующая в образовании химической связи, носит название несвязывающей . Ее энергия равна энергии исходной АО.
6)На одной молекулярной орбитали (как, впрочем, и атомной) возможно нахождение не более двух электронов.
7)Электроны занимают молекулярную орбиталь с наименьшей энергией (принцип наименьшей энергии).
8)Заполнение вырожденных (с одинаковой энергией) орбиталей происходит последовательно по одному электрону на каждую из них.
Метод молекулярных орбиталей исходит из того, что каждую молекулярную орбиталь представляют в виде алгебраической суммы (линейной комбинации) атомных орбиталей. Например, в молекуле водорода в образовании МО могут участвовать только 1s атомные орбитали двух атомов водорода, которые дают две МО, представляющие собой сумму и разность атомных орбиталей 1s 1 и 1s 2 – МО ± = C 1 1s 1 ±C 2 1s 2 .
Электронная плотность этих двух состояний пропорциональна |MO ± | 2 . Поскольку в молекуле водорода взаимодействие возможно только по оси молекулы, то каждая из MO ± может быть переобозначена как σ св = 1s 1 + 1s 2 и σ* = 1s 1 – 1s 2 и названа соответственно связывающей (σ св) и разрыхляющей (σ*) молекулярными орбиталями.
Из рис. 10 видно, что электронная плотность посередине между ядрами для σ св значительна, а для σ* равна нулю. Отрицательно заряженное электронное облако, сконцентрированное в межъядерном пространстве, притягивает положительно заряженные ядра и соответствует связывающей молекулярной орбитали σ св. А МО с нулевой плотностью в межъядерном пространстве соответствует разрыхляющей орбитали σ*. Состояния σ св и σ* отвечают разным уровням энергии, причем молекулярная орбиталь σ св имеет более низкую энергию по сравнению с исходными АО двух невзаимодействующих атомов водорода 1s 1 и 1s 2 .
Переход двух электронов на МО σ св способствует понижению энергии системы; этот энергетический выигрыш равен энергии связи между атомами в молекуле водорода H–H. Даже удаление одного электрона с МО (σ св) 2 c образованием (σ св) 1 в молекулярном ионе Н 2 + оставляет эту систему более устойчивой, чем отдельно существующие атом H и ион H + .
Применим метод МО ЛКАО и разберем строение молекулы водорода. Изобразим на двух параллельных диаграммах энергетические уровни атомных орбиталей исходных атомов водорода
Видно(см.рис.11 и 12), что имеется выигрыш в энергии по сравнению с несвязанными атомами. Свою энергию понизили оба электрона, что соответствует единице валентности в методе валентных связей (связь образуется парой электронов).
Метод МО ЛКАО позволяет наглядно объяснить образование ионов Н 2 + и Н 2 - (см.рис.13 и 14), что вызывает трудности в методе валентных связей. На σ-связывающую молекулярную орбиталь катиона Н 2 + переходит один электрон атома H с выигрышем энергии. Образуется устойчивое соединение с энергией связи 255кДж/моль. Кратность связи равна ½. Молекулярный ион парамагнитен. Молекула обычного водорода содержит уже два электрона с противоположными спинами на σ cв 1s-орбитали: Энергия связи в Н 2 больше, чем в H 2 + - 435 кДж/моль. В молекуле Н 2 имеется одинарная связь, молекула диамагнитна.
В анионе Н 2 - на двух молекулярных орбиталях необходимо разместить уже три электрона.
Если два электрона, опустившись на связывающую орбиталь, дают выигрыш в энергии, то третьему электрону приходится повысить свою энергию. Однако энергия, выигранная двумя электронами, больше, чем проигранная одним. Такая частица может существовать.,
Известно, что щелочные металлы в газообразном состоянии существуют в виде двухатомных молекул. Попробуем убедиться в возможности существования двухатомной молекулы Li 2 , используя метод МО ЛКАО(рис.15). Исходный атом лития содержит электроны на двух энергетических уровнях – первом и втором (1s
и 2s
).
Перекрывание одинаковых 1s
-орбиталей атомов лития даст две молекулярные орбитали (связывающую и разрыхляющую), которые согласно принципу минимума энергии будут полностью заселены четырьмя электронами. Выигрыш в энергии, получаемый в результате перехода двух электронов на связывающую молекулярную орбиталь, не способен компенсировать ее потери при переходе двух других электронов на разрыхляющую молекулярную орбиталь. Вот почему вклад в образование химической связи между атомами лития вносят лишь электроны внешнего (валентного) электронного слоя.
Перекрывание валентных 2s
-орбиталей атомов лития приведет также к образованию одной σ-связывающей и одной разрыхляющей молекулярных орбиталей. Два внешних электрона займут связывающую орбиталь, обеспечивая общий выигрыш в энергии (кратность связи равна 1).
Используя метод МО ЛКАО, рассмотрим возможность образования молекулы He 2 .
В этом случае два электрона займут связывающую молекулярную орбиталь, а два других – разрыхляющую. Выигрыша в энергии такое заселение двух орбиталей электронами не принесет. Следовательно, молекулы He 2 не существует.
Заполнение молекулярных орбиталей происходит при соблюдении принципа Паули и правила Хунда по мере увеличения их энергии в такой последовательности:
σ1s < σ*1s < σ2s < σ*2s < σ2p z < π2p x = π2p y < π*2p x =π*2p y < σ*2p z
Значения энергии σ2p и π2p близки и для некоторых молекул(В 2 ,С 2 ,N 2) соотношение обратное приведённому: сначала π2p потом σ2p
Таблица 2 Энергия и порядок связи в молекулах элементов 1 периода
Согласно методу МО порядок связи в молекуле определяется разностью между числом связывающих и разрыхляющих орбиталей, деленный на два. Порядок связи может быть равен нулю (молекула не существует), целому или дробному положительному числу. При нулевой кратности связи,как в случае Не 2 ,молекула не образуется.
На рисунке 17 изображена энергетическая схема образования молекулярных орбиталей из атомных для двухатомных гомоядерных (одного и того же элемента) молекул элементов второго периода. Число связывающих и разрыхляющих электронов зависит от их числа в атомах исходных элементов.
Рис.17 Энергетическая диаграмма образования двухатомных молекул
элементов 2 периода
Следует отметить, что при образовании молекул В 2 , С 2 и N 2 энергия связывающей s 2 p x -орбитали больше энергии связывающих p 2 p y - и p 2 p z -орбиталей, тогда как в молекулах О 2 и F 2 , наоборот, энергия связывающих p 2 p y - и p 2 p z -орбиталей больше энергии связывающей s 2 p x -орбитали. Это нужно учитывать при изображении энергетических схем соответствующих молекул.
Подобно электронным формулам, показывающим распределение электронов в атоме по атомным орбиталям, в методе МО составляются формулы молекул, отражающие их электронную конфигурацию. По аналогии с атомными s -, p -, d -, f - орбиталями молекулярные орбитали обозначаются греческими буквами s, p, d,j.
Образование молекул из атомов элементов II периода может быть записано следующим образом (К – внутренние электронные слои):
Li 2
Be 2 молекула не обнаружена, как и молекула Не 2
B 2 молекула парамагнитна
O 2 молекула парамагнитна
Ne 2 молекула не обнаружена
Методом МО ЛКАО легко продемонстрировать парамагнитные свойства молекулы кислорода. С тем чтобы не загромождать рисунок, не будем рассматривать перекрывание 1s -орбиталей атомов кислорода первого (внутреннего) электронного слоя. Учтем, что p -орбитали второго (внешнего) электронного слоя могут перекрываться двумя способами. Одна из них перекроется с аналогичной с образованием σ-связи.
Две других p -АО перекроются по обе стороны от оси x с образованием двух π-связей.
Энергии молекулярных орбиталей могут быть определены по данным спектров поглощения веществ в ультрафиолетовой области. Так, среди молекулярных орбиталей молекулы кислорода, образовавшихся в результате перекрывания p -АО, две π-связывающие вырожденные (с одинаковой энергией) орбитали обладают меньшей энергией, чем σ-связывающая, впрочем, как и π*-разрыхляющие орбитали обладают меньшей энергией в сравнении с σ*-разрыхляющей орбиталью.
В молекуле O 2 два электрона с параллельными спинами оказались на двух вырожденных (с одинаковой энергией) π*-разрыхляющих молекулярных орбиталях. Именно наличием неспаренных электронов и обусловлены парамагнитные свойства молекулы кислорода, которые станут заметными, если охладить кислород до жидкого состояния.
Так, электронная конфигурация молекул О 2 описывается следующим образом:О 2 [КК(σ s) 2 (σ s *) 2 (σ z) 2 (π x) 2 (π y) 2 (π x *) 1 (π y *) 1 ]
Буквами КК показано, что четыре 1 s -электрона (два связывающих и два разрыхляющих) практически не оказывают влияния на химическую связь.
Среди двухатомных молекул одной из наиболее прочных является молекула CO. Метод МО ЛКАО легко позволяет объяснить этот факт.
Энергии АО атома кислорода лежат ниже энергий соответствующих орбиталей углерода (1080 кДж/моль), они расположены ближе к ядру. Результатом перекрывания p
-орбиталей атомов O и C является образование двух вырожденных π-связывающих и одной σ-связывающей орбитали. Эти молекулярные орбитали займут шесть электронов. Следовательно, кратность связи равна трем. Электронная конфигурация такая же, как и у N 2:
[КК(σ s) 2 (σ s *) 2 (σ z) 2 (π x) 2 (π y) 2 (σ z) 2 ] . Прочность связи в молекулах СО(1021кДж/моль) и N 2 (941кДж/моль) близки.
При удалении одного электрона,который уходит со связывающей орбиты (образование иона CO +)б прочность связи уменьшается до 803 кДж/моль. Кратность связи становится равной 2,5.
Метод МО ЛКАО можно использовать не только для двухатомных молекул, но и для многоатомных. Разберем в качестве примера в рамках данного метода строение молекулы аммиака.
Поскольку три атома водорода имеют только три 1s -орбитали, то суммарное число образованных молекулярных орбиталей будет равно шести (три связывающих и три разрыхляющих). Два электрона атома азота окажутся на несвязывающей молекулярной орбитали (неподеленная электронная пара).
Наилучшим способом квантовомеханической трактовки химической связи в настоящее время считается метод молекулярных орбиталей (МО). Однако он гораздо сложнее метода ВС и не столь нагляден, как последний.
Существование связывающих и разрыхляющих МО подтверждается физическими свойствами молекул. Метод МО позволяет предвидеть, что если при образовании молекулы из атомов электроны в молекуле попадают на связывающие орбитали, то потенциалы ионизации молекул должны быть больше, чем потенциалы ионизации атомов, а если электроны попадают на разрыхляющие орбитали, то наоборот.Так, потенциалы ионизации молекул водорода и азота (связывающие орбитали) – 1485 и 1500 кДж/моль соответственно – больше, чем потенциалы ионизации атомов водорода и азота – 1310 и 1390 кДж/моль, а потенциалы ионизации молекул кислорода и фтора (разрыхляющие орбитали) – 1170 и 1523 кДж/моль – меньше, чем у соответствующих атомов – 1310 и 1670 кДж/моль. При ионизации молекул прочность связи уменьшается, если электрон удаляется со связывающей орбитали (H 2 и N 2), и увеличивается, если электрон удаляется с разрыхляющей орбитали(О 2 и F 2).
Рассмотрим образование МО в молекуле фтористого водорода HF. Поскольку потенциал ионизации фтора (17,4 эВ или 1670 кДж/моль) больше, чем у водорода (13,6 эВ или 1310 кДж/моль), то 2р-орбитали фтора имеют меньшую энергию, чем 1s-орбиталь водорода. Вследствие большого различия энергий 1s-орбиталь атома водорода и 2s-орбиталь атома фтора не взаимодействуют. Таким образом, 2s-орбиталь фтора становится без изменения энергии МО в HF. Такие орбитали называются несвязывающими. 2р у - и 2р z –орбитали фтора также не могут взаимодействовать с 1s-орбиталью водорода вследствие различия симметрии относительно оси связи. Они тоже становятся несвязывающими МО. Связывающая и разрыхляющая МО образуются из 1s-орбитали водорода и 2р х -орбитали фтора. Атомы водорода и фтора связаны двухэлектронной связью с энергией 560 кДж/моль.
Рассмотренные выше недостатки МВС способствовали развитию другого квантовомеханического метода описания химической связи, который получил название метода молекулярных орбиталей (ММО) . Основные принципы данного метода были заложены Ленардом-Джонсом, Гундом и Малликеном. В его основе лежит представление о многоатомной частице как о единой системе ядер и электронов. Каждый электрон в такой системе испытывает притяжение со стороны всех ядер и отталкивание со стороны всех других электронов. Такую систему удобно описывать при помощи молекулярных орбиталей , которые являются формальными аналогами атомных орбиталей. Отличие атомных и молекулярных орбиталей заключается в том, что одни описывают состояние электрона, находящегося в поле единственного ядра, а другие состояние электрона в поле нескольких ядер. Учитывая аналогичность подхода к описанию атомных и молекулярных систем, можно сделать вывод, что орбитали n-атомной молекулы должны обладать следующими свойствами:
а) состояние каждого электрона в молекуле описывается волновой функцией ψ, а величина ψ 2 выражает вероятность нахождения электрона в любом единичном объёме многоатомной системы; указанные волновые функции называют молекулярными орбиталями (МО) и они, по определению, являются многоцентровыми, т.е. описывают движение электрона в поле всех ядер (вероятность нахождения в любой точке пространства);
б) каждая молекулярная орбиталь характеризуется определённой энергией;
в) каждый электрон в молекуле имеет определённое значение спинового квантового числа, принцип Паули в молекуле выполняется;
г) молекулярные орбитали конструируются из атомных, путём линейной комбинации последних: ∑с n ψ n (если общее число использованных при суммировании фолновых функций равно k, то n принимает значения от 1 до k), с n – коэффициенты;
д)минимум энергии МО достигают при максимальном перекрывании АО;
е) чем ближе по энергии исходные АО, тем ниже энергия МО, сформированных на их основе.
Из последнего положения можно сделать вывод, что внутренние орбитали атомов, имеющие очень низкую энергию, практически не будут принимать участия в образовании МО и их вкладом в энергию этих орбиталей можно пренебречь.
С учётом описанных выше свойств МО рассмотрим их построение для двухатомной молекулы простого вещества, например для молекулы Н 2 . Каждый из атомов, составляющих молекулу (Н А и Н В) имеют по одному электрону на 1s орбитале, тогда МО можно представить в виде:
Ψ МО = с А ψ А (1s) + с В ψ В (1s)
Так как в рассматриваемом случае атомы, образующие молекулу идентичны, нормирующие множители (с), показывающие долю участия АО при конструировании МО, равны по абсолютному значению и, следовательно возможны два варианта Ψ МО при с А = с В и с А = - с В:
Ψ МО(1) = с А ψ А (1s) + с В ψ В (1s) и
Ψ МО(2) = с А ψ А (1s) - с В ψ В (1s)
Молекулярная орбиталь Ψ МО(1) соответствует состоянию с более высокой электронной плотностью между атомами по сравнению с изолированными атомными орбиталями, а электроны располагающиеся на ней и имеющие противоположные значения спинов в соответствии с принципом Паули – более низкую энергию по сравнению с их энергией в атоме. Такая орбиталь в ММО ЛКАО называется связывающей.
В то же время молекулярная орбиталь Ψ МО(2) представляет собой разность волновых функций исходных АО, т.е. характеризует состояние системы с пониженной электронной плотностью в межъядерном пространстве. Энергия такой орбитали выше, чем исходных АО и нахождения на ней электронов приводит к росту энергии системы. Такие орбитали носят название разрыхляющих. На рисунке 29.3 показано формирование связывающей и разрыхляющей орбиталей в молекуле водорода.
Рис.29.3. Образование σ - связывающей и σ-разрыхляющей орбиталей в молекуле водорода.
Ψ МО(1) и Ψ МО(2) имеют цилиндрическую симметрию относительно оси, проходящей через центры ядер. Орбитали такого типа называются σ – симметричными и записываются: связывающая – σ1s, разрыхляющая - σ ٭ 1s . Таким образом молекуле водорода в основном состоянии отвечает конфигурация σ1s 2 , а конфигурации иона Не 2 + , который образуется в электрическом разряде, в основном состоянии может быть записана в виде σ1s 2 σ ٭ 1s (рис. 30.3).

Рис. 30.3. Энергетическая диаграмма образования связующей и разрыхляющей орбиталей и электронное строение молекул и ионов элементов первого периода.
В молекуле Н 2 оба электрона занимают связывающую орбиталь, что приводит к снижению энергии системы по сравнению с исходной (два изолированных атома водорода). Как уже отмечалось энергия связи в этой молекуле 435 кДж/моль, а длина связи равна 74 пм. Удаление электрона со связывающей орбитали повышает энергию системы (понижает стабильность продукта реакции по сравнению с прекурсором): энергия связи в Н 2 + составляет 256 кДж/моль, а длина связи увеличивается до 106 пм. В частице Н 2 - число электронов увеличивается до трёх, поэтому один из них располагается на разрыхляющей орбитали, что приводит к дестабилизации системы по сравнению с ранее описанными: Е(Н 2 -) = 14,5 кДж/моль. Следовательно, появление электрона на разрыхляющей орбитали в большей степени влияет на энергию химической связи, чем удаление электрона со связывающей орбитали. Приведённые выше данные свидетельствуют о том, что суммарная энергия связи определяется разностью между числом электронов на связывающих и разрыхляющих орбиталях. Для бинарных частиц эта разность, делённая пополам называется порядком связи:
ПС = (ē св – ē несв.)/2
Если ПС равен нулю, то химическая связь не образуется (молекула Не 2 рис 30.3). Если в нескольких системах число электронов на разрыхляющих орбиталях одинаково, то наибольшую стабильность имеет частица с максимальным значением ПС. В то же время при одинаковом значении ПС более стабильна частица с меньшим числом электронов на разрыхляющих орбиталях (например, ионы Н 2 + и Н 2 -). Из рисунка 30.3 следует и ещё один вывод: атом гелия может образовывать химическую связь с ионом Н + . Несмотря на то, что энергия 1s орбитали Не очень низка (- 2373 кДж/моль), её линейная комбинация с 1s орбиталью атома водорода (Е =-1312 кДж/моль) приводит к образованию связывающей орбитали, энергия которой ниже АО гелия. Так как на разрыхляющих орбиталях частицы НеН + нет электронов, она более стабильна, по сравнению с системой образованной атомами гелия и ионами водорода.
Аналогичные рассуждения применимы и к линейным комбинациям атомных р-орбиталей. Если ось z совпадает с осью, проходящей через центры ядер, как показано на рисунке 31.3, то связывающая и разрыхляющая орбитали описываются уравнениями:
Ψ МО(1) = с А ψ А (2р z) + с В ψ В (2р z) и Ψ МО(2) = с А ψ А (2р z) - с В ψ В (2р z)
Когда МО конструируются из р-орбиталей, оси которых перпендикулярны линии соединяющей атомные ядра, то происходит образование π-связывающих и π-разрыхляющих молекулярных орбиталей рис.32.3. Молекулярные π у 2р и π у ٭ 2р- орбитали аналогичны представленным на рис. 32.3, но повёрнуты относительно первых на 90 о. Таким образом π2р и π ٭ 2р- орбитали дважды вырождены.
Следует отметить, что линейную комбинацию можно строить не из любых АО, а только из тех, которые обладают достаточно близкой энергией и перекрывание которых возможно с геометрической точки зрения. Парами таких орбиталей пригодными для образования σ-связывающих σ-разрыхляющих орбиталей могут s – s, s – p z , s – d z 2 , p z – p z , p z – d z 2 , d z 2 - d z 2 , тогда как при линейной комбинации p x – p x , p y – p y , p x – d xz , p y – d yz , образуются молекулярные π-связывающие и π-разрыхляющие молекулярных орбитали.
Если же строить МО из АО типа d x 2- y 2 - d x 2- y 2 или d xy - d xy то образуются δ-МО. Таким образом, как отмечалось выше, деление МО на σ,π и δ предопределяется их симметрией относительно линии соединяющей атомные ядра. Таким образом, для σ-МО число узловых плоскостей равно нулю, π-МО имеет одну такую плоскость, а δ-МО – две.
Для описания в рамках ММО ЛКАО гомоатомных молекул второго периода необходимо учесть, что линейная комбинация атомных орбиталей возможна только в том случае, когда АО орбитали близки по энергии и обладают одинаковой симметрией.

Рис.31.3. Образование σ-связывающих σ-разрыхляющих орбиталей из атомных р-орбиталей

Рис.32.3.Образование π-связывающих и π-разрыхляющих молекулярных орбиталей из атомных р-орбиталей.
Из орбиталей второго периода одинаковой симмерией относительно оси z обладают орбитали 2s и 2p z . Различие в их энергиях для атомов Li, Be, B и C относительно невелико, поэтому волновые функции 2s и 2p в данном случае могут смешиваться. Для атомов O и F различия в энергии 2s и 2p значительно больше, поэтому их смешение не происходит (таблица 4.3)
Таблица 4.3.
∆Е энергии между 2s и 2p орбиталями различных элементов
Согласно данными таблицы 4.3, а также проведённых расчётов показано, что относительная энергия МО различна для молекул Li 2 – N 2 c одной стороны и для молекул О 2 – F 2 c другой. Для молекул первой группы порядок возрастания энергии МО можно представить в виде ряда:
σ2sσ ٭ 2sπ2p x π2p y σ2p z π٭2p x π ٭ 2p y σ ٭ 2p z , а для молекул О 2 и F 2 в виде:
σ2sσ ٭ 2sσ2p z π2p x π2p y π٭2p x π ٭ 2p y σ ٭ 2p z (рис 33.3).
Орбитали типа 1s имеющих очень низкую энергию по сравнения с орбиталями второго энергетического уровня, переходят в молекулу в неизменном виде, т.е остаются атомными и на энергетической диаграмме молекулы не указываются.
На основе энергетических диаграмм молекул и молекулярных ионов можно сделать выводы о стабильности частиц и их магнитных свойствах. Так о стабильности молекул, МО которых конструируются из одинаковых АО, ориентировочно можно судить по значению порядка связи, а о магнитных свойствах – по числу неспаренных электронов на МО (рис.34.3).
Необходимо отметить, что АО орбитали не валентных, внутренних уровней с точки зрения ММО ЛКАО не принимают участия в образовании МО, но оказывают заметное влияние на энергию связи. Так, например, при переходе от Н 2 к Li 2 энергия связи понижается более чем в четыре раза (с 432 кДж/моль до 99 кДж/моль).

Рис.33.3 Распределение МО по энергии в молекулах (а) О 2 и F 2 и (б) Li 2 – N 2 .

Рис.34.3 Энергетические диаграммы бинарных молекул элементов второго периода.
Отрыв электрона от молекулы Н 2 снижает энергию связи в системе до 256 кДж/моль, что вызвано уменьшением числа электронов на связывающей орбитали и снижением ПС с 1 до 0,5. В случае же отрыва электрона от молекулы Li 2 энергия связи возрастает со 100 до 135,1 кДж/моль, хотя как видно из рисунка 6.9, электрон, также как в предыдущем случае удаляется со связывающей орбитали и ПС снижается до 0,5. Причина этого заключается в том, что при удалении электрона из молекулы Li 2 снижается отталкивание между электронами, находящимися на связывающей МО и электронами занимающими внутреннюю 1s орбиталь. Эта закономерность наблюдается для молекул всех элементов главной подгруппы первой группы Периодической системы.
По мере увеличения заряда ядра влияние электронов 1s орбиталь на энергию МО снижается, потому в молекулах В 2 , С 2 и N 2 отрыв электрона будет повышать энергию системы (снижение значения ПС, уменьшение суммарной энергии связей) из за того, что электрон удаляется со связывающей орбитали. В случае же молекул O 2 , F 2 и Ne 2 удаление электрона происходит с разрыхляющей орбитали, что ведёт к росту ПС и суммарной энергии связи в системе, например, энергия связи в молекуле F 2 равна 154,8 кДж/моль, а в ионе F 2 + практически в два раза выше (322,1 кДж/моль). Приведённые рассуждения справедливы для любых молекул, независимо от их качественного и количественного состава. Рекомендуем читателю провести сравнительный анализ стабильности бинарных молекул и их отрицательно заряженных молекулярных ионов, т.е. оценить изменение энергии системы в процессе А 2 + ē = А 2 - .
Из рисунка 34.3 также следует, что только молекулы В 2 и О 2 , имеющие неспаренные электроны, парамагнитны, тогда как остальные бинарные молекулы элементов второго периода относятся к диомагнитным частицам.
Доказательством справедливости ММО, т.е. свидетельством реального существования уровней энергии в молекулах, служит различие в значениях потенциалов ионизации атомоа и образованных из них молекул (таблица 5.3).
Таблица 5.3.
Потенциалы ионизации атомов и молекул
|
атом |
первый потенциал ионизации кДж/моль |
молекула |
первый потенциал ионизации кДж/моль |
|
H 2 | |||
|
N 2 | |||
|
O 2 | |||
|
C 2 | |||
|
F 2 |
Представленные в таблице данные свидетельствуют о том, что у одних молекул потенциалы ионизации больше, чем у атомов из которых они образованы, у других – меньше. Данный факт необъясним с точки зрения МВС. Анализ данных рисунка 34.3 приводит к выводу, что потенциал молекулы больше чем у атома в том случае, когда электрон удаляется со связывающей орбитали (молекулы Н 2 , N 2 , С 2). Если же электрон удаляется с разрыхляющей МО (молекулы О 2 и F 2), то этот потенциал будет меньше, по сравнению с атомным.
Переходя к рассмотрению гетероатомных бинарных молекул в рамках ММО ЛКАО, необходимо напомнить, что орбитали атомов различных элементов, имеющие одинаковые значения главного и побочного квантовых чисел отличаются по своей энергии. Чем выше эффективный заряд ядра атома по отношению к рассматриваемым орбиталям, тем ниже их энергия. На рисунке 35.3 приведена энергетическая диаграмма МО гетероатомных молекул типа АВ, в которой атом В более электроотрицателен. Орбитали этого атома по энергии ниже аналогичных орбиталей атома А. В связи с этим вклад орбиталей атома В в связывающие МО будет больше, чем в разрыхляющие. Наоборот, основной вклад в разрыхляющие МО будут вносить АО атома А. Энергия внутренних орбиталей обоих атомов при образовании молекулы практически не изменяется, например, в молекуле фтороводорода орбитали 1s и 2s атома фтора сосредоточены вблизи его ядра, что, в частности, обуславливает полярность данной молекулы (µ = 5,8 ∙ 10 -30). Рассмотрим с использованием рисунка 34 описание молекулы NO. Энергия АО кислорода ниже АО азота, вклад первых выше в связывающие орбитали, вторых – в разрыхляющие. Орбитали 1s и 2s обоих атомов не изменяют свою энергию (σ2s и σ ٭ 2s заняты электронными парами, σ1s и σ ٭ 1s на рисунке не показаны). На 2р орбиталях атомов, соответственно, кислорода и азота находятся четыре и три электрона. Общее число этих электронов 7, а связующих орбиталей образованных за счёт 2р орбиталей три. После их заполнения шестью электронами становится очевидным, что седьмой электрон в молекуле расположен на одной из разрыхляющих π-орбиталей и, следовательно локализован вблизи атома азота. ПС в молекуле: (8 – 3)/2 = 2,5 т.е. суммарная энергия связи в молекуле высокая. Однако электрон расположенный на разрыхляющей орбитали имеет большую энергию и его удаление из системы приведёт к её стабилизации. Указанный вывод позволяет прогнозировать, что энергия активации процессов окисления NO будет низкой, т.е. эти процессы могут протекать даже при с.у..
В то же время, термическая стабильность этих молекул будет высокой, ион NO + по суммарной энергии связи будет близок к молекулам азота и СО, при низких температурах NO будет димеризоваться.
Анализ молекулы NO в рамках данного метода приводит к ещё одному важному выводу – наиболее стабильными будут бинарные гетероатомные молекулы, в состав которых входят атомы с суммарным числом электронов на валентных s и р-орбиталях, равных 10. В этом случае ПС = 3. Увеличение или уменьшение этого числа приведёт к уменьшению значения ПС, т.е. к дестабилизации частицы.
Многоатомные молекулы в ММО ЛКАО рассматриваются исходя из тех же принципов, которые описаны выше для духатомных частиц. Молекулярные орбитали в данном случае формируют путём линейной комбинации АО всех атомов, входящих в состав молекулы. Следовательно, МО в таких частицах многоцентровые, делокализованные и описывают химическую связь в системе как единое целое. Равновесные расстояния между центрами атомов в молекуле, отвечают минимуму потенциальной энергии системы.

Рис.35.3. Энергетическая диаграмма МО бинарных гетероатомных молекул
(атом В имеет большую электроотрицательность).

Рис.36.3.Энергетические диаграммы молекул различных типов в
рамках ММО. (ось р х орбитали совпадает с осью связей)
На рисунке 36.3 представлены МО молекул различных типов. Принцип их построения рассмотрим на примере молекулы ВеН 2 (рис.37.3). В образовании трёхцентровых МО в данной частице принимают участие 1s орбитали двух атомов водорода, а также 2s и 2р орбитали атома Ве (1s орбиталь этого атома в образовании МО участия не принимает и локализована вблизи его ядра). Примем, что ось р z -орбитали Ве совпадает с линией связи в рассматриваемой частице. Линейная комбинация s орбиталей атомов водорода и бериллия приводит к образованию σ s и σ s ٭ , а такая же операция с участием s орбиталей атомов водорода и р z -орбитали Ве к образованию связывающей и разрыхляющей МО σ z и σ z ٭ , соответсвенно.

Рис.37.3. МО в молекуле ВеН 2
Валентные электроны располагаются в молекуле на связывающих орбиталях, т.е. её электронная формула может быть представлена в виде (σ s) 2 (σ z) 2 . Энергия этих связывающих орбиталей ниже энергии орбиталей атома Н, что обеспечивает относительную стабильность рассматриваемой молекулы.
В том случае, когда все системы атомы имеют подходящие для линейной комбинации р-орбитали, наряду с σ-МО, образуются многоцентровые связывающие, несвязывающие и разрыхляющие π-МО. Рассмотрим такие частицы на примере молекулы СО 2 (рис.38.3 и 39.3).

Рис.38.3 Связывающие и разрыхляющие σ-МО молекулы СО 2

Рис.39.3. Энергетическая диаграмма МО в молекуле СО 2 .
В этой молекуле σ-МО образуются при комбинации 2s и 2р х орбиталей атома углерода с 2р х орбиталями атомов кислорода. Делокализованные π-МО формируются за счёт линейной комбинации p y и p z орбиталей всех атомов,
входящих в состав молекулы. В результате этого образуется три пары π-МО с различной энергией: связывающие - π y c в π z св, несвязывающие - π y π z (по энергии соответствующие р-орбиталям атомов кислорода), и разрыхляющие - π y разр π z разр.
При рассмотрении молекул в рамках ММО ЛКАО часто используют сокращённые схемы описания частиц (рис.40.3). При формировании МО, например, в молекуле BCI 3 достаточно указать только те АО, которые принимают реальное участие в линейной комбинации (на рисунке не указаны одна из АО р-орбиталей бора и 6 из 9 р-орбиталей атомов хлора, линейная комбинация которых даёт несвязывающие МО)

Рис.40.3. МО в молекуле BCI 3
Энергетическая диаграмма МО в молекуле СН 4 представлена на рис.41.3.. Анализ электронного строения атома углерода показывает, что в связи с разнонаправленностью его 2р орбиталей образование в молекуле СН 4 пятицентровых МО с участием этих АО невозможно по геометрически соображениям. В то же время, 2s орбиталь углерода в равной степени способна перекрываться с 1s орбиталями атомов водорода, в результате чего образуется пятицентровые σ s и σ s ٭ МО. В случае комбинаций 2р и 1s орбиталей, число атомных функций в линейной комбинации равно только трём, т.е. энергия σ-МО в данном случае будет выше, чем у соответствующих σ s и σ s ٭ .

Рис.41.3.. Энергетическая диаграмма МО молекулы СН 4 .
Различную энергию пятицентровой и трёхцентровых связывающих орбиталей подтверждают экспериментальные данные по потенциалам ионизации, которые различны для электронов удаляющихся с σ s и с σ x (σ y . σ z).
Хронологически метод МО появился позже метода ВС, поскольку оставались в теории ковалентной связи вопросы, которые не могли получить объяснение методом ВС. Укажем некоторые из них.
Как известно, основное положение метода ВС состоит в том, что связь между атомами осуществляется за счет электронных пар (связующих двухэлектронных облаков). Но это не всегда так. В ряде случаев в образовании химической связи участвуют отдельные электроны. Так, в молекулярном ионе Н 2 + одноэлектронная связь. Метод ВС образование одноэлектронной связи объяснить не может, она противоречит его основному положению.
Метод ВС не объясняет также роли неспаренных электронов в молекуле. Молекулы, имеющие неспаренные электроны, парамагнитны , т. е. втягиваются в магнитное поле, так как неспаренный электрон создает постоянный магнитный момент. Если в молекулах нет неспаренных электронов, то они диамагнитны – выталкиваются из магнитного поля. Молекула кислорода парамагнитна, в ней имеется два электрона с параллельной ориентацией спинов, что противоречит методу ВС. Необходимо также отметить, что метод ВС не смог объяснить ряд свойств комплексных соединений – их цветность и др.
Чтобы объяснить эти факты, был предложен метод молекулярных орбиталей (ММО).
4.5.1. Основные положения ммо, мо.
1. В молекуле все электроны являются общими. Сама молекула - это единое целое, совокупность ядер и электронов.
2. В молекуле каждому электрону соответствует молекулярная орбиталь, подобно тому как каждому электрону в атоме соответствует атомная орбиталь. И обозначения орбиталей аналогичны:
АО s, p, d, f
МО σ, π, δ, φ
3. В первом приближении молекулярная орбиталь представляет собой линейную комбинацию (сложение и вычитание) атомных орбиталей. Поэтому говорят о методе МО ЛКАО (молекулярная орбиталь есть линейная комбинация атомных орбиталей), при которой из N АО образуется N МО (это основное положение метода).
Рис. 12. Энергетическая
схема образования моле-
кулы водорода Н 2
Рассмотрение химических связей в методе МО заключается в распределении электронов в молекуле по ее орбиталям. Последние заполняются в порядке возрастания энергии и с учетом принципа Паули. В этом методе предполагается увеличение электронной плотности между ядрами при образовании ковалентной связи.Пользуясь положениями 1-3, объясним образование молекулы H 2 с точки зрения метода МО. При достаточном сближении атомов водорода происходит перекрывание их электронных орбиталей. Согласно п. 3 из двух одинаковых ls-орбиталей образуются две молекулярные орбитали: одна из них от сложения атомных орбиталей, другая от их вычитания (рис.12). Энергия первой E 1 < E 2 , а энергия второй E 2 < E 3 .
Молекулярная
орбиталь, энергия которой меньше энергии
атомной орбитали изолированного
атома, называется связывающей
(обозначается символом
 св),
а находящиеся на ней электроны-связывающими
электронами.
св),
а находящиеся на ней электроны-связывающими
электронами.
Молекулярная
орбиталь, энергия которой больше энергии
атомной орбитали, называется антисвязывающей
или разрыхляющей
(обозначается символом
 разр),
а находящиеся на ней электроны -
разрыхляющими
электронами.
разр),
а находящиеся на ней электроны -
разрыхляющими
электронами.
Если у соединяющихся атомов водорода спины электронов антипараллельны, то они займут связывающую МО, возникает химическая связь (рис. 12), сопровождающаяся выделением энергии E 1 (435 кДж/моль). Если же спины электронов атомов водорода параллельны, то они в соответствии с принципом Паули не могут разместиться на одной молекулярной орбитали: один из них разместится на связывающей, а другой на разрыхляющей орбитали, значит химическая связь образоваться не может.
Согласно методу МО образование молекул возможно, если число электронов на связывающих орбиталях больше числа электронов на разрыхляющих орбиталях. Если же число электронов на связывающих и разрыхляющих орбиталях одинаково, то такие молекулы образоваться не могут. Так, теория не допускает существования молекулы Нe 2 , так как в ней два электрона находились бы на связывающей орбитали и два - на разрыхляющей. Всегда разрыхляющий электрон сводит на нет действие связывающего электрона.
В системе обозначений метода МО реакцию образования молекулы водорода из атомов записывают так:
2H = H 2 [(σ CB 1s) 2 ],
т.е. используются символы, выражающие размещение электронов на атомных и молекулярных орбиталях. При этом символ каждой МО заключается в круглые скобки и над скобками справа проставляется число электронов на этой орбитали.
Число валентных связей определяется по формуле:

где: В – число связей;
N СВ N РАЗР – соответственно число связывающих и разрыхляющих электронов в молекуле.
В молекуле водорода В = (2-0) : 2=1, водород одновалентен. Молекула Н 2 диамагнитна (электроны спарены).
Теперь
легко объясняется одноэлектронная
связь в молекулярном ионе Н 2 +
(рис.13). Единственный электрон этого
иона занимает энергетически наиболее
выгодную орбиталь
 св 1s.
Уравнение процесса:
св 1s.
Уравнение процесса:
H + H + = H 2 + [(σ св 1s) 1 ], ∆H = - 259,4 кДж


Рис. 13. Энергетическая схема Рис. 14. Энергетическая схема
образования молекулярного образования дигелий-иона Hе 2
иона водорода H 2
Число связей в ионе H 2 + равно ½ (связь одним электроном). Ион H 2 + - парамагнитен (имеет один неспаренный электрон).
Возможно существование молекулярного дигелий иона Не 2 + (рис.14). Уравнение его образования
He + He + = He 2 + [(σ CB 1s) 2 (σ разр 1s) 1 ], ∆H = - 292,8 кДж
Этот
ион экспериментально обнаружен. Число
связей в нем
Рис.
15 . Энергетическая схема образования
двухатомных гомонуклеарных молекул
элементов
второго
периода
4.5.2. Основные двухатомные гомонуклеарные молекулы элементов 2-го периода. Рассмотренный принцип построения МО из двух одинаковых АО сохраняется при построении гомонуклеарных молекул элементов 2-го периода системы Д.И. Менделеева. Они образуются в результате взаимодействия 2s- и 2р x -, 2р y - и 2р z -орбиталей.
Участием внутренних электронов 1s-орбиталей можно пренебречь (на последующих энергетических схемах они не учтены). 2s-орбиталь одного атома взаимодействует только с 2s-орбиталью другого атома (должна быть близость значений энергий взаимодействующих орбиталей), образуя МО σ 2 s св и σ 2 s разр. При перекрывании (взаимодействии) 2р-орбиталей обоих атомов образуются МО: σ х св, σ х разр, π у св, π у разр, π z св, π z разр
(
Рис.
16. Энергети-ческая схема об-разования
моле-кулы Li 2
 ,
а из р у -
и р z -
– буквой
,
а из р у -
и р z -
– буквой
 .
С помощью рис. 15 легко представить
электронные конфигурации этих молекул
в системе обозначений метода МО.
.
С помощью рис. 15 легко представить
электронные конфигурации этих молекул
в системе обозначений метода МО.
Пример 1. Молекула лития Li 2 . Схема ее образования представлена на рис.16. В ней два связывающих электрона, молекула диамагнитна (электроны спарены). Написание уравнения и формулы можно упростить, обозначив внутренний уровень через K:
2Li = Li 2
Число связей равно 1.
Пример 2. Молекула бериллия Be 2 . Восемь электронов молекулы размещены на МО следующим образом:
Ве 2
Как видно, число связей в молекуле равно нулю: два разрыхляющих электрона уничтожают действие двух связывающих. Такая молекула не может существовать, и она до сих пор не обнаружена. Необходимо отметить, что невозможны двухатомные молекулы у всех элементов IIА-группы, палладия и инертных элементов, так как их атомы имеют замкнутую электронную структуру.
Пример 3. Молекула азота N 2 (рис. 17). Распределение 14 электронов по МО записывается так:
N 2 [(σ CB 1s) 2 (σ разр 1s) 2 (σ CB 2s) 2 (σ разр 2s) 2 (π CB 2p y) 2 (π CB 2p z) 2 (σ CB 2p x) 2 ]
или сокращенно:
N 2 [КК (σ s CB)2 (σ s разр)2(π y CB)2(π z CB)2(σ x CB)2]
1 -1 +1 +1 +1=3

Рис. 17. Энергетическая схема образования молекулы N 2
Под формулой указано число связей в молекуле, исходя из расчета, что два электрона, расположенные на одной МО, образуют валентную связь; знак плюс обозначает связующие орбитали, знак минус – разрыхляющие. Число связей в молекуле 3. нет неспаренных электронов – молекула диамагнитна.
Пример 4. Молекула O 2 (рис. 18). Электроны размещаются по МО в последовательности:
O 2 [КК(σ s CB)2(σ s разр)2(π y CB)2(π z CB)2(σ x CB)2(π y разр)1(π z разр)1]
1 -1 +1 +1 +1 - 1 / 2 - 1 / 2 =2

Рис. 18. Энергетическая схема образования молекулы O 2
В молекуле две валентные связи. Послед-ние два электрона размес-тились на различных π-разрыхляющих орбиталях в соответствии с правилом Гунда. Два неспаренных электрона обусловливают парамагнетизм молекулы кислорода.4.5.3. Двухатомные гетеронуклеарные молекулы элементов 2-го периода. Энергетическая схема образования МО гетеронуклеарных двухатомных молекул, состоящих из атомов элементов 2-го периода, представлена на рис. 19. Она сходна со схемой образования МО гомонуклеарных молекул.
Основное
различие сводится к тому, что значения
энергии одноименных орбиталей атомов
разных элементов не равны между собой,
поскольку различны заряды ядер атомов.
В качестве примера рассмотрим электронную
валентную конфи-гурацию молекул СО и
NO.
Рис.
19 . Энергетическая схема образования
двух атомных гетеро-нуклеарных молекул
элементов второго периода
СО[КК(σ s CB)2 (σ s разр)2(π y CB)2(π z CB)2 (σ х CB)2]
1 -1 +1 +1 +1=3
Как и предусматривалось теорией ВС, в молекуле СО три валентные связи (сравните с N 2). Молекула диамагнитна – все электроны спарены.
Пример 6. Молекула NO. На МО молекулы оксида азота (II) должны разместиться 11 электронов: пять азота – 2s 2 2p 3 и шесть кислорода – 2s 2 2p 4 . Десять изних размещаются так же, как и электроны молекулы оксида углерода (II) (пример 5), а одиннадцатый разместится на одной из разрыхляющих орбиталей – π y разр или π Z разр (эти орбитали энергетически эквивалентны между собой). Тогда
NО[КК(σ s CB)2(σ s разр)2(π y CB)2(π z CB)2(σ х CB)2(π y разр)1]
1 -1 +1 +1 +1 - 1 / 2 =2 1 / 2
Значит, молекула NO имеет две с половиной валентные связи, энергия связи большая - 677,8кДж/моль. Она парамагнитна, так как содержит один неспаренный электрон.
Приведенные примеры служат иллюстрацией возможностей метода МО в объяснении строения и свойств молекул.
Пример 7. Какую валентность, обусловленную неспаренными электронами (спинвалентность), может проявлять фосфор в нормальном и возбужденном состояниях?
Решение.
Распределение электронов внешнего
энергетического уровня фосфора 3s 2 3р 3
(учитывая правило Хунда,
 )
по квантовым
ячейкам имеет вид:
)
по квантовым
ячейкам имеет вид:
3s 3рx 3py 3pz
Атомы фосфора имеют свободные d-орбитали, поэтому возможен переход одного 3s-электрона в 3d-состояние:
3s 3px 3py 3pz 3dxy
Отсюда валентность (спинвалентность) фосфора в нормальном состоянии равна трем, а в возбужденном - пяти.
Пример 8 . Что такое гибридизация валентных орбиталей? Какое строение имеют молекулы типа АВ n , если связь в них образуется за счет sp -, sp 2 -, sp 3 -гибридизации орбиталей атома А?
Решение. Теория валентных связей (ВС) предполагает участие в образовании ковалентных связей не только чистых АО, но и смешанных, так называемых гибридных, АО. При гибридизации первоначальная форма и энергия орбиталей (электронных облаков) взаимно изменяются и образуются орбитали (облака) новой одинаковой формы и с одинаковой энергией. Число гибридных орбиталей (q) равно числу исходных. Ответ см. в табл. 13.
Как было показано в предыдущих параграфах, метод ВС позволяет понять способность атомов к образованию определенного числа ковалентных связей, объясняет направленность ковалентной связи, дает удовлетворительное описание структуры и свойств большого числа молекул. Однако в ряде случаев метод ВС не может объяснить природу образующихся химических связей или приводит к неверным заключениям о свойствах молекул.
Так, согласно методу ВС, все ковалентные связи осуществляются общей парой электронов. Между тем, еще в конце прошлого века было установлено существование довольно прочного молекулярного иона водорода : энергия разрыва связи составляет здесь . Однако никакой электронной пары в этом случае образоваться не может, поскольку в состав иона входит всего один электрон. Таким образом, метод ВС не дает удовлетворительного объяснения существованию иона .

Согласно такому описанию, молекула не содержит неспаренных электронов. Однако магнитные свойства кислорода указывают на то, что в молекуле имеются два неспаренных электрона.
Каждый электрон, благодаря наличию у него спина, создает собственное магнитное поле. Направление этого поля определяется направлением спина, так что магнитные поля, образованные двумя спареиными электронами, взаимнокомпенсируют друг друга.
Поэтому молекулы, в состав которых входят только спаренные электроны, не создают собственного магнитного поля. Вещества, состоящие из таких молекул, являются диамагнитными - они выталкиваются из магнитного поля. Напротив, вещества, молекулы которых содержат неспаренные электроны, обладают собственным магнитным полем и являются парамагнитными; такие вещества втягиваются в магнитное поле.
Кислород - вещество парамагнитное, что свидетельствует о наличии в его молекуле неспаренных электронов.
На основе метода ВС трудно объяснить и то, что отрыв электронов от некоторых молекул приводит к упрочнению химической связи. Так, энергия разрыва связи в молекуле составляет , а в молекулярном ионе - ; аналогичные величины для молекул и молекулярного иона составляют соответственно 494 и .
Приведенные здесь и многие другие факты получают более удовлетворительное объяснение на основе метода молекулярных орбиталей (метод МО).
Мы уже знаем, что состояние электронов в атоме описывается квантовой механикой как совокупность атомных электронных орбиталей (атомных электронных облаков); каждая такая орбиталь характеризуется определенным набором атомных квантовых чисел. Метод МО исходит из предположения, что состояние электронов в молекуле также может быть описано как совокупность молекулярных электронных орбиталей (молекулярных электронных облаков), причем каждой молекулярной орбитали (МО) соответствует определенный набор молекулярных квантовых чисел. Как и в любой другой многоэлектронной системе, в молекуле сохраняет свою справедливость принцип Паули (см. § 32), так что на каждой МО может находиться не более двух электронов, которые должны обладать противоположно направленными спинами.
Молекулярное электронное облако может быть сосредоточено вблизи одного из атомных ядер, входящих в состав молекулы: такой электрон практически принадлежит одному атому и не принимает участия в образовании химических связей. В других случаях преобладающая часть электронного облака расположена в области пространства, близкой к двум атомным ядрам; это соответствует образованию двухцентровой химической связи. Однако в наиболее общем случае электронное облако принадлежит нескольким атомным ядрам и участвует в образовании многоцентровой химической связи. Таким образом, с точки зрения метода МО двухцентровая связь представляет собой лишь частный случай многоцентровой химической связи.
Основная проблема метода МО - нахождение волновых функций, описывающих состояние электронов на молекулярных орбиталях. В наиболее распространенном варианте этого метода, получившем сокращенное обозначение «метод МО ЛКАО» (молекулярные орбитали, линейная комбинация атомных орбиталей), эта задача решается следующим образом.
Пусть электронные орбитали взаимодействующих атомов характеризуются волновыми функциями и т. д. Тогда предполагается, что волновая функция , отвечающая молекулярной орбитали, может быть представлена в виде суммы
где некоторые численные коэффициенты.
Для уяснения физического смысла такого подхода вспомним, что волновая функция соответствует амплитуде волнового процесса, характеризующего состояние электрона (см. § 26). Как известно, при взаимодействии, например, звуковых или электромагнитных волн их амплитуды складываются. Как видно, приведенное уравнение равносильно предположению, что амплитуды молекулярной «электронной волны» (т. е. молекулярная волновая функция) тоже образуются сложением амплитуд взаимодействующих атомных «электронных волн» (т. е. сложением атомных волновых функций). При этом, однако, под влиянием силовых полей ядер и электронов соседних атомов волновая функция каждого атомного электрона изменяется по сравнению с исходной волновой функцией этого электрона в изолированном атоме. В методе МО ЛКАО эти изменения учитываются путем введения коэффициентов и т. д., так что при нахождении молекулярной волновой функции складываются не исходные, а измененные амплитуды - и т. д.
Выясним, какой вид будет иметь молекулярная волновая функция , образованная в результате взаимодействия волновых функций ( и ) -орбиталей двух одинаковых атомов. Для этого найдем сумму В данном случае оба рассматриваемых атома одинаковы, так что коэффициенты и равны по величине , и задача сводится к определению суммы . Поскольку постоянный коэффициент С не влияет на вид искомой молекулярной волновой функции, а только изменяет ее абсолютные значения, мы ограничимся нахождением суммы .
Для этого расположим ядра взаимодействующих атомов на том расстоянии друг от друга (r), на котором они находятся в молекуле, и изобразим волновые функции -орбиталей этих атомов (рис. 43,а); каждая из этих функций имеет вид, показанный на рис. 9, а(стр. 76). Чтобы найти молекулярную волновую функцию , сложим величины и : в результате получится кривая, изображенная на рис. 43,б. Как видно, в пространстве между ядрами значения молекулярной волновой функции больше, чем значения исходных атомных волновых функций. Но квадрат волновой функции характеризует вероятность нахождения электрона в соответствующей области пространства, т. е. плотность электронного облака (см. § 26). Значит, возрастание в сравнении с и означает, что при образовании МО плотность электронного облака в межъядерном пространстве увеличивается.

Рис. 43. Схема образования связывающей МО из атомных -орбиталей.
В результате возникают силы притяжения положительно заряженных атомных ядер к этой области--образуется химическая связь. Поэтому МО рассматриваемого типа называется связывающей.
В данном случае область повышенной электронной плотности находится вблизи оси связи, так что образовавшаяся МО относится к -типу. В соответствии с этим, связывающая МО, полученная в результате взаимодействия двух атомных -орбиталей, обозначается .
Электроны, находящиеся на связывающей МО, называются связывающими электронами.
Как указывалось на стр. 76, волновая функция -орбитали обладает постоянным знаком. Для отдельного атома выбор этого знака произволен: до сих пор мы считали его положительным. Но при взаимодействии двух атомов знаки волновых функций их -орбиталей могут оказаться различными. Значит, кроме случая, изображенного на рис. 43, а, где знаки обеих волновых функций одинаковы, возможен и случай, когда знаки волновых функций взаимодействующих -орбиталей различны. Такой случай представлен на рис. 44,а: здесь волновая функция -орбитали одного атома положительна, а другого - отрицательна. Пр и сложении этих волновых функций получится кривая, показанная на рис. 44, б. Молекулярная орбиталь, образующаяся при подобном взаимодействии, характеризуется уменьшением абсолютной величины волновой функции в межъядерном пространстве по сравнению с ее значением в исходных атомах: на оси связи появляется даже точка, в которой значение волновой функции, а, следовательно, и ее квадрата, обращается в нуль. Это означает, что в рассматриваемом случае уменьшится и плотность электронного облака в пространстве между атомами.

Рис. 44. Схема образования разрыхляющей МО из атомных -орбиталей.
В результате притяжение каждого атомного ядра в направлении к межъядерной области пространства окажется более слабым, чем в противоположном направлении, т. е. возникнут силы, приводящие к взаимному отталкиванию ядер. Здесь, следовательно, химическая связь не возникает; образовавшаяся в этом случае МО называется разрыхляющей , а находящиеся на ней электроны - разрыхляющими электронами.
Переход электронов с атомных -орбиталей на связывающую МО, приводящий к возникновению химической связи, сопровождается выделением энергии. Напротив, переход электронов с атомных -орбиталей на разрыхляющую МО требует затраты энергии. Следовательно, энергия электронов на орбитали ниже, а на орбитали выше, чем на атомных -орбиталях. Это соотношение энергий показано на рис. 45, на котором представлены как исходные -орбитали двух атомов водорода, так и молекулярные орбитали и сразу . Приближенно можно считать, что при переходе -электрона на связывающую МО выделяется столько же энергии, сколько необходимо затратить для его перевода на разрыхляющую МО.
Мы знаем, что в наиболее устойчивом (невозбужденном) состоянии атома электроны занимают атомные орбитали, характеризующиеся наименьшей возможной энергией. Точно так же наиболее устойчивое состояние молекулы достигается в том случае, когда электроны занимают МО, отвечающие минимальной энергии. Поэтому при образовании молекулы водорода оба электрона перейдут с атомных -орбиталей на связывающую молекулярную орбиталь (рис. 46); в соответствии с принципом Паули, электроны, находящиеся на одной МО, должны обладать противоположно направленными спинами.

Рис. 45. Энергетическая схема образования МО при взаимодействии -орбиталей двух одинаковых атомов.

Рис. 46. Энергетическая схема образования молекулы водорода.
Используя символы, выражающие размещение электронов на атомных и молекулярных орбиталях, образование молекулы водорода можно представить схемой:
В методе ВС кратность связи определяется числом общих электронных пар: простой считается связь, образованная одной общей электронной парой, двойной - связь, образованная двумя общими электронными парами, и т. д. Аналогично этому, в методе МО кратность связи принято определять по числу связывающих электронов, участвующих в ее образовании: два связывающих электрона соответствуют простой связи, четыре связывающих электрона - двойной связи и т. д. При этом разрыхляющие электроны компенсируют действие соответствующего числа связывающих электронов. Так, если в молекуле имеются 6 связывающих и 2 разрыхляющих электрона, то избыток числа связывающих электронов над числом разрыхляющих равен четырем, что соответствует образованию двойной связи. Следовательно, с позиции метода МО химическую связь в молекуле водорода,образованную двумя связывающими электронами, следует рассматривать как простую связь.
Теперь становится понятной возможность существования устойчивого молекулярного иона его образовании единственный электрон переходит с атомной орбитали на связывающую орбиталь , что сопровождается выделением энергии (рис. 47) и может быть выражено схемой:
В молекулярном ионе (рис. 48) имеется всего три электрона. На связывающей молекулярной орбитали могут разместиться, согласно принципу Паули, только два электрона, по этому третий электрон занимает разрыхляющую орбиталь .

Рис. 47. Энергетическая схема образования молекулярного иона водорода .

Рис. 48. Энергетическая схема образования молекулярного иона гелия .

Рис. 49. Энергетическая схема образования молекулы лития .

Рис. 50. Энергетическая схема образования МО при взаимодействии -орбиталей двух одинаковых атомов.
Таким образом, число связывающих электронов здесь на единицу больше числа разрыхляющих. Следовательно, ион должен быть энергетически устойчивым. Действительно, существование иона экспериментально подтверждено и установлено, что при его образовании выделяется энергия;
Напротив, гипотетическая молекула должна быть энергетически неустойчивой, поскольку здесь из четырех электронов, которые должны разместиться на МО, два займут связывающую, а два - разрыхляющую МО. Следовательно, образование молекулы не будет сопровождаться выделением энергии. Действительно, молекулы экспериментально не обнаружены.
В молекулах элементов второго периода МО образуются в результате взаимодействия атомных и -орбиталей; участие внутренних -электронов в образовании химической связи здесь пренебрежимо мало. Так, на рис. 49 приведена энергетическая схема образования молекулы : здесь имеются два связывающих электрона, что соответствует образованию простой связи. В молекуле же число связывающих и разрыхляющих электронов одинаково, так что эта молекула, подобно молекуле , энергетически неустойчива. Действительно, молекул обнаружить не удалось.
Схема образования МО при взаимодействии атомных -орби-талей показана на рис. 50. Как видно, из шести исходных -орбиталей образуются шесть МО: три связывающих и три разрыхляющих. При этом одна связывающая () и одна разрыхляющая орбитали принадлежат к -типу: они образованы взаимодействием атомных -орбиталей, ориентированных вдоль связи. Две связывающие и две разрыхляющие () орбитали образованы взаимодействием -орбиталей, ориентировванных перпендикулярно оси связи; эти орбитали принадлежат к -типу.
 Аквариум – маленькая искусственная экосистема
Аквариум – маленькая искусственная экосистема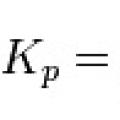 энергия связи – это энергия, необходимая для разрыва химической связи
энергия связи – это энергия, необходимая для разрыва химической связи Галлий где содержится. Применение галлия. Где встречается галлий в природе
Галлий где содержится. Применение галлия. Где встречается галлий в природе