Ett gen ett enzym moderne tolkning. Teorien om ett gen - ett enzym
4.2.1. Hypotesen "ett gen, ett enzym".
Første forskning. Etter at Garrod i 1902 påpekte at den genetiske defekten i alkaptonuri var assosiert med kroppens manglende evne til å bryte ned homogentisinsyre, var det viktig å belyse den spesifikke mekanismen som lå til grunn for denne lidelsen. Siden det allerede på den tiden var kjent at metabolske reaksjoner katalyseres av enzymer, kunne det antas at det var forstyrrelsen av et enzym som førte til alkaptonuri. En slik hypotese ble diskutert av Driesch (i 1896). Det ble også uttrykt av Haldane (1920, se) og Garrod (1923). Viktige stadier Utviklingen av biokjemisk genetikk begynte med arbeidet til Küchn og Butenandt om studiet av øyefarge i kvernmøll Ephestia kuhniella og lignende studier av Beadle og Ephrussi on Drosophila(1936). I disse banebrytende arbeidene ble insektmutanter som tidligere ble studert med genetiske metoder valgt for å belyse mekanismene for genvirkning. Denne tilnærmingen førte imidlertid ikke til suksess. Problemet viste seg å være for komplekst, og for å løse det var det nødvendig:
1) velg en enkel modellorganisme som er praktisk for eksperimentell studie;
2) se etter det genetiske grunnlaget for biokjemiske egenskaper, snarere enn det biokjemiske grunnlaget for genetisk bestemte egenskaper. Begge betingelsene ble oppfylt i arbeidet til Beadle og Tatum i 1941 (se også Beadle, 1945).
Beadle og Tatums modell. Artikkelen til disse forskerne begynte slik:
"Fra et fysiologisk genetikks synspunkt kan utviklingen og funksjonen til en organisme reduseres til et komplekst system av kjemiske reaksjoner som på en eller annen måte kontrolleres av gener. Det er ganske logisk å anta at disse genene... enten fungerer som enzymer selv eller bestemmer deres spesifisitet. Det er kjent at genetiker-fysiologer vanligvis prøver å undersøke det fysiologiske og biokjemiske grunnlaget for allerede kjente arvelige egenskaper. Denne tilnærmingen gjorde det mulig å etablere så mange bio kjemiske reaksjoner kontrollert av spesifikke gener. Slike studier har vist at enzymer og gener har spesifisitet av samme rekkefølge. Mulighetene til denne tilnærmingen er imidlertid begrenset. Den mest alvorlige begrensningen er at i dette tilfellet blir forskere oppmerksomme på arvelige egenskaper som ikke har en dødelig effekt og derfor er assosiert med reaksjoner som ikke er veldig viktige for organismens liv. Den andre vanskeligheten... er at den tradisjonelle tilnærmingen til problemet innebærer bruk av ytre manifesterte tegn. Mange av dem er morfologiske variasjoner basert på biokjemiske reaksjonssystemer så komplekse at deres analyse er uvanlig vanskelig.
Lignende betraktninger førte oss til følgende konklusjon. Studiet av det generelle problemet med genetisk kontroll av biokjemiske reaksjoner som bestemmer utvikling og metabolisme bør utføres ved hjelp av prosedyre motsatt av den generelt aksepterte: I stedet for å prøve å finne ut det kjemiske grunnlaget for kjente arvelige egenskaper, er det nødvendig å etablere om og hvordan gener kontrollerer kjente biokjemiske reaksjoner. Neurospora, som tilhører ascomycetene, har egenskaper som gjør det mulig å implementere en slik tilnærming og fungerer samtidig som et praktisk objekt for genetisk forskning. Det er derfor programmet vårt ble bygget på bruken av denne spesielle organismen. Vi antok at røntgeneksponering forårsaker mutasjoner i gener som kontrollerer visse kjemiske reaksjoner. Anta at for å overleve i et gitt miljø, må en organisme utføre en slags kjemisk reaksjon, så vil en mutant som mangler en slik evne være ulevedyktig under disse forholdene. Imidlertid kan den opprettholdes og studeres hvis den dyrkes i et medium hvor det vitale produktet av en genetisk blokkert reaksjon er tilsatt."
4 Virkning av gener 9
Ris. 4.1. Opplegg for et eksperiment for å oppdage biokjemiske mutanter av Neurospora I et komplett medium forstyrrer ikke mutasjoner indusert av røntgenstråler eller ultrafiolett stråling veksten av soppen. Imidlertid vokser ikke mutanten på minimalt medium. Når vitaminer tilsettes et minimalt medium, gjenopprettes evnen til å vokse. Når aminosyrer tilsettes, er det ingen vekst. Basert på disse dataene kan det antas at mutasjonen har skjedd i et gen som styrer vitaminmetabolismen. neste trinn er å identifisere et vitamin som kan gjenopprette normal funksjon En genetisk blokkering er funnet blant reaksjonene til vitaminbiosyntesen.Deretter beskriver Beadle og Tatum det eksperimentelle designet (fig. 4.1). Det komplette mediet inneholdt agar, uorganiske salter, maltekstrakt, gjærekstrakt og glukose. Minimalt medium inneholdt bare agar, salter, biotin og en karbonkilde. Mutantene som vokste i komplett medium og ikke vokste i minimalt medium ble studert i mest detalj. For å identifisere forbindelsen hvis syntese var svekket i hver av mutantene, ble individuelle komponenter av det komplette mediet tilsatt til minimal agar.
På denne måten ble det isolert stammer som ikke var i stand til å syntetisere visse vekstfaktorer: pyridoksin, tiamin og para-aminobenzosyre. Disse defektene har vist seg å være forårsaket av mutasjoner på spesifikke loki. Arbeidet la grunnlaget for en rekke studier på Neurospora, bakterier og gjær, der korrespondansen mellom "genetiske blokker" som er ansvarlige for individuelle metabolske stadier og spesifikke enzymforstyrrelser ble etablert. Denne tilnærmingen har raskt blitt et verktøy som lar forskere avdekke metabolske veier.
Hypotesen "ett gen - ett enzym" har fått sterk eksperimentell bekreftelse. Som arbeidet i de påfølgende tiårene viste, viste det seg å være overraskende fruktbart. Analyse av defekte enzymer og deres normale varianter gjorde det snart mulig å identifisere en klasse av genetiske lidelser som førte til endringer i funksjonen til enzymet, selv om proteinet i seg selv fortsatt var påvisbart og beholdt sine immunologiske egenskaper. I andre tilfeller endret temperaturoptimumen for enzymaktivitet. Noen varianter kan forklares med en mutasjon som påvirker en generell reguleringsmekanisme og som et resultat endrer aktiviteten til en hel gruppe enzymer. Lignende studier førte til etableringen av konseptet for regulering av genaktivitet i bakterier, som inkluderte konseptet om et operon.
10 4. Virkning av gener
De første eksemplene på enzymatiske lidelser hos mennesker. Den første arvelige menneskelige sykdommen som en enzymatisk lidelse kunne påvises for, var methemoglobinemi med en recessiv arvemåte (Gibson og Harrison, 1947; Gibson, 1948) (25080). I dette tilfellet er det skadede enzymet NADH - avhengig methemoglobinreduktase. Det første forsøket på systematisk å studere en gruppe menneskelige sykdommer assosiert med metabolske defekter ble gjort i 1951. I en studie av glykogenlagringssykdom viste Coreys at i åtte av ti tilfeller av den patologiske tilstanden som ble diagnostisert som Gierkes sykdom (23220), var leverglykogenstrukturen normal, og i to tilfeller var den tydelig unormal. Det var også åpenbart at leverglykogen, akkumulert i overkant, ikke kunne omdannes direkte til sukker, siden pasienter hadde en tendens til hypoglykemi. Mange enzymer er nødvendig for å bryte ned glykogen for å danne glukose i leveren. To av dem, amylo-1,6-glukosidase og glukose 6-fosfatase, ble valgt for studier som mulige defekte elementer i enzymsystemet. Frigjøringen av fosfat fra glukose-6-fosfat ble målt i leverhomogenater ved forskjellige pH-verdier. Resultatene er presentert i fig. 4.2. I normal lever ble det funnet høy aktivitet med et optimum ved pH 6-7. Alvorlig leverdysfunksjon ved cirrhose korrelerte med en svak reduksjon i aktivitet. På den annen side, ved Gierkes sykdom med dødelig utfall, kunne enzymaktivitet ikke påvises i det hele tatt; det samme resultatet ble oppnådd ved undersøkelse av en annen lignende pasient. To pasienter med mindre alvorlige symptomer hadde en signifikant reduksjon i aktivitet.
Det ble konkludert med at i disse tilfellene av dødelig Gierkes sykdom var det en defekt i glukose-6-fosfatase. Men i de fleste mildere tilfeller var aktiviteten til dette enzymet ikke lavere enn ved levercirrhose, og hos kun to pasienter var den litt lavere (fig. 4.2).
Ifølge Coreys kan den unormale akkumuleringen av glykogen i muskelvev ikke assosieres med mangel på glukose-6-fosfatase, siden dette enzymet er fraværende i musklene og er normalt. De foreslo svekket amylo-1,6-glukosidaseaktivitet som en mulig forklaring på muskelglykogenose. Denne spådommen ble snart bekreftet: Forbes oppdaget en slik defekt i et av de klinisk signifikante tilfellene av glykogenlagringssykdom som involverte hjerte- og skjelettmuskulaturen. Nå vi
4. Virkning av gener 11
Et stort antall enzymdefekter er kjent ved glykogenlagringssykdom.
Selv om de ulike formene for denne sykdommen avviker noe i graden av manifestasjon, har de klinisk mye til felles. Med ett unntak, er de alle arvet på en autosomal recessiv måte. Hvis enzymdefekter ikke hadde blitt oppdaget, ville patologien til glykogenlagring bli betraktet som én sykdom med karakteristiske intrafamiliære korrelasjoner i alvorlighetsgrad, symptomatiske detaljer og tidspunkt for død. Vi har altså foran oss et eksempel hvor genetisk heterogenitet, som kun kunne antas basert på studiet av fenotypen (avsnitt 3.3.5), ble bekreftet ved analyse på biokjemisk nivå: forskning enzymatisk aktivitet tillot identifisering av spesifikke gener.
I de påfølgende årene økte forskningstakten innen enzymdefekter, og for de 588 identifiserte recessive autosomale genene som McKusick beskriver i den sjette utgaven av boken Mendelian Inheritance in Man (1983), ble det funnet spesifikke enzymdefekter i mer enn 170 saker. Vår fremgang på dette feltet er direkte relatert til utviklingen av konsepter og metoder for molekylær genetikk.
Noen stadier av å studere enzymatiske lidelser hos mennesker. Vi presenterer bare de viktigste milepælene i denne pågående prosessen: 1934 Fölling oppdaget fenylketonuri
1941 Beadle og Tatum formulerte "ett gen, ett enzym"-hypotesen 1948 Gibson beskrev det første tilfellet av en enzymatisk lidelse i en menneskelig sykdom (recessiv methemoglobinemi)
1952 The Coreys oppdaget glukose-6-fosfatase-mangel i Gierkes sykdom
1953 Jervis demonstrerte fraværet av fenylalaninhydroksylase i fenylketonuri. Bickel rapporterte det første forsøket på å dempe en enzymatisk lidelse ved å bruke en diett med lavt fenylalanin
1955 Smithies utviklet stivelsegelelektroforeseteknikk
1956 Carson et al oppdaget en defekt i glukose-6-fosfatdehydrogenase (G6PD) i et tilfelle av indusert hemolytisk anemi
1957 Kalkar et al. beskrev enzymatisk mangel ved galaktosemi, og viste at mennesker og bakterier har identiske defekter i enzymatisk aktivitet
1961 Krut og Weinberg demonstrerte en enzymdefekt i galaktosemi in vitro i dyrkede fibroblaster
1967 Seegmiller et al oppdaget en hypoxanthin-guanine phosphoribosyltransferase (HPRT) defekt i Lesch-Nyhan syndrom
1968 Cleaver beskrev en forstyrrelse av eksisjonsreparasjon i xeroderma pigmentosum
1970 Neufeld identifiserte enzymatiske defekter i mukopolysakkaridoser, noe som gjorde det mulig å identifisere veier for nedbrytning av mukopolysakkarider
1974 Brown og Goldstein beviste at genetisk betinget overproduksjon av hydroksymetylglutarylCoA-reduktase ved familiær hyperkolesterolemi skyldes en defekt i den membranlokaliserte lipoproteinreseptoren med lav tetthet, som modulerer aktiviteten til dette enzymet (HMG)
1977 Sly et al demonstrerte at mannose-6-fosfat (som en komponent av lysosomale enzymer) gjenkjennes av fibroblastreseptorer. En genetisk prosesseringsfeil forhindrer bindingen av lysosomale enzymer, som et resultat av at deres frigjøring til cytoplasmaet og påfølgende sekresjon i plasma blir svekket (I-cellesykdom)
12 4. Virkning av gener
1980 Ved pseudohypoparathyroidisme oppdages en defekt i proteinet som sikrer koblingen av reseptoren og cyclase.
Mange kjemiske reaksjoner forekommer i hver levende celle. Enzymer er proteiner med spesielle og ekstremt viktige funksjoner. De kalles biokatalysatorer. Det viktigste i kroppen er å akselerere biokjemiske reaksjoner. De første reagensene, hvis interaksjon katalyseres av disse molekylene, kalles substrater, og de endelige forbindelsene kalles produkter.
I naturen fungerer enzymproteiner bare i levende systemer. Men i moderne bioteknologi, klinisk diagnostikk, legemidler og medisin, rensede enzymer eller deres komplekser brukes, samt tilleggskomponenter som er nødvendige for driften av systemet og datavisualisering for forskeren.
Biologisk betydning og egenskaper til enzymer
Uten disse molekylene ville ikke en levende organisme kunne fungere. Alle vitale prosesser fungerer problemfritt takket være enzymer. Hovedfunksjonen til enzymproteiner i kroppen er å regulere stoffskiftet. Uten dem er normal metabolisme umulig. Regulering av aktiviteten til molekyler skjer under påvirkning av aktivatorer (induktorer) eller inhibitorer. Kontrollen opererer på ulike nivåer protein syntese. Det "fungerer" også på et ferdiglaget molekyl.
Hovedegenskapene til enzymproteiner er spesifisitet til et spesifikt substrat. Og følgelig evnen til å katalysere bare en eller, sjeldnere, en rekke reaksjoner. Vanligvis er slike prosesser reversible. Ett enzym er ansvarlig for begge funksjonene. Men det er ikke alt.

Rollen til enzymproteiner er avgjørende. Uten dem oppstår ikke biokjemiske reaksjoner. På grunn av virkningen av enzymer blir det mulig for reagenser å overvinne aktiveringsbarrieren uten betydelig energiforbruk. Det er ikke mulig for kroppen å varme opp temperaturen over 100 °C eller bruke aggressive komponenter som f.eks kjemisk laboratorium. Enzymproteinet binder seg til underlaget. I bundet tilstand skjer modifikasjon med den påfølgende utgivelsen av sistnevnte. Dette er nøyaktig hvordan alle katalysatorer som brukes i kjemisk syntese fungerer.
Hva er organiseringsnivåene til et protein-enzymmolekyl?
Vanligvis har disse molekylene en tertiær (kule) eller kvartær (flere sammenkoblede kuler) protein struktur. De syntetiseres først i lineær form. Og så kollapser de inn i den nødvendige strukturen. For å sikre aktivitet trenger en biokatalysator en viss struktur.

Enzymer, som andre proteiner, blir ødelagt av varme, ekstreme pH-verdier og aggressive kjemiske forbindelser.
Ytterligere egenskaper ved enzymer
Blant dem er følgende funksjoner til komponentene:
- Stereospesifisitet - dannelsen av bare ett produkt.
- Regioselektivitet - gap kjemisk forbindelse eller modifikasjon av gruppen i bare én posisjon.
- Kjemoselektivitet - katalyse av bare én reaksjon.
Funksjoner ved arbeid
Nivået varierer. Men ethvert enzym er alltid aktivt mot et spesifikt substrat eller gruppe av forbindelser som er like i struktur. Ikke-proteinkatalysatorer har ikke denne egenskapen. Spesifisitet måles ved bindingskonstanten (mol/L), som kan nå 10−10 mol/L. Arbeidet til det aktive enzymet er raskt. Ett molekyl katalyserer tusenvis til millioner av operasjoner per sekund. Graden av akselerasjon av biokjemiske reaksjoner er betydelig (1000-100000 ganger) høyere enn for konvensjonelle katalysatorer.
Virkningen av enzymer er basert på flere mekanismer. Den enkleste interaksjonen skjer med ett substratmolekyl etterfulgt av dannelsen av et produkt. De fleste enzymer er i stand til å binde 2-3 forskjellige molekyler som inngår i en reaksjon. For eksempel overføring av en gruppe eller et atom fra en forbindelse til en annen eller dobbel substitusjon ved å bruke "ping-pong"-prinsippet. I disse reaksjonene kombineres vanligvis ett substrat, og det andre er knyttet til enzymet gjennom en funksjonell gruppe.
Studien foregår ved hjelp av metoder:
- Definisjoner av mellom- og sluttprodukter.
- Studerer geometrien til strukturen og funksjonelle grupper knyttet til underlaget og gir høy
- Mutasjoner av enzymgener og bestemmelse av endringer i dets syntese og aktivitet.

Aktivt og bindingssted
Substratmolekylet er mye mindre i størrelse enn enzymproteinet. Derfor oppstår binding på grunn av et lite antall funksjonelle grupper i biokatalysatoren. De danner et aktivt senter som består av et spesifikt sett med aminosyrer. Strukturen inneholder en protesegruppe av ikke-protein natur, som også kan være en del av det aktive senteret.
En egen gruppe enzymer bør skilles ut. Molekylet deres inneholder et koenzym som hele tiden binder seg til molekylet og frigjøres fra det. Et ferdigdannet enzymprotein kalles et holoenzym, og når kofaktoren fjernes, kalles det et apoenzym. Vitaminer, metaller, derivater av nitrogenholdige baser (NAD - nikotinamidadenindinukleotid, FAD - flavinadenindinukleotid, FMN - flavinmononukleotid) fungerer ofte som koenzymer.

Bindingsstedet gir substrataffinitetsspesifisitet. På grunn av det dannes et stabilt substrat-enzymkompleks. Strukturen til kulen er konstruert på en slik måte at den har en nisje (spalte eller fordypning) av en viss størrelse på overflaten, noe som sikrer binding av underlaget. Denne sonen er vanligvis plassert i nærheten av det aktive senteret. Individuelle enzymer har steder for binding til kofaktorer eller metallioner.
Konklusjon
Enzymprotein spiller en viktig rolle i kroppen. Slike stoffer katalyserer kjemiske reaksjoner og er ansvarlige for den metabolske prosessen - metabolisme. I enhver levende celle skjer det stadig hundrevis av biokjemiske prosesser, inkludert reduksjonsreaksjoner, spaltning og syntese av forbindelser. Stoffer oksideres konstant med en stor frigjøring av energi. Det brukes på sin side på dannelsen av karbohydrater, proteiner, fett og deres komplekser. Nedbrytningsprodukter er strukturelle elementer for syntese av nødvendige organiske forbindelser.
» , » Ett gen, ett enzym
Ett gen, ett enzym
92
Publiseringsdato: 24. juli 2018
Hypotesen om ett gen, ett enzym er ideen, fremsatt tidlig på 1940-tallet, at hvert gen kontrollerer syntesen eller aktiviteten til ett enzym. Konseptet, som kombinerer feltene genetikk og biokjemi, ble foreslått av den amerikanske genetikeren George Wells Beadle og den amerikanske biokjemikeren Edward L. Tatum, som forsket på Neurospora crassa. Eksperimentene deres innebar først å avbilde formen til mutasjonsinduserende røntgenstråler og deretter dyrke den i minimalt vekstmedium som bare inneholdt de essensielle næringsstoffene som trengs for at villtypestammen skal overleve. De oppdaget at de mutante muggstammene krevde tilsetning av visse aminosyrer for å vokse. Ved å bruke denne informasjonen var forskerne i stand til å koble mutasjoner i visse gener til forstyrrelse av spesifikke enzymer i metabolske veier som vanligvis produserte de manglende aminosyrene. Det er nå kjent at ikke alle gener koder for et enzym og at noen enzymer består av flere korte polypeptider kodet av to eller flere gener.
Funn av ekson-intron-organiseringen av eukaryote gener og muligheten for alternativ spleising viste at den samme nukleotidsekvensen til det primære transkriptet kan sikre syntesen av flere polypeptidkjeder med ulike funksjoner eller deres modifiserte analoger. For eksempel inneholder gjærmitokondrier et boksgen (eller cob) som koder for respirasjonsenzymet cytokrom b. Det kan eksistere i to former: Det "lange" genet, bestående av 6400 bp, har 6 eksoner med en total lengde på 1155 bp. og 5 introner. Den korte formen av genet består av 3300 bp. og har 2 introner. Det er faktisk et "langt" gen som mangler de tre første intronene. Begge former for genet er like godt uttrykt.
Etter å ha fjernet det første intronet til det "lange" boksgenet, basert på den kombinerte nukleotidsekvensen til de to første eksonene og en del av nukleotidene til det andre intronet, dannes en matrise for et uavhengig protein - RNA-maturase (fig. 3,43). Funksjonen til RNA-maturase er å sikre det neste trinnet med spleising - fjerning av det andre intronet fra det primære transkriptet og til slutt dannelsen av en mal for cytokrom b.
Et annet eksempel er en endring i spleisemønsteret til det primære transkriptet som koder for strukturen til antistoffmolekyler i lymfocytter. Membranformen av antistoffer har en lang "hale" av aminosyrer ved C-terminalen, som sikrer fiksering av proteinet på membranen. Den utskilte formen av antistoffer har ikke en slik hale, noe som forklares ved fjerning av nukleotidene som koder for denne regionen fra det primære transkriptet under spleising.
I virus og bakterier er det beskrevet en situasjon hvor ett gen samtidig kan være en del av et annet gen, eller en viss DNA-nukleotidsekvens kan være en del av to forskjellige overlappende gener. For eksempel viser det fysiske kartet av genomet til fag FX174 (fig. 3.44) at sekvensen til gen B er lokalisert inne i gen A, og gen E er en del av sekvensen til gen D. Dette trekk ved organiseringen av fagen genomet var i stand til å forklare den eksisterende avviket mellom dens relativt lille størrelse (den består av 5386 nukleotider) og antall aminosyrerester i alle syntetiserte proteiner, som overstiger det som er teoretisk tillatt for en gitt genomkapasitet. Muligheten for å sette sammen forskjellige peptidkjeder på mRNA syntetisert fra overlappende gener (A og B eller E og D) er sikret ved tilstedeværelsen av ribosombindingsseter i dette mRNA. Dette gjør at translasjon av et annet peptid kan begynne fra et nytt utgangspunkt.
Nukleotidsekvensen til gen B er samtidig en del av gen A, og gen E er en del av gen D
Overlappende gener, oversatt både med en rammeforskyvning og i samme leseramme, ble også funnet i λ-faggenomet. Det antas også at det er mulig å transkribere to forskjellige mRNA fra begge komplementære tråder i en DNA-seksjon. Dette krever tilstedeværelse av promoterregioner som bestemmer bevegelsen av RNA-polymerase i forskjellige retninger langs DNA-molekylet.
De beskrevne situasjonene, som indikerer tillateligheten av å lese forskjellig informasjon fra samme DNA-sekvens, antyder at overlappende gener er et ganske vanlig element i organiseringen av genomet til virus og muligens prokaryoter. I eukaryoter tillater gendiskontinuitet også syntese av en rekke peptider fra samme DNA-sekvens.
Med alt dette i tankene er det nødvendig å endre definisjonen av genet. Det er klart at vi ikke lenger kan snakke om et gen som en kontinuerlig sekvens av DNA som unikt koder for et spesifikt protein. Tilsynelatende, for tiden, bør formelen "Ett gen - ett polypeptid" fortsatt anses som den mest akseptable, selv om noen forfattere foreslår å endre den: "Ett polypeptid - ett gen". I alle fall må begrepet gen forstås som en funksjonell enhet av arvelig materiale, som i sin kjemiske natur er et polynukleotid og bestemmer muligheten for å syntetisere en polypeptidkjede, tRNA eller rRNA.
Ett gen, ett enzym.
I 1940 brukte J. Beadle og Edward Tatum en ny tilnærming til å studere hvordan gener gir metabolisme i et mer praktisk forskningsemne - den mikroskopiske soppen Neurospora crassa. De oppnådde mutasjoner der; det var ingen aktivitet av ett eller annet metabolsk enzym. Og dette førte til at den mutante soppen ikke var i stand til å syntetisere en bestemt metabolitt på egen hånd (for eksempel aminosyren leucin) og bare kunne leve når leucin ble tilsatt næringsmediet. Teorien om "ett gen, ett enzym" formulert av J. Beadle og E. Tatum fikk raskt bred anerkjennelse blant genetikere, og de ble selv tildelt Nobelprisen.
Metoder. utvalg av såkalte "biokjemiske mutasjoner" som fører til forstyrrelser i virkningen av enzymer som gir forskjellige metabolske veier, viste seg å være svært fruktbart, ikke bare for vitenskapen, men også for praksis. Først førte de til fremveksten av genetikk og seleksjon av industrielle mikroorganismer, og deretter til den mikrobiologiske industrien, som bruker stammer av mikroorganismer som overproduserer så strategisk viktige stoffer som antibiotika, vitaminer, aminosyrer osv. Prinsippene for seleksjon og genteknologi av superprodusentstammer er basert på ideen om at "ett gen koder for ett enzym." Og selv om denne ideen er utmerket for praksis, gir overskudd på flere millioner dollar og redder millioner av liv (antibiotika) - er den ikke endelig. Ett gen er ikke bare ett enzym.
| " |
Genetikk- Vitenskap er på ingen måte ung; forskning på den har blitt utført i flere århundrer, og startet med Mendel i 1865 til i dag. Begrepet "gen" for en enhet med arvelig karakteristikk ble først foreslått av Johannsen i 1911, og ble foredlet på 1940-tallet av konseptet "ett gen, ett enzym" foreslått av Tatum og Beadle.
Denne posisjonen ble bestemt i forsøk på Drosophila-fluer, men gjelder like mye for mennesker; Til syvende og sist er livet til alle vesener bestemt av deres DNA. Det menneskelige DNA-molekylet er større enn alle andre organismer, og strukturen er mer kompleks, men essensen av funksjonene er den samme i alle levende vesener.
Konsept" ett gen - ett enzym", som oppsto på grunnlag av ideene til Tatum og Beadle, kan formuleres som følger:
1. Alt biologiske prosesser er under genetisk kontroll.
2. Alle biokjemiske prosesser skjer i form av trinnvise reaksjoner.
3. Hver biokjemisk reaksjon er til syvende og sist under kontroll av ulike individuelle gener.
4. En mutasjon i et bestemt gen fører til en endring i cellens evne til å utføre en viss kjemisk reaksjon.
Siden den gang har konseptet "ett gen - ett enzym" utvidet seg noe, og høres nå ut som " ett gen - ett protein" I tillegg tyder nyere forskning på at noen gener virker sammen med andre for å produsere unike proteiner, det vil si at noen gener kan kode for mer enn ett protein.
Menneskets genom inneholder ca. 3 milliarder nukleotidpar; det antas å inneholde fra 50 000 til 100 000. Etter å ha dechiffrert genomet, viste det seg at det bare er rundt 30 000 gener.Samspillet mellom disse genene er mye mer komplekst enn forventet. Gener er kodet i DNA-tråder, som kombineres med visse kjerneproteiner for å danne kromosomer.
Gener- ikke bare DNA-segmenter: de er dannet av kodende sekvenser - eksoner, ispedd ikke-kodende sekvenser - nitroner. Eksoner, som den uttrykte delen av DNA, utgjør bare en liten del av organismens viktigste molekyl; det meste kommer ikke til uttrykk, er dannet av nitroner og kalles ofte "stille" DNA.
Omtrentlig størrelse og struktur menneskelig genom er presentert i figuren nedenfor. Den funksjonelle lengden til det menneskelige kromosomet uttrykkes i centimorganider. Centimorganide (cM) er avstanden som sannsynligheten for å krysse over under meiose er 1 %. Genkoblingsanalyse har vist at lengden på det menneskelige genomet er omtrent 3000 cM.
Gjennomsnitt kromosom inneholder omtrent 1500 gener kodet i 130 millioner nukleotidbasepar. Figuren nedenfor viser skjematisk de fysiske og funksjonelle størrelsene til genomet: den første beregnes i nukleotidpar, og den andre i cM. Det meste av det menneskelige genomet er representert av "stille" DNA og kommer ikke til uttrykk.
På DNA-matrise Som et resultat av transkripsjonsprosessen syntetiseres RNA, og deretter protein. Følgelig bestemmer DNA-sekvensen fullstendig sekvensen av funksjonelle proteiner i cellen. Alle proteiner syntetiseres som følger:
DNA => RNA => protein

Det genetiske apparatet til mennesker og andre pattedyr er mer komplekst enn det til andre levende organismer, siden deler av noen gener hos pattedyr kan kombineres med deler av andre gener, noe som resulterer i syntese av et helt nytt protein eller kontroll av en separat cellulær funksjon.
Følgelig er det hos mennesker mulig å øke antall uttrykte gener uten å faktisk øke volumet av uttrykte gener. DNA eller det absolutte antallet gener.
Totalt sett er omtrent 70 % av alt genetisk materiale ikke uttrykt.
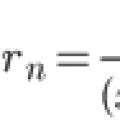 Taylor-serieutvidelse Omtrentlig løsning av Cauchy-problemet for den vanlige
Taylor-serieutvidelse Omtrentlig løsning av Cauchy-problemet for den vanlige Hva læres IKKE på skolen Hva læres ikke på skolen spør
Hva læres IKKE på skolen Hva læres ikke på skolen spør Money Thinking Formel (A
Money Thinking Formel (A