Гидрид устөрөгчийн хадгалах систем. Шилжилтийн элементийн гидридүүд Ердийн металл хоорондын гидридүүд
Хавтан тектоникийн онол нь "ялалтаа" тэмдэглэж, газрын хэвлийн бүтцийг цаашид судлах явцад сул талуудыг олж авч, нуралт руу шилжиж байсан бол дэлхийн тэлэлтийн онол хоёр үндсэн асуудлыг шийдэж, Үүний зэрэгцээ - ийм өргөтгөлийн механизмын хувилбар олдсон бөгөөд энэ нь цөм дэх "хэт их" даралтаар бүх асуултыг нэгэн зэрэг арилгадаг.
Удаан хугацааны мухардлаас гарах арга замыг гучин жилийн өмнө Зөвлөлтийн эрдэмтэн Владимир Ларин (одоо геологийн шинжлэх ухааны доктор) санал болгосон бөгөөд тэрээр энэ асуудалд огт өөр өнцгөөс ханддаг байв.
Цагаан будаа. 69. Металл ба устөрөгчийн атомын диаграмм
Юуны өмнө, устөрөгчийг метал дахь уусгах нь түүнийг зүгээр л металлын атомуудтай холих явдал биш юм - энэ тохиолдолд устөрөгч нь зөвхөн нэг л байдаг электроноо уусмалын нийтлэг санд өгч, туйлын "нүцгэн" хэвээр байна. ” протон. Протоны хэмжээсүүд нь ямар ч атомын хэмжээнээс 100 мянга дахин (!) бага байдаг бөгөөд энэ нь эцсийн дүндээ (протоны цэнэг ба массын асар их концентрацитай хамт) бусад атомуудын электрон бүрхүүлд гүн нэвтрэх боломжийг олгодог. (нүцгэн протоны энэ чадвар нь туршилтаар аль хэдийн батлагдсан).
Гэхдээ протон нь өөр атом руу нэвтэрч, энэ атомын цөмийн цэнэгийг нэмэгдүүлж, электронуудын таталцлыг нэмэгдүүлж, улмаар атомын хэмжээг багасгадаг. Тиймээс метал дахь устөрөгчийг уусгах нь хичнээн парадоксик мэт санагдаж байсан ч ийм уусмалыг сулруулахад хүргэдэггүй, харин эсрэгээрээ анхны металлыг нягтруулах. Хэвийн нөхцөлд (өөрөөр хэлбэл, хэвийн атмосферийн даралт ба өрөөний температурт) энэ нөлөө нь ач холбогдолгүй боловч өндөр даралт, температурт энэ нь мэдэгдэхүйц юм.
Тиймээс дэлхийн гаднах шингэн цөмд их хэмжээний устөрөгч агуулагддаг гэсэн таамаглал нь нэгдүгээрт, үүнтэй зөрчилддөггүй. химийн шинж чанар; хоёрдугаарт, хүдрийн ордуудад устөрөгчийн гүн агуулахын асуудлыг аль хэдийн шийдсэн; Гуравдугаарт, бидний хувьд юу илүү чухал вэ? Энэ нь түүний доторх даралтыг мэдэгдэхүйц нэмэгдүүлэхгүйгээр бодисыг их хэмжээгээр нягтруулах боломжийг олгодог.
“Москвагийн их сургуульд тэд металл хоорондын нэгдэл [лантан, никелийн хайлш] дээр суурилсан цилиндр бүтээжээ. Цорго эргүүл, нэг литрийн цилиндрээс мянган литр устөрөгч ялгарна!” (М. Курячаяа, “Байгаагүй байсан гидридүүд”).
Гэтэл энэ бүхэн “үр” болох нь тодорхой боллоо...
Металлын гидридийн хувьд, өөрөөр хэлбэл устөрөгчтэй металлын химийн нэгдлүүдийн хувьд бид өөр дүр зурагтай байдаг: устөрөгч нь электроноо өгдөггүй (ерөнхийдөө сул электрон гахайн банкинд), харин метал нь гаднаасаа салдаг. электрон бүрхүүл, устөрөгчтэй ионы холбоо гэж нэрлэгддэг. Үүний зэрэгцээ, устөрөгчийн атом нь аль хэдийн эргэлдэж буй электрон тойрог замд нэмэлт электрон хүлээн авснаар хэмжээ нь бараг өөрчлөгддөггүй. Гэхдээ металлын атомын ионы радиус, өөрөөр хэлбэл гаднах электрон бүрхүүлгүй атом нь атомын радиусаас хамаагүй бага юм. Төмөр, никелийн хувьд ионы радиус нь төвийг сахисан атомын радиусын ойролцоогоор 0.6-тай тэнцүү байдаг ба бусад зарим металлын хувьд энэ харьцаа илүү гайхалтай байдаг. Металлын ионуудын хэмжээ ийнхүү багассан нь ийм нягтралын үр дүнд даралт ихсэхгүйгээр тэдгээрийг гидрид хэлбэрээр хэд хэдэн удаа нягтруулах боломжийг олгодог!
Нэмж дурдахад гидридийн тоосонцорыг хэт нягтруулах чадварыг ердийн хэвийн нөхцөлд ч туршилтаар илрүүлдэг (Хүснэгт 1-ийг үзнэ үү), өндөр даралттай үед энэ нь улам бүр нэмэгддэг.
Нягт, г/см
Металл
Гидрид
Нягтралт, %
Хүснэгт 1. Зарим гидридийн нягтрал (хэвийн нөхцөлд)
Нэмж дурдахад гидридүүд өөрсдөө нэмэлт устөрөгчийг уусгах чадвартай байдаг. Нэгэн цагт тэд түлш хадгалах зориулалттай устөрөгчийн автомашины хөдөлгүүрийг хөгжүүлэхэд энэ чадварыг ашиглахыг оролдсон.
“...жишээ нь, нэг шоо см магнийн гидрид шингэн устөрөгчийн нэг шоо см-т агуулагдах жингээс нэг хагас дахин, зуун тавин атмосфер хүртэл шахагдсан хийнээс долоо дахин их устөрөгч агуулдаг! ” (М. Курячаяа, “Байгаагүй байсан гидридүүд”).
Нэг асуудал бол гидрид нь хэвийн нөхцөлд маш тогтворгүй байдаг...
Гэхдээ бидэнд хэвийн нөхцөл шаардлагагүй, учир нь бид тэдний даралт нь мэдэгдэхүйц өндөр байдаг гаригийн гэдэсний гүнд оршин тогтнох боломжийн талаар ярьж байна. Даралт ихсэх тусам гидридийн тогтвортой байдал мэдэгдэхүйц нэмэгддэг.
Өнөө үед эдгээр шинж чанаруудын туршилтын баталгааг олж авсан бөгөөд улам олон геологичид гидридийн цөмийн загвар нь өмнөх төмөр-никелийн загвараас илүү бодит байдалд илүү ойр байж магадгүй гэж аажмаар итгэх хандлагатай байна. Түүгээр ч зогсохгүй манай гаригийн гэдэс доторх нөхцөл байдлын нарийн тооцоолол нь түүний цөм дэх "цэвэр" төмөр-никелийн загвар хангалтгүй байгааг харуулж байна.
Газар хөдлөлтийн хэмжилтээс үзэхэд дэлхийн дотоод (хатуу) ба гадна (шингэн) цөм нь ижил физик-химийн параметрийн дагуу зөвхөн металл төмрөөс бүрдсэн цөмийн загварт үндэслэн олж авсан утгатай харьцуулахад бага нягтралтай болохыг харуулж байна. .
Цөмд устөрөгч байгаа эсэх нь атмосферийн даралтад төмрийг бага уусгадаг тул удаан хугацааны турш маргаантай байсаар ирсэн. Гэсэн хэдий ч сүүлийн үеийн туршилтууд нь төмрийн гидрид FeH нь өндөр температур, даралтанд үүсч, гүн рүү ороход 62 ГПа-аас дээш даралтанд тогтвортой байдаг нь ~1600 км-ийн гүнд тохирч байгааг тогтоожээ. Үүнтэй холбогдуулан цөмд их хэмжээний (40 моль.%) устөрөгч байгаа нь хүлээн зөвшөөрөгдөхүйц бөгөөд түүний нягтыг сейсмологийн өгөгдөлд нийцсэн утга болгон бууруулдаг"(Ю. Пущаровский, "Дэлхийн мантийн тектоник ба геодинамик").
Гэхдээ хамгийн чухал зүйл бол тодорхой нөхцөлд, жишээлбэл, даралт буурах эсвэл халах үед гидрид нь бүрэлдэхүүн хэсгүүдэд хуваагдах чадвартай байдаг. Металлын ионууд нь бүх үр дагавартай атомын төлөвт хувирдаг. Бодисын эзэлхүүн нь массыг өөрчлөхгүйгээр, өөрөөр хэлбэл материйн хадгалалтын хуулийг зөрчихгүйгээр мэдэгдэхүйц нэмэгдэх процесс явагддаг. Метал дахь уусмалаас устөрөгч ялгарах үед ижил төстэй үйл явц тохиолддог (дээрхийг үзнэ үү).
Энэ нь гаригийн хэмжээг нэмэгдүүлэх бүрэн ойлгомжтой механизмыг аль хэдийн хангасан байна !!!
"Дэлхий анх гидрид болсон гэсэн таамаглалын гол геологи, тектоник үр дагавар нь геологийн түүхийн туршид мэдэгдэхүйц, магадгүй олон талт үр дагавар юм. түүний эзлэхүүнийг нэмэгдүүлэх, энэ нь устөрөгчийн хийгүйжүүлэлт, гидрид нь метал руу шилжих явцад гаригийн дотоод хэсэг зайлшгүй задарч байгаатай холбоотой юм.
Тиймээс Ларин хүдрийн ордуудын зарим асуудлыг шийдэж, дэлхийн түүхэн дэх хэд хэдэн үйл явцыг тайлбарлаад зогсохгүй (бид буцаж ирэх болно) онолыг санал болгов. гариг - гаж нөлөө.
Ларин хамгийн чухал зүйлийг хийсэн - тэр дэлхийн тэлэлтийн онолын бүх гол асуудлуудыг арилгасан!..
Үлдсэн зүйл бол "техникийн дэлгэрэнгүй мэдээлэл" юм.
Жишээлбэл, манай гараг оршин тогтнох бүх хугацаанд яг ямар хэмжээгээр өссөн, түүний тэлэлт яг ямар хурдтай явагдсан нь тодорхойгүй байна. Өөр өөр судлаачид бие биенээсээ эрс ялгаатай тооцоог гаргаж байсан бөгөөд үүнээс гадна хуруугаа хөхөхийг маш их санагдуулдаг.
"... Палеозойн үед энэ таамаглалын дагуу дэлхийн радиус орчин үеийнхээс ойролцоогоор 1.5-1.7 дахин бага байсан тул түүнээс хойш дэлхийн хэмжээ ойролцоогоор 3.5-5 дахин нэмэгдсэн байна" (О. Сорохтин, "Тэлж буй дэлхийн сүйрэл").
"Дэлхийн харьцангуй дунд зэргийн тэлэлтийн талаархи хамгийн их магадлалтай санаа бол Археаны эхэн үеэс (өөрөөр хэлбэл 3.5 тэрбум жилийн турш) түүний радиус нэгээс хагасаас хоёр дахин нэмэгдэх боломжтой байсан. , протерозойн сүүл үеэс (өөрөөр хэлбэл 1.6 тэрбум гаруй жил) - 1.3 - 1.5 дахин ихгүй, мезозойн эхэн үеэс (өөрөөр хэлбэл сүүлийн 0.25 тэрбум жилийн хугацаанд) 5-аас ихгүй байна. 10 хувь" (Е. Милановский, "Дэлхий тэлж байна уу? Дэлхий лугшиж байна уу?").
Харамсалтай нь. Ларины таамаглал ч энэ асуултад шууд хариулдаггүй.
Түүгээр ч зогсохгүй бүх судлаачид энэ үйл явц нь дэлхий үүссэн эхэн үеэс их бага хэмжээгээр жигд явагддаг (гидридын онолыг зохиогч В.Ларин ч энэ таамаглалыг баримталдаг) гэсэн үндсэн дээр үндэслэсэн. Энэ нь тэлэлтийн хурд багатай тул орчин үеийн багаж хэрэгслээр үүнийг илрүүлэх бараг боломжгүй юм. Мөн онолын үнэн зөв эсэхийг шалгах нь зөвхөн алс холын ирээдүйн асуудал юм шиг санагддаг.
Бусад бүх металлын устөрөгчийн деривативтай харьцуулахад устөрөгчийн торийн харилцан үйлчлэлийн бүтээгдэхүүн нь дараахь зүйлийг агуулдаг. хамгийн их тооустөрөгч бөгөөд найрлага нь ThH 3.75 харьцаатай тохирч, өөрөөр хэлбэл IV бүлгийн элементүүдийн хамгийн их валенттай тохирох найрлагад ойртдог. Устөрөгч агуулсан торийн нягт нь металлын нягтаас бараг 30% бага байдаг бол титан дэд бүлгийн бусад элементүүдийн хувьд устөрөгчтэй харилцан үйлчлэх үед нягтын өөрчлөлт нь ойролцоогоор 15% байдаг.
Нүүрстөрөгчийн дэд бүлгийн элементүүдийн хамгийн энгийн гидридүүд - нүүрстөрөгч, цахиур, германий, цагаан тугалга, хар тугалга нь дөрвөн валент бөгөөд MeH 4 ерөнхий томъёотой тохирч байна. IV бүлгийн элементүүдийн гидридийн дулааны тогтвортой байдал нь эдгээр элементүүдийн атомын жин ба атомын радиус нэмэгдэх тусам аажмаар буурдаг.
Ванадийн дэд бүлэг В бүлгүүд . Устөрөгчийн ванадий, ниобий, танталтай харилцан үйлчлэл нь бараг ижил байдаг. Эдгээр системд яг стехиометрийн найрлагатай химийн нэгдлүүд олдсонгүй. Устөрөгчийн шингээлт ба десорбци нь металл танталын бүтцэд эргэлт буцалтгүй өөрчлөлтийг үүсгэдэг тул тантал-устөрөгчийн системд, ниоби-устөрөгчийн системд тодорхой хэмжээний завсрын төрлийн химийн холбоо үүсэх боломжтой байдаг.
Азот, фосфор, хүнцэл, сурьма, висмутын энгийн гидридүүд нь ерөнхий томъёо MeH3. V бүлгийн элементүүдийн гидридүүд нь IV ба VI бүлгийн элементүүдээс бага тогтвортой байдаг. V бүлгийн ихэнх элементүүд нь NH 3 зэрэг энгийн гидридүүдээс гадна устөрөгчтэй илүү төвөгтэй нэгдлүүдийг үүсгэдэг.
Хромын дэд бүлгийн элементүүдээс VI бүлэг - хром, молибден, вольфрам, уран, зөвхөн ураны гидрид UH 3-ыг судалсан. Энэ нэгдэл дэх химийн холбоо нь UH 3-ийн шинж чанартай нийцэж байгаа ковалентаар биш харин устөрөгчийн гүүр байгаагаар тайлбарлагдана. Ураны гидрид үүсэх нь ураны нягтын огцом бууралт (бараг 42%) дагалддаг. Энэхүү нягтралын бууралтын зэрэг нь судлагдсан металлын устөрөгчийн деривативуудын дунд хамгийн дээд хэмжээ бөгөөд хэмжээ нь I бүлгийн шүлтлэг металлын гидрид үүсэх үед ажиглагдсан нягтын өсөлттэй тохирч байна. Устөрөгчийн хром, молибден, вольфрамтай харилцан үйлчлэлцэх замаар нарийн стехиометрийн найрлагатай химийн нэгдлүүдийг үйлдвэрлэх талаар найдвартай мэдээлэл байдаггүй.
Энэ бүлгийн элементүүдийн гидридийг устөрөгчтэй элементүүдийн шууд харилцан үйлчлэлээр олж авч болно. H 2 O, H 2 S, H 2 Se, H 2 Te ба H 2 Ro цувралд гидридийн дулааны тогтвортой байдал хурдан буурдаг.
Устөрөгчийн элементүүдтэй химийн харилцан үйлчлэлийн талаар VIII бүлэг тогтмол хүснэгт - төмөр, никель, кобальт - уран зохиолд зөрчилтэй өгөгдөл байдаг. Мэдээжийн хэрэг, эдгээр элементүүдийн гидридийн бодит оршин тогтнолын талаар эргэлзээ төрж байна. Өндөр температурт устөрөгчийн төмөр, кобальт, никельтэй харилцан үйлчлэлцэх нь нийтээр хүлээн зөвшөөрөгдсөн утгаараа химийн процесс биш юм. Гэсэн хэдий ч энэ нь эдгээр элементийн гидрид байх боломжгүй гэдгийг хараахан нотлоогүй байна.
Олон судлаачид гидрид гэж үздэг бүтээгдэхүүн олж авсан гэж мэдээлсэн. Тиймээс төмрийн гидридийн шууд бус үйлдвэрлэлийн тухай мэдээлэл байдаг - FeH, FeH 2 ба FeH 3, тэдгээр нь 150 хэмээс доош температурт тогтвортой байдаг ба түүнээс дээш задардаг. Никель, кобальт гидридийн үйлдвэрлэл бас бүртгэгдсэн. Үүссэн бүтээгдэхүүн нь бараан өнгөтэй, нилээд тархсан пирофор нунтаг байв. Зарим зохиогчдын үзэж байгаагаар энэ төрлийн бодисууд нь үнэндээ гидрид биш, харин гадаргуу дээр физик шингэсэн их хэмжээний устөрөгч агуулсан, нарийн тархсан бууруулсан металлууд юм. Бусад нь шингэсэн устөрөгч нь атомын төлөвт металын гадаргуу дээр байдаг гэж үздэг химийн холбоометаллын атомуудтай.
Устөрөгчийн VIII бүлгийн бусад элементүүдтэй химийн харилцан үйлчлэлийн талаар маш бага тогтвортой мэдээлэл байдаг (палладийг эс тооцвол).
Хүснэгтэнд Хүснэгт 5-д устөрөгчтэй харилцан үйлчлэх үед металлын нягтын өөрчлөлтийн талаархи мэдээллийг харуулав.
Тарилгын холболтын найрлагаас эхэлье. Шилжилтийн элементүүдийн гидридийн жишээн дээр энэ асуудлыг авч үзье. Хэрэв завсрын үе шат үүсэх үед устөрөгчийн атомууд зөвхөн металл тор дахь тетраэдр хоосон зайд унадаг бол ийм нэгдэл дэх хязгаарлагдмал устөрөгчийн агууламж нь MeH 2 томьёотой тохирч байх ёстой (энэ нь Ме нь атомууд нь нягт савлагаа үүсгэдэг металл юм. ). Эцсийн эцэст, торонд тетраэдрийн хоосон зай нь хоорондоо нягт савлаж буй атомуудаас хоёр дахин их байдаг. Хэрэв устөрөгчийн атомууд зөвхөн октаэдр хоосон зайд унадаг бол ижил дүгнэлтээс үзэхэд устөрөгчийн хязгаарлагдмал агууламж нь MeH томьёотой тохирч байх ёстой - нягт савлагаа дахь олон тооны октаэдр хоосон зай нь энэ савлагааг бүрдүүлдэг атомууд байдаг.
Ихэвчлэн шилжилтийн металлын нэгдлүүд устөрөгчтэй үүсэх үед октаэдр эсвэл тетраэдр хоосон зайг дүүргэдэг. Эхлэх материалын шинж чанар, үйл явцын нөхцлөөс хамааран бүрэн эсвэл хэсэгчлэн дүүргэх боломжтой. Сүүлчийн тохиолдолд нэгдлийн найрлага нь бүхэл тоон томъёоноос хазайж, тодорхойгүй байх болно, жишээлбэл MeH 1-x; MeN 2-x. Хэрэгжилтийн холболтууд нь мөн чанараараа байх ёстой хувьсах найрлагатай нэгдлүүд,өөрөөр хэлбэл, тэдгээрийн найрлага нь тэдгээрийг бэлтгэх, цаашдын боловсруулалт хийх нөхцлөөс хамааран нэлээд өргөн хүрээнд өөр өөр байдаг.
Устөрөгчтэй нэгдлүүдийн жишээг ашиглан завсрын фазын зарим шинж чанарыг авч үзье. Үүнийг хийхийн тулд зарим шилжилтийн элементийн гидридийг гидридтэй харьцуулна шүлтлэг металл(литий).
Лити нь устөрөгчтэй нэгдэх үед LiH тодорхой найрлагатай бодис үүсдэг. By физик шинж чанарЭнэ нь анхны металлтай ямар ч нийтлэг зүйлгүй. Лити нь цахилгаан гүйдэл дамжуулдаг, металл гялбаа, уян хатан чанар, нэг үгээр хэлбэл бүхэл бүтэн цогцолбор юм. металл шинж чанар. Лити гидрид эдгээр шинж чанаруудын аль нь ч байдаггүй. Энэ бол өнгөгүй давстай төстэй бодис бөгөөд металтай огт адилгүй. Бусад шүлтлэг ба шүлтлэг шороон металлын гидридийн нэгэн адил литийн гидрид нь ердийн ионы нэгдэл бөгөөд литийн атом нь эерэг цэнэгтэй, устөрөгчийн атом нь адилхан сөрөг цэнэгтэй байдаг. Литийн нягт нь 0.53 г/см 3, литийн гидридийн нягт 0.82 г/см 3 - тохиолддог. нягтралын мэдэгдэхүйц өсөлт. (Бусад шүлтлэг ба шүлтлэг шороон металлын гидрид үүсэх үед ижил зүйл ажиглагддаг).
Палладий (шилжилтийн ердийн элемент) устөрөгчтэй харьцахдаа огт өөр өөрчлөлтөд ордог. Сайн мэддэг үзүүлэх туршлага, нэг талдаа хий нэвтэрдэггүй лакаар бүрсэн палладийн хавтан нь устөрөгчөөр үлээхэд нугалж байна.
Энэ нь үүссэн палладий гидридын нягт багассантай холбоотой юм. Энэ үзэгдэл зөвхөн металлын атомуудын хоорондох зай ихсэх үед л тохиолдож болно. Оруулсан устөрөгчийн атомууд нь металлын атомуудыг "түлхэж", болор торны шинж чанарыг өөрчилдөг.
Устөрөгчийг шингээх үед металлын хэмжээ нэмэгдэж, завсрын үе шат үүсэх нь маш мэдэгдэхүйц бөгөөд устөрөгчөөр ханасан металлын нягт нь анхны металлын нягтаас хамаагүй бага болж хувирдаг (Хүснэгт 2-ыг үз).
Хатуухан хэлэхэд металын атомуудаас үүссэн тор нь устөрөгчийг энэ металлаар шингээж авсны дараа ихэвчлэн өөрчлөгдөөгүй хэвээр үлддэг. Устөрөгчийн атом хичнээн жижиг байсан ч энэ нь торонд гажуудал үүсгэдэг. Энэ тохиолдолд ихэвчлэн тор дахь атомуудын хоорондын зай пропорциональ нэмэгдэхээс гадна түүний тэгш хэмийн зарим өөрчлөлтүүд байдаг. Тиймээс устөрөгчийн атомыг хоосон зайд өтгөн савлагаатай оруулдаг гэж энгийнээр хэлдэг - устөрөгчийн атомыг оруулах үед металл атомын нягт савлагаа тасалдсан хэвээр байна.
Хүснэгт 2 Устөрөгчтэй завсрын фаз үүсэх үед зарим шилжилтийн металлын нягтын өөрчлөлт.
Энэ нь ердийн болон шилжилтийн металлын гидридын цорын ганц ялгаанаас хол байна.
Завсрын гидрид үүсэх үед металлын гялбаа, цахилгаан дамжуулах чанар зэрэг металлын ердийн шинж чанарууд хадгалагдана. Үнэн, тэдгээр нь үндсэн металлаас бага тод томруун байж магадгүй юм. Тиймээс завсрын гидридүүд нь шүлтлэг ба шүлтлэг шороон металлын гидридээс илүү эх металлуудтай илүү төстэй байдаг.
Хуванцар чанар гэх мэт шинж чанар нь илүү их өөрчлөгддөг - устөрөгчөөр ханасан металууд хэврэг болдог, ихэвчлэн анхны металууд нунтаг болж хувирах нь хэцүү байдаг, гэхдээ ижил металлын гидридийн хувьд энэ нь илүү хялбар байдаг.
Эцэст нь бид завсрын гидридийн маш чухал шинж чанарыг тэмдэглэх хэрэгтэй. Шилжилтийн металууд устөрөгчтэй харилцан үйлчлэхэд металлын дээж устдаггүй. Үүнээс гадна, энэ нь анхны хэлбэрээ хадгалдаг. Урвуу үйл явцын үед ижил зүйл тохиолддог - гидридийн задрал (устөрөгчийн алдагдал).
Байгалийн асуулт гарч ирж магадгүй: завсрын үе шат үүсэх үйл явцыг үгийн бүрэн утгаараа химийн гэж үзэж болох уу? Илүү их "хими" агуулсан усан уусмал үүсэх боломжтой юу?
Хариулахын тулд бид химийн термодинамикийг ашиглах хэрэгтэй.
Энгийн бодисоос (мөн бусад химийн процессууд) химийн нэгдлүүд үүсэх нь ихэвчлэн мэдэгдэхүйц эрчим хүчний нөлөөлөл дагалддаг гэдгийг мэддэг. Ихэнх тохиолдолд эдгээр нөлөө нь экзотермик бөгөөд илүү их энерги ялгарах тусам үүссэн холболт илүү хүчтэй болдог.
Дулааны нөлөөлөл нь зөвхөн бодис холилдохоос гадна химийн урвал явагдаж байгааг илтгэх хамгийн чухал шинж тэмдгүүдийн нэг юм. Системийн дотоод энерги өөрчлөгдсөний дараа шинэ холболтууд үүсдэг.
Завсрын гидрид үүсэхэд ямар эрч хүчтэй нөлөө үзүүлдэгийг одоо харцгаая. Эндээс харахад нэлээд том тархалттай байна. Тогтмол системийн бүлгийн III, IV, V хажуугийн дэд бүлгийн металлуудад завсрын гидрид үүсэх нь 30-50 ккал / моль (энгийн бодисоос литийн гидрид үүсэх үед) дулаан ялгарах замаар дагалддаг. , ойролцоогоор 21 ккал/моль ялгардаг). Завсрын гидридүүд, дор хаяж заасан дэд бүлгүүдийн элементүүд нь нэлээд "бодит" гэдгийг хүлээн зөвшөөрч болно. химийн нэгдлүүд. Гэхдээ шилжилтийн цуврал бүрийн хоёрдугаар хагаст байрладаг олон металлын хувьд (жишээлбэл, төмөр, никель, зэс) завсрын гидрид үүсэх энергийн нөлөө бага байдаг гэдгийг тэмдэглэх нь зүйтэй. Жишээлбэл, ойролцоогоор FeH 2 найрлагатай гидридын хувьд дулааны нөлөө нь ердөө 0.2 ккал/моль байна. .
Ийм гидридийн DN-ийн бага утга нь тэдгээрийг бэлтгэх аргуудыг зааж өгдөг - металлын устөрөгчтэй шууд харилцан үйлчлэхгүй, харин шууд бус арга юм.
Хэд хэдэн жишээг харцгаая.
Найрлага нь NiH 2-тэй ойролцоо байдаг никель гидридийг никель хлоридын эфирийн уусмалыг H 2 урсгалд фенилмагнийн бромидоор эмчлэх замаар олж авч болно.
Энэ урвалын үр дүнд олж авсан никель гидрид нь хар нунтаг бөгөөд устөрөгчийг амархан ялгаруулдаг (энэ нь ерөнхийдөө завсрын гидридийн шинж чанар юм); хүчилтөрөгчийн агаар мандалд бага зэрэг халах үед гал авалцдаг.
Үүнтэй адилаар никелийн хөршүүдийн гидридийг олж авч болно. тогтмол хүснэгт- кобальт ба төмөр.
Шилжилтийн гидрид бэлтгэх өөр нэг арга нь литийн аланат LiAlH ашиглахад суурилдаг.Харгалзах металлын хлорид нь эфирийн уусмалд LiAlH 4-тэй урвалд ороход энэ металлын аланат үүснэ.
MeCl 2 +LiAlH 4 >Би(AlH 4 ) 2 +LiCl(5)
Олон металлын хувьд аланатууд нь температур нэмэгдэхэд задардаг эмзэг нэгдлүүд юм.
Би(AlH 4 ) 2 >MeH 2 + Al + H 2 (6)
Гэхдээ хоёрдогч дэд бүлгийн зарим металлын хувьд өөр процесс явагддаг.
Би(AlH 4 ) 2 >MeH 2 +AlH 3 (7)
Энэ тохиолдолд устөрөгч ба хөнгөн цагааны хольцын оронд эфирт уусдаг хөнгөн цагаан гидрид үүсдэг. Урвалын бүтээгдэхүүнийг эфирээр угааснаар цэвэр шилжилтийн металл гидридийг үлдэгдэл болгон авч болно. Ийм аргаар жишээлбэл цайр, кадми, мөнгөн усны тогтвортой байдал багатай гидридүүдийг гаргаж авсан.
Хажуугийн дэд бүлгийн элементүүдийн гидридийг бэлтгэх нь органик бус синтезийн ердийн аргууд дээр суурилдаг гэж дүгнэж болно: солилцооны урвал, тодорхой нөхцөлд эмзэг нэгдлүүдийн дулааны задрал гэх мэт Эдгээр аргуудаар бараг бүх шилжилтийн элементүүдийн гидридүүд, тэр ч байтугай маш хэврэгүүдийг олж авсан. Үүссэн гидридийн найрлага нь ихэвчлэн стехиометрийн ойролцоо байдаг: FeH 2, CoH 2, NiH 2 ZnH 2, CdH 2, HgH 2. Эдгээр урвал явагддаг бага температур нь стехиометрийн амжилтыг хөнгөвчлөх бололтой.
Одоо үүссэн завсрын гидридийн найрлагад урвалын нөхцлийн нөлөөг авч үзье. Энэ нь Ле Шательегийн зарчмаас шууд гардаг. Устөрөгчийн даралт ихсэх, температур бага байх тусам металын устөрөгчөөр ханасан байдал нь хязгаарлах утгад ойртдог. Өөрөөр хэлбэл, тодорхой температур, даралтын утга тус бүр нь металын устөрөгчөөр ханасан тодорхой зэрэгтэй тохирч байна. Үүний эсрэгээр, температур бүр нь металлын гадаргуу дээрх устөрөгчийн тодорхой тэнцвэрт даралттай тохирч байна.
Шилжилтийн элементийн гидридийн боломжит хэрэглээний нэг нь эндээс гаралтай. Зарим системд та хатуу тодорхойлсон устөрөгчийн даралтыг бий болгох хэрэгтэй гэж үзье. Устөрөгчөөр ханасан металыг ийм системд байрлуулсан (туршилтанд титан ашигласан). Тодорхой температурт халааснаар та систем дэх устөрөгчийн хийн шаардлагатай даралтыг бий болгож чадна.
Аливаа ангиллын нэгдлүүд өөрийн гэсэн сонирхолтой байдаг химийн шинж чанар, тэдгээрийн бүрдэх хэсгүүдийн бүтэц, бүтэц, эдгээр хэсгүүдийн хоорондын холболтын шинж чанар. Химичид онолын болон туршилтын ажлаа үүнд зориулдаг. Тэд хэрэгжүүлэх үе шатаас үл хамаарах зүйл биш юм.
Завсрын гидридийн мөн чанарын талаар тодорхой үзэл бодол хараахан гараагүй байна. Ихэнхдээ өөр өөр, заримдаа эсрэг тэсрэг үзэл бодол нь ижил баримтуудыг амжилттай тайлбарладаг. Өөрөөр хэлбэл, завсрын нэгдлүүдийн бүтэц, шинж чанарын талаар нэгдсэн онолын үзэл бодол хараахан гараагүй байна.
Зарим туршилтын баримтуудыг авч үзье.
Палладий устөрөгчийг шингээх үйл явцыг хамгийн нарийн судалсан. Тогтмол температурт ууссан устөрөгчийн концентраци нь гадаад устөрөгчийн даралтын квадрат язгууртай пропорциональ байдаг нь энэхүү шилжилтийн металлын онцлог юм.
Ямар ч температурт устөрөгч нь тодорхой хэмжээгээр чөлөөт атомуудад задардаг тул тэнцвэрт байдал бий болно.
Энэ тэнцвэрийн тогтмол нь:
Хаана Р Н -- атомын устөрөгчийн даралт (концентраци).
Эндээс (11)
Хийн фаз дахь атомын устөрөгчийн концентраци нь молекул устөрөгчийн даралтын квадрат язгууртай пропорциональ байгааг харж болно. Гэхдээ палладий дахь устөрөгчийн концентраци нь ижил утгатай пропорциональ байна.
Эндээс бид палладий устөрөгчийг бие даасан атом хэлбэрээр уусгадаг гэж дүгнэж болно.
Тэгэхээр палладий гидрид дэх бондын шинж чанар юу вэ? Энэ асуултад хариулахын тулд хэд хэдэн туршилт хийсэн.
Хажуугаар нь өнгөрөхдөө тэр нь тогтоогдсон цахилгаан гүйдэлустөрөгчөөр ханасан палладигаар дамжин металл бус атомууд катод руу шилждэг. Металл торонд агуулагдах устөрөгч нь протон (жишээ нь, H + ион) болон электронуудад бүрэн эсвэл хэсэгчлэн задардаг гэж үзэх ёстой.
тухай мэдээлэл цахим бүтэцсоронзон шинж чанарыг судлах замаар палладийн гидридийг олж авсан. Гидридын соронзон шинж чанар нь бүтцэд орж буй устөрөгчийн хэмжээнээс хамаарч өөрчлөгдөхийг судалсан. Бодисын соронзон шинж чанарыг судалсны үндсэн дээр энэ бодисоос бүрдэх хэсгүүдэд агуулагдах хосгүй электронуудын тоог тооцоолох боломжтой. Дунджаар нэг палладийн атомд ойролцоогоор 0.55 хосгүй электрон байдаг. Палладий устөрөгчөөр ханасан үед хосгүй электронуудын тоо буурдаг. Мөн PdH 0.55 найрлагатай бодист хосгүй электрон бараг байдаггүй.
Эдгээр өгөгдлүүд дээр үндэслэн бид дараах дүгнэлтийг хийж болно: хосгүй палладийн электронууд нь устөрөгчийн атомын хосгүй электронуудтай хос үүсгэдэг.
Гэсэн хэдий ч завсрын гидридийн шинж чанарыг (ялангуяа цахилгаан ба соронзон) эсрэг таамаглал дээр үндэслэн тайлбарлаж болно. Завсрын гидридүүд нь металл торонд агуулагдах хагас чөлөөт электронуудын нэг хэсгийг устөрөгчийн атомууд барьж авсны улмаас үүсдэг H - ионуудыг агуулдаг гэж үзэж болно. Энэ тохиолдолд металаас гаргаж авсан электронууд нь устөрөгчийн атомууд дээр байгаа электронуудтай хосууд үүсгэдэг. Энэ арга нь соронзон хэмжилтийн үр дүнг мөн тайлбарладаг.
Хоёр төрлийн ион завсрын гидридэд зэрэгцэн орших боломжтой. Металл электрон ба устөрөгчийн электронууд хос үүсгэдэг тул а ковалент холбоо. Эдгээр электрон хосуудыг нэг градус эсвэл өөр атомын аль нэг рүү - металл эсвэл устөрөгч рүү шилжүүлж болно.
Электрон хос нь палладий эсвэл никель гидрид зэрэг электрон өгөх магадлал багатай металлын гидрид дэх металлын атом руу илүү чиглэнэ. Гэхдээ сканди ба ураны гидридүүдэд электрон хос устөрөгч рүү хүчтэй шилждэг бололтой. Тиймээс лантанид ба актинидын гидрид нь олон талаараа шүлтлэг шороон металлын гидридтэй төстэй байдаг. Дашрамд хэлэхэд лантан гидрид нь LaH 3 найрлагад хүрдэг. Ердийн завсрын гидридийн хувьд бидний мэдэж байгаагаар устөрөгчийн агууламж нь MeH эсвэл MeH 2 томъёонд харгалзах хэмжээнээс ихгүй байна.
Өөр нэг туршилтын баримт нь завсрын гидрид дэх бондын шинж чанарыг тодорхойлоход бэрхшээлтэй байгааг харуулж байна.
Хэрэв бага температурт палладийн гидридээс устөрөгчийг салгавал устөрөгчөөр ханасан палладийд байсан гажсан ("өргөсөн") торыг хадгалах боломжтой. Ийм палладийн соронзон шинж чанар (үүнийг анхаарна уу), цахилгаан дамжуулах чанар, хатуулаг нь гидридийнхтэй ерөнхийдөө ижил байдаг.
Эндээс үзэхэд завсрын гидрид үүсэх явцад шинж чанарын өөрчлөлт нь зөвхөн тэдгээрийн доторх устөрөгч байгаа эсэхээс гадна тор дахь атом хоорондын зайны өөрчлөлтөөс үүдэлтэй юм.
Завсрын гидридийн мөн чанарын тухай асуудал маш нарийн төвөгтэй бөгөөд эцэслэн шийдэгдээгүй гэдгийг бид хүлээн зөвшөөрөх ёстой.
Хүн төрөлхтөн аливаа үзэгдлийн бүхий л талыг бүрэн мэдэхгүй байсан ч эдгээр үзэгдлүүдийг бодитоор ашиглах боломжтой байдгаараа үргэлж алдартай байсан. Энэ нь завсрын гидридүүдэд бүрэн хамаарна.
Зарим тохиолдолд завсрын гидрид үүсэх нь практикт зориудаар ашиглагддаг бол бусад тохиолдолд эсрэгээр тэд үүнээс зайлсхийхийг хичээдэг.
Завсрын гидрид нь халаахад, заримдаа бага температурт устөрөгчийг харьцангуй амархан ялгаруулдаг. Би энэ өмчийг хаана ашиглаж болох вэ? Мэдээжийн хэрэг, исэлдэлтийн процесст. Түүнээс гадна завсрын гидридээс ялгарах устөрөгч нь процессын зарим үе шатанд атомын төлөвт байдаг. Энэ нь завсрын гидридийн химийн идэвхжилтэй холбоотой байж магадгүй юм.
Наймдугаар бүлгийн металлууд (төмөр, никель, цагаан алт) нь устөрөгчийг аливаа бодист холбох урвалын сайн катализатор гэдгийг мэддэг. Магадгүй тэдний катализаторын үүрэг нь тогтворгүй завсрын гидридийн завсрын үүсэхтэй холбоотой байж болох юм. Цаашид задрах замаар гидрид нь урвалын системийг тодорхой хэмжээний атомын устөрөгчөөр хангадаг.
Жишээлбэл, нарийн тархсан цагаан алт (цагаан алтны хар гэж нэрлэгддэг) нь устөрөгчийг хүчилтөрөгчөөр исэлдүүлэх процессыг хурдасгадаг - түүний дэргэд энэ урвал нь өрөөний температурт ч мэдэгдэхүйц хурдтай явагддаг. Цагаан алтны хар өнгийн энэ шинж чанарыг түлшний эсүүд - төхөөрөмжүүдэд ашигладаг химийн урвалдулааны эрчим хүчний үйлдвэрлэлийг (шаталтын үе шат) алгасаж шууд цахилгаан эрчим хүч үйлдвэрлэхэд ашигладаг. Уусмалын цахилгаан химийн шинж чанарыг судлах чухал хэрэгсэл болох устөрөгчийн электрод нь нарийн тархсан цагаан алтны ижил шинж чанар дээр суурилдаг.
Завсрын гидрид үүсэх нь өндөр цэвэр металлын нунтаг авахад ашиглагддаг. Уран металл болон бусад актинид, түүнчлэн маш цэвэр титан, ванади нь уян хатан байдаг тул металлыг нунтаглах замаар тэдгээрээс нунтаг бэлтгэх бараг боломжгүй юм. Металлыг уян хатан чанараас нь салгахын тулд устөрөгчөөр ханасан (энэ үйлдлийг металлын "хэврэгжилт" гэж нэрлэдэг). Үүссэн гидрид нь амархан нунтагладаг. Зарим металлууд устөрөгчөөр ханасан ч нунтаг төлөвт (уран) хувирдаг. Дараа нь вакуумд халаахад устөрөгчийг зайлуулж, үлдсэн зүйл нь цэвэр металлын нунтаг юм.
Зарим гидридийн (UH 3, TiH 2) дулааны задралыг цэвэр устөрөгч үйлдвэрлэхэд ашиглаж болно.
Титан гидридийн хэрэглээний хамгийн сонирхолтой газрууд. Энэ нь хөөс металл (жишээлбэл, хөнгөн цагаан хөөс) үйлдвэрлэхэд ашиглагддаг. Үүнийг хийхийн тулд гидридийг хайлсан хөнгөн цагаанд оруулна. Өндөр температурт энэ нь задарч, үүссэн устөрөгчийн бөмбөлөгүүд нь шингэн хөнгөн цагааныг хөөсөрдөг.
Титан гидридийг зарим металлын ислийг бууруулах бодис болгон ашиглаж болно. Энэ нь металл эд ангиудыг холбох гагнуурын үүрэг гүйцэтгэдэг бөгөөд нунтаг металлургийн металлын тоосонцорыг задлах процессыг хурдасгадаг бодис юм. Сүүлийн хоёр тохиолдолд тэдгээрийг бас ашигладаг нөхөн сэргээх шинж чанаргидрид. Металл тоосонцор болон металл эд ангиудын гадаргуу дээр ихэвчлэн ислийн давхарга үүсдэг. Энэ нь металлын зэргэлдээ хэсгүүдийг наалдуулахаас сэргийлдэг. Халах үед титан гидрид нь эдгээр ислийг багасгаж, улмаар металлын гадаргууг цэвэрлэнэ.
Титан гидридийг зарим тусгай хайлш үйлдвэрлэхэд ашигладаг. Хэрэв энэ нь зэсийн бүтээгдэхүүний гадаргуу дээр задарвал зэс-титан хайлшийн нимгэн давхарга үүснэ. Энэ давхарга нь бүтээгдэхүүний гадаргуугийн тусгай механик шинж чанарыг өгдөг. Тиймээс та хэд хэдэн бүтээгдэхүүнийг нэг бүтээгдэхүүнд нэгтгэж болно чухал шинж чанарууд(цахилгаан дамжуулалт, хүч чадал, хатуулаг, элэгдэлд тэсвэртэй гэх мэт).
Эцэст нь, титан гидрид нь нейтрон, гамма туяа болон бусад хатуу цацрагаас хамгаалах маш үр дүнтэй хэрэгсэл юм.
Заримдаа эсрэгээрээ завсрын гидрид үүсэхтэй тэмцэх хэрэгтэй болдог. Металлурги, хими, газрын тос болон бусад үйлдвэрүүдэд устөрөгч эсвэл түүний нэгдлүүд нь даралт, өндөр температурт байдаг. Ийм нөхцөлд устөрөгч нь халсан металлаар тодорхой хэмжээгээр тархаж, төхөөрөмжөөс зүгээр л "явдаг" болно. Нэмж дурдахад (мөн энэ нь магадгүй хамгийн чухал юм!), завсрын гидрид үүссэний улмаас металл тоног төхөөрөмжийн бат бөх чанарыг ихээхэн бууруулж болно. Энэ нь өндөр даралттай ажиллахад аль хэдийн ноцтой аюул учруулж байна.
Устөрөгчийг гидрид хэлбэрээр хадгалснаар шахсан устөрөгчийн хийг хадгалахад их хэмжээний, хүнд цилиндр, шингэн устөрөгчийг хадгалахад хэцүү, үнэтэй сав шаардагдахгүй. Устөрөгчийг гидрид хэлбэрээр хадгалах үед системийн эзэлхүүн нь цилиндрт хадгалах хэмжээтэй харьцуулахад ойролцоогоор 3 дахин багасдаг. Устөрөгчийн тээвэрлэлтийг хялбаршуулсан. Устөрөгчийг хувиргах, шингэрүүлэх зардал гарахгүй.
Металл гидридээс устөрөгчийг гидролиз ба диссоциаци гэсэн хоёр урвалаар гаргаж авч болно.
Гидролизийн аргаар гидрид агуулагдах устөрөгчөөс хоёр дахин их устөрөгч авах боломжтой. Гэсэн хэдий ч энэ үйл явц нь бараг эргэлт буцалтгүй юм. Гидридийн дулааны диссоциацийн аргаар устөрөгчийг үйлдвэрлэх арга нь систем дэх температур, даралтын бага зэрэг өөрчлөлт нь гидрид үүсэх урвалын тэнцвэрт байдалд мэдэгдэхүйц өөрчлөлт оруулахад хүргэдэг устөрөгчийн аккумляторыг бий болгох боломжийг олгодог.
Устөрөгчийг гидрид хэлбэрээр хадгалах суурин төхөөрөмжүүд нь масс, эзэлхүүний хувьд хатуу хязгаарлалтгүй байдаг тул тодорхой гидридийг сонгоход хязгаарлах хүчин зүйл нь түүний өртөг байх болно. Зарим хэрэглээний хувьд ванадийн гидрид нь 270 К-тэй ойролцоо температурт сайн задалдаг тул ашигтай байж болох юм. Магнийн гидрид нь харьцангуй хямд боловч диссоциацийн температур нь 560-570 К, үүсэх өндөр дулаантай байдаг. Төмөр-титан хайлш нь харьцангуй хямд бөгөөд түүний гидрид нь 320-370 К-ийн температурт бага дулаан үүсэх үед задалдаг.
Гидрид ашиглах нь аюулгүй байдлын чухал давуу талтай. Гэмтсэн устөрөгчийн гидридын сав нь гэмтсэн шингэн устөрөгчийн сав эсвэл устөрөгчөөр дүүрсэн даралтат савнаас хамаагүй бага аюул учруулдаг.
Устөрөгчийг металтай холбох нь дулаан ялгарах үед явагдах нь чухал юм. Металлын M устөрөгчөөс гидрид үүсэх экзотермик процесс (цэнэглэх) ба гидридээс устөрөгчийг ялгаруулах (цэнэглэх) эндотермик процессыг дараахь урвалын хэлбэрээр илэрхийлж болно.

Гидридийн техникийн хэрэглээний хувьд гидрид дэх устөрөгчийн диссоциацийн даралт 0.1 МПа-аас дээш утгад хүрэх температур нь онцгой ач холбогдолтой юм. Усны хөлдөх цэгээс доош температурт 0.1 МПа-аас дээш диссоциацийн даралтыг бий болгодог гидридийг бага температур гэж нэрлэдэг. Хэрэв энэ даралт нь ус буцалгах цэгээс дээш температурт хүрсэн бол ийм гидридийг өндөр температурт тооцно.
Зам тээврийн хэрэгцээнд онолын хувьд 1 м 3 металл гидрид тутамд 130-140 кг устөрөгч агуулсан гидридүүдийг бий болгодог. Гэсэн хэдий ч гидридийн хүчин чадал нь 80 кг / м 3-аас хэтрэх магадлал багатай боловч 130 дм 3 багтаамжтай сав дахь устөрөгчийн агууламж нь 400 км замыг туулахад хангалттай юм. Эдгээр нь ашиглалтын бодит үзүүлэлт боловч гидридээр дүүргэсэн савны массын өсөлтийг анхаарч үзэх хэрэгтэй. Жишээлбэл, латан-никель гидридын масс 1 тонн, магнийн гидридийн жин 400 кг хүрдэг.
Өнөөдрийг хүртэл өргөн хүрээний шинж чанартай металл гидридүүдийг нэгтгэж, судалж байна. Үйлдвэрлэлийн хэрэгцээнд хамгийн их ашиг тустай зарим гидридын шинж чанарын талаархи мэдээллийг Хүснэгтэнд үзүүлэв. 10.3 ба 10.4. Хүснэгтээс харж болно. Жишээлбэл, магнийн гидрид нь 1 кг гидридийн масс тутамд 77 г H2 хадгалах боломжтой байдаг бол 20 МПа даралттай цилиндрт 1 кг саванд ердөө 14 г байдаг. Шингэн устөрөгчийн хувьд та 1 кг саванд 500 г хадгалж болно.
Устөрөгчийн эрчим хүч, түлшний эсийн эрэл хайгуул, судалгаа, хөгжлийн ажлын цогц хөтөлбөр нь палладий судлахаар төлөвлөж байна. Цагаан алтны бүлгийн металл палладий нь түлшний эс болон бүх устөрөгчийн энергийн гол материалын нэг юм. Үүний үндсэн дээр катализатор, цэвэр устөрөгч үйлдвэрлэх мембран төхөөрөмж, нэмэгдсэн материалууд функциональ шинж чанарууд, түлшний эс, электролизер, устөрөгчийг тодорхойлох мэдрэгч. Палладий нь устөрөгч, ялангуяа палладийн нано нунтагыг үр дүнтэй хуримтлуулж чаддаг.
Устөрөгчийн энергиээс гадна палладий нь ердийн автомашины яндангийн хийг цэвэрлэхэд катализаторт ашиглагддаг; усыг задлах замаар устөрөгч ба хүчилтөрөгч үйлдвэрлэх электролизер; зөөврийн түлшний эсүүд, ялангуяа метанол; палладий дээр суурилсан электрод бүхий хатуу исэл электролизер; агаараас хүчилтөрөгч авах төхөөрөмж, түүний дотор эмнэлгийн зориулалтаар; нарийн төвөгтэй хийн хольцыг шинжлэх мэдрэгч.
Манай улс устөрөгч үйлдвэрлэхэд шаардлагатай энэ металлын дэлхийн үйлдвэрлэлийн 50 орчим хувийг хянадаг гэдгийг тэмдэглэх нь зүйтэй. Одоогоор Черноголовка дахь Оросын ШУА-ийн Химийн физикийн хүрээлэнд металл гидрид дээр суурилсан устөрөгчийн батерейг бүтээх ажил хийгдэж байна.
Зарим гидридийн шинж чанарууд
Хүснэгт 10.3
Гидридийн системд ашигласан материалын хэд хэдэн онцлог шинж чанарыг нэрлэе.
1) HY-STOR барааны тэмдгийг агуулсан бүх хайлшийг Energies, Inc үйлдвэрлэдэг. Энэ догол мөрөнд өгөгдсөн ихэнх өгөгдлүүдийг Хьюстон, Сандрок нарын бүтээлээс авсан болно. Химийн томъёонд M тэмдэг нь ихэвчлэн моназитын тоосноос гаргаж авсан ховор металлын холимог болох мишметалыг илэрхийлдэг. Мишметалын тэгш өндөрлөгийн даралтад үзүүлэх нөлөө нь металын энэ хольц дахь цери ба лантаны харьцаанаас ихээхэн хамаардаг.
Талбайн налуу
Дараагийн догол мөрөнд тайлбарласан гидридийн системийн хялбаршуулсан термодинамик загварын дагуу тэнцвэрийн хамаарал дахь өндөрлөг | концентрацийн даралт хэвтээ байх ёстой. Гэсэн хэдий ч практик дээр; хатуу фаз дахь устөрөгчийн концентраци нэмэгдэхийн хэрээр өндөрлөг дээрх даралт бага зэрэг нэмэгддэг.
Талбайн налууг налуугийн коэффициент d n(pd)/d(H, M)-аар тоон байдлаар тодорхойлж болно, энд pd нь десорбцийн изотерм дээрх өндөрлөг дээрх даралт юм. Зураг дээр. 9.7, 25 ° C-д харгалзах десорбцийн изотермоор дамжин өнгөрөх тасархай шугам нь pd = 9.1 атм цэг дээр H/M = 0 босоо шугам, pd = 14.8 атм цэг дээр H/M = 1.2 шугамыг огтолж байна. Дараа нь
dlnpd 14.8-д 9.1
M) 1.2 ' ■ U '
Энэ коэффициентийн утгыг хүлээн зөвшөөрөх боломжтой.Жишээ нь TiFe хайлшийн хувьд тэнцвэрийн даралтын өндөрлөгийн налуугийн параметр нь тэг байхад зарим кальцийн хайлшийн хувьд энэ үзүүлэлтийн утга гурваас давсан байна. Хайлш хатуурах үед (үйлдвэрлэлийн шатанд) тусгаарлах хандлагатай байдаг, өөрөөр хэлбэл хайлшийг бүрдүүлдэг зарим элементүүдийг ялгаруулдаг. Энэ үзэгдэл нь тэгш өндөрлөгийн налуу үүсэх гол шалтгаан болж байгаа бололтой, учир нь термодинамикийн үүднээс авч үзвэл, нэгэн төрлийн хайлшийн хувьд тэнцвэрийн даралт нь устөрөгчийн концентрациас хамааралтай байх нь хэвтээ өндөрлөг байх ёстой. Материалыг нунтаглахын өмнө анивчих нь өндөрлөгийн налууг багасгаж болно. Налуугийн коэффициент болон бусад шинж чанаруудын утгыг хүснэгтэд үзүүлэв. 9.4, 9.5 ба 9.6.
Шингээх-десорбцийн гистерезис
Дээр дурьдсанчлан шингээлтийн үеийн өндөрлөг даралт нь ихэвчлэн десорбцийн үеийнхээс арай өндөр байдаг. Өөрөөр хэлбэл, хайлшийг циклээр цэнэглэх, цэнэглэх үед шингээлт ба десорбцийн процессын гистерезис ажиглагдаж байна (9.7-р зургийг үз).
9.8, 9.10 ба 9.11).
|
Хүснэгт 9.4. Зарим металл гидридийн термодинамик шинж чанар
|
|
өндөрлөгийн налуу8*, ^ |
Гистерезисийн коэффициент Па/Пд |
||
|
Хүснэгт 9.6. Зарим металл гидридийн устөрөгчийн хамгийн их агууламж ба дулааны багтаамж
|
Гистерезийн үзэгдэл нь болор торны хуванцар хэв гажилт, тухайлбал устөрөгчийг шингээх үед тэлэх, шахах үед дулаан ялгарах эргэлт буцалтгүй үйл явцтай холбоотой юм.
Гистерезисийн үзэгдэл нь AHM = 0.5, ихэвчлэн 25 ° C температурт шингээлт ба десорбцийн үед устөрөгчийн тэнцвэрт даралтын утгуудын харьцаагаар тоон тодорхойлогддог. Энэ харьцаа нь температураас хамаардаггүй гэдгийг ерөнхийд нь хүлээн зөвшөөрдөг.
Ашигтай хүчин чадал гэдэг нь гидрид дэх металлын атомд шингэсэн устөрөгчийн атомын тоо N/M өөрчлөгдөхөд даралт нь өндөрлөгийн даралтын 10 дахин их утгаас 0.1 өндөрлөгийн даралтын утга болж өөрчлөгдөхийг хэлнэ. Ашигтай хүчин чадлыг тодорхойлох энэ арга нь арай хэтрүүлсэн утгыг өгдөг. Хэрэв даралтын хүрээ мэдэгдэхүйц нарийссан бол илүү бодит утгыг олж авна.
Зураг дээр. 9.9 (Fe0 8ІЧІ(| 2Ті) хайлш) 70 0С-ийн температурт өндөрлөг дээрх даралт ойролцоогоор 0.9 атм байна.Заасан хэмжээнээс 10 дахин их даралттай үед N/M харьцаа 0.65, даралттай үед. Талбай дээрх даралтаас 10 дахин бага, Н/М = 0,02.Иймээс ялгаа A(N/M) = 0,63.Өөрөөр хэлбэл 1 кмоль гидридээс 0,63 кмоль атомын устөрөгч (0,63 кг) гаргаж авах боломжтой.
FeTi хайлш (9.4-р зургийг үзнэ үү)
Дулааны багтаамж
Гидридын системийг температурын өөрчлөлтөөр идэвхжүүлдэг. Ийм системийг зохион бүтээхийн тулд төрөл бүрийн хайлшийн дулааны багтаамжийн талаархи мэдээлэлтэй байх шаардлагатай. Хэд хэдэн хайлшийн дулааны багтаамжийн утгыг Хүснэгтэнд үзүүлэв. 9.6.
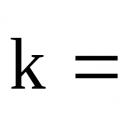 Урвалын хурдны тогтмол Лабораторийн ажлын удирдамж
Урвалын хурдны тогтмол Лабораторийн ажлын удирдамж Үхлийн дараах амьдрал бий юу?
Үхлийн дараах амьдрал бий юу? Эрдэмтэд: Дэлхий бол хүн төрөлхтний "сансрын шорон" Эрдэмтэд: Дэлхий бол сансрын шорон
Эрдэмтэд: Дэлхий бол хүн төрөлхтний "сансрын шорон" Эрдэмтэд: Дэлхий бол сансрын шорон