Фторын талаар сонирхолтой мэдээлэл. Химийн түүхийн зарим сонирхолтой баримтууд
Фторыг хэрхэн нээсэн
БАФторыг нээсэн түүх эмгэнэлт явдалаар дүүрэн байдаг. Чөлөөт фторыг ялгах туршилтууд шиг шинэ элементүүдийг илрүүлэх оролдлого урьд өмнө хэзээ ч ийм олон золиос болж байгаагүй. Энэ түүх ерөнхийд нь дараах байдалтай байна.
1670 онд Германы химич К.Шванквард хүхрийн хүчлээр хайлуур жоншоор хийсэн савыг авч шилэн хавтангаар таглавал ялгарах хийн нөлөөгөөр зэвэрдэг болохыг анзаарчээ.
1768 онд эрдэмтэн А.Марграф гидрофторын (гидрофторын) хүчлийг тодорхойлсон бөгөөд дараа нь 1771 онд К.Шээле судалжээ.
Улмаар К.Шээле, Ж.Престли нар жонш нь үл мэдэгдэх хүчлийн кальцийн давс гэсэн дүгнэлтэд хүрч, Шеэл үүнийг фтор гэж нэрлэхийг санал болгож, 1779 онд металл саванд үйлдвэрлэх аргыг тодорхойлсон. 30 жилийн дараа Ж.Гэй-Люссак, Л.Тенард нар усгүй фторын хүчил гаргаж авсан.
Алдарт физикч А.Ампер 1810 онд Г.Дэвигийн ажлын талаар мэдэж, хлорыг элемент гэж үзэх хандлагатай байсан тул фторын хүчилд хлор, иодтой төстэй шинж чанар бүхий элемент байх ёстой гэж санал болгожээ. Устөрөгчийн фторын хүчил нь фтор хэмээх тусгай элементтэй устөрөгчийн нэгдэл юм. Дэви энэ үзэл бодолтой бүрэн санал нийлж байна.
Латин нэр жоншлатин үгнээс гаралтай флюо- гоожих. Ингэж нэрлэх болсон шалтгаан нь Г.Агрикола гэдэг нэрээр мэддэг эрдсээр фторын хүчлийг гаргаж авсан явдал байв. жонш номин(флюорит – жонш – CaF 2). Энэ ашигт малтмалыг урсгал (флюс) хэлбэрээр удаан хугацаанд ашиглаж байсан тул цэнэгт нэмэхэд хүдрийн хайлах цэг буурдаг.
"Фтор" гэсэн нэрийг 1810 онд Ампер фторын хүчлийн шинж чанарыг илүү сайн мэддэг болсон үед нэвтрүүлсэн. Энэ үг грек хэлнээс гаралтай phthoros- хор хөнөөлтэй. Гэсэн хэдий ч энэ нэрийг зөвхөн Оросын химичүүд хүлээн зөвшөөрсөн бөгөөд бусад бүх оронд "флюор" гэсэн нэр хадгалагдан үлджээ.
МФторыг тусгаарлах олон оролдлого нь элементийн хүчтэй идэвхжилээс болж удаан хугацаанд амжилтгүй болсон бөгөөд тусгаарлах үед нь савны хана, ус гэх мэт харилцан үйлчлэлцдэг байв.
Устөрөгчийн фторын хүчлийг исэлдүүлэн үнэгүй фтор авах оролдлого бүтэлгүйтсэн төдийгүй фтор устөрөгчийн хүчтэй хордлогын улмаас хэд хэдэн хохирогч болсон.
Ирландын Шинжлэх ухааны академийн хоёр гишүүн болох ах дүү Жорж, Томас Нокс нар фторын анхны хохирогч болсон юм. Тэд жоншноос нэлээд овсгоотой аппарат хийсэн ч чөлөөт фтор авч чадаагүй. Удалгүй Томас Нокс хордлогын улмаас нас барж, түүний ах Жорж хөдөлмөрийн чадвараа алдаж, Неаполь хотод гурван жил эмчлүүлж, амрахаас өөр аргагүйд хүрчээ. Дараагийн хохирогч нь Брюсселийн химич П.Лайет байсан бөгөөд ах дүү Нокс туршилтын үр дагаврыг мэдсээр байж, амиа харамгүй үргэлжлүүлж, амь насаараа хохирсон. Нэнсигийн нэрт химич Ж.Никлс ч мөн адил амиа алдсан. Гей-Люссак, Тенард нар бага хэмжээний фтор устөрөгчийн уушгинд үзүүлэх нөлөөгөөр ихээхэн хохирол амссан. 1814 оноос хойш Дэвигийн өвчин нь устөрөгчийн фторын хордлоготой холбоотой юм. Эдгээр бүтэлгүйтэл нь Г.Роско чөлөөт фторыг ялгах асуудал нь "орчин үеийн химийн хамгийн хэцүү асуудлуудын нэг" гэж тунхаглахад хүргэсэн.
Гэвч химичүүд фторыг тусгаарлах найдвараа алдсангүй. Жишээлбэл, Дэви зөвхөн хээрийн жоншоор хийсэн саванд хийж гүйцэтгэсэн тохиолдолд фторын үйлдвэрлэл амжилттай болно гэдэгт итгэлтэй байсан.
Фторыг ялгах оролдлогыг Францын эрдэмтэн Э.Фреми, А.Моиссан багшийн хийсэн. Тэрээр усгүй фторын хүчлийг бэлтгэж, фторыг электролизээр авахыг хүссэн боловч хүчтэй идэвхжилтэй тул хий нь анод дээр үүссэнгүй.
1869 онд Английн цахилгаан химич Г.Гор тодорхой хэмжээний чөлөөт фтор олж авч чадсан боловч тэр даруй устөрөгчтэй (тэсрэлтээр) нийлэв. Энэ эрдэмтэн олон арван бодисыг анод (нүүрс, цагаан алт, палладий, алт гэх мэт) туршиж үзсэн боловч тэдгээрийг бүгдийг нь фтор устгасан болохыг тогтоож чадсан. Үүний зэрэгцээ тэрээр фторын идэвхийг сулруулахын тулд электролизерын температурыг бууруулах шаардлагатай гэсэн дүгнэлтэд хүрчээ.
Анри Мойсан
|
Эдгээр бүх оролдлого нь дэмий хоосон байсангүй бөгөөд 19-р зууны сүүл ба 20-р зууны эхэн үеийн Францын нэрт химич Моиссан дараагийн системчилсэн туршилтуудад харгалзан үзсэн. Moissan эхлээд цагаан алтнаас U хэлбэрийн электролизер бүтээж байсан боловч хожим үүнийг зэсээр ч хийж болох нь тогтоогдсон. Сүүлийнх нь зэсийн хайлуур жоншны нимгэн давхаргаар бүрсэн бөгөөд энэ нь фторыг цаашид өртөхөөс сэргийлдэг. Усгүй фторын хүчлийг электролит болгон авсан. Гэхдээ энэ бодис нь усгүй байдалд цахилгаан гүйдэл дамжуулдаггүй тул түүнд бага хэмжээний калийн гидродифторид KHF 2 нэмсэн. Шингэн устөрөгчийн хайлуур жоншийг олж авах, фторын идэвхийг бууруулахын тулд бүх төхөөрөмжийг этил хлорид C2H5Cl-тай хөргөх хольцонд дүрж, 12.5 ° C-т буцалгана. Үүний үр дүнд төхөөрөмжийг -23 хэм хүртэл хөргөнө. Электродууд нь цагаан алт эсвэл цагаан алтны иридидээр хийгдсэн бөгөөд ялгарсан фтортой урвалд ордоггүй жоншны залгуураар тусгаарлагдсан байв. Фторыг цуглуулахын тулд бусад зэс хоолойг боолтоор бэхэлсэн. Фторыг анх 1886 онд энэ төхөөрөмжөөс гаргаж авсан.
Хоёр хоногийн дараа Мойсан нээлтийн талаар Парисын Шинжлэх Ухааны Академид мэдэгдэв. Мойсан энэхүү мэдэгдэлдээ "Газрын хийн шинж чанарын талаар янз бүрийн таамаг дэвшүүлж болно. Бид фтортой харьцаж байна гэж таамаглах нь хамгийн энгийн зүйл боловч энэ нь полиустөрөгчийн хайлуур жонш байж магадгүй юм. Энэ хий нь талст цахиурын хүчилд үзүүлэх хүчтэй үйлдлийг тайлбарлахад хангалттай идэвхтэй байдаг фторын хүчил ба озоны холимог."
Моиссаны мэдэгдлийг академи хүлээн авч, түүний тогтоосон ёсоор нээлтийг шалгах нэр хүндтэй эрдэмтдийн тусгай хороог томилжээ. Туршилтын явцад Моиссаны аппарат дур булаам болж, туршилт хийсэн хүн фторын бөмбөлгийг ч авч чадахгүй байв.
Францын нэрт химич А.Л-ын түүх хадгалагдан үлджээ. Ле Шателье Моиссан анх Парисын Шинжлэх Ухааны Академид фторыг тусгаарлах туршилтыг хэрхэн явуулсан тухай.
"Нью Сорбонн (Парисын Их Сургууль) дахь Фриделийн лабораторид суралцах жижиг буланг хүлээн авсны дараа Мойсан хэсэг хугацааны дараа фторын элементийн үйлдвэрлэлийн туршилт амжилттай дууссанаа зарлав. Фридел энэ тухай Шинжлэх ухааны академид шуурхай мэдээлэв. Энэ зорилгоор тодорхой өдөр хуралдсан Моиссаны бүтээлүүдтэй танилцах тусгай комисс байгуулагдсан. Моиссан туршилтаа эхлүүлсэн боловч түүний их харамссанаар туршилт бүтэлгүйтсэн: фторыг олж аваагүй.
Комисс явахад Мойсан болон түүний туслах ажлынхаа бүх явцыг сайтар судалж, туршилт амжилтгүй болсон шалтгааныг хайж эхлэв. Үүний үр дүнд тэд энэ шалтгаан нь хачирхалтай мэт санагдаж байсан ч аяга таваг хэтэрхий цэвэрхэн угаасан гэсэн дүгнэлтэд хүрчээ. Тийм ч учраас фторын калийн ул мөр үлдсэнгүй. Моиссанд төхөөрөмж дэх шингэн устөрөгчийн фторид дээр бага зэрэг калийн фтор нэмж, цахилгаан гүйдэл дамжуулахад хангалттай байсан бөгөөд тэр даруй чөлөөт фторыг олж авсан.
Маргааш нь Моиссан өөрийн нээлтийн бодит байдалд хороог итгүүлэхийн тулд хангалттай хэмжээний хий авчээ. Мойсан Фремигийн багш түүнд халуун баяр хүргээд: "Багш хүн шавь нараа өөрөөсөө илүү ахиж, ахиж байгааг харахдаа үргэлж баяртай байдаг" гэж хэлэв.
1925 онд фтор үйлдвэрлэх илүү хялбар аргыг санал болгосон. Энд байгаа электролит нь калийн бифторид юм. Энэ тохиолдолд электролиз хийх сав нь зэс эсвэл никель, электродууд нь янз бүрийн металлаар хийгдсэн байдаг: катод нь зэс, анод нь никель юм. Бага зэрэг өөрчлөгдсөн хэлбэрээр энэ аргыг өнөөг хүртэл ашиглаж байна.
Фтор зэрэг химийн элемент нь ихэвчлэн шүдний оо, тэр ч байтугай зарим ундаанд нэмэлт бодис болдог. Үйлдвэрлэгчдийн үзэж байгаагаар бүтээгдэхүүнд энэ бүрэлдэхүүн хэсэг байгаа нь цооролтоос найдвартай хамгаалалт болдог. Гэсэн хэдий ч, хэрэв та статистикийг харвал хүмүүс цоорох өвчнөөр бага өвддөггүй гэдгийг тэмдэглэж болно. Энэ нь фтор гэж юу болохыг олж мэдэх санааг төрүүлсэн.
Фторын тухай 10 баримт нь энэхүү химийн элементийн талаар олон шинэ, сонирхолтой зүйлийг сурахад тусална.
1. Дэлхийн ихэнх соёл иргэншсэн орнууд ундны усаа цэвэрлэхдээ фтор хэрэглэдэггүй. Америкчууд фторжуулсан усны дийлэнх хувийг хэрэглэдэг. Тэд бусад бүх орноос илүү их уудаг. Хэрэв бид Баруун Европын тухай ярих юм бол тэнд байгаа ундааны 97% нь энэ бодисыг нэмэлгүйгээр үйлдвэрлэдэг.
Эрдэмтэд амьтан, хүн дээр 100 гаруй судалгаа хийсний үр дүнд фтор нь тархинд нөхөж баршгүй гэмтэл учруулж, бага насны хүүхдийн IQ буурахад нөлөөлдөг болохыг нотолсон. Үүнээс гадна фторын хордлого нь бие махбодид дараах эмгэг өөрчлөлтүүдийг үүсгэдэг болохыг судалгаагаар тогтоожээ.
- хар тугалгын шингээлт нэмэгдсэн;
- нойрмоглох эсвэл хэт идэвхжил;
- коллагены нийлэгжилтийг тасалдуулах;
- булчингийн эмгэг;
- артрит үүсэх;
- бамбай булчирхайн үйл ажиллагааны доголдол (таргалалт орно);
- ясны хугарал;
- хөгшрөлтийн хөгжил;
- ясны хорт хавдрын илрэл;
- одоо байгаа хавдрын хавдрын явц;
- үйл ажиллагааг дарангуйлах;
- эсрэгбие үүсэхийг дарах;
- генетикийн гэмтэл, эсийн үхэл;
- дархлааны тогтолцооны үйл ажиллагааг тасалдуулах;
- эр бэлгийн эсийн гэмтэл, үргүйдлийн аюул.
4. Усан хангамжийн олон системд фторжуулах процесс явагддаг нь үнэхээр зүйн хэрэг юм. Энэ элемент нь ариутгагч бодисоор сайн ажилладаг тул зарим процесст үүнийг ашиглахгүйгээр хийх боломжгүй юм. Гэсэн хэдий ч байгальд фторжуулсан ус байдаггүй тул фтороор боловсруулсан усыг хоол хүнс болгон хэрэглэх эсэх нь эргэлзээтэй байдаг.
5. АНУ-ын өсвөр насныхны 40 гаруй хувь нь флюороз гэх мэт аймшигт өвчний шинж тэмдэгтэй байдаг. Бие махбодид фторыг удаан хугацаагаар хуримтлуулж, түүнээс бие даан гадагшлуулдаггүй үед үүсдэг. Энэхүү архаг эмгэгийн үед фторын давс нь ясанд хуримтлагддаг бөгөөд энэ нь эхлээд шүдний паалан дээр хөх-хөх толбо хэлбэрээр илэрдэг бөгөөд дараа нь ясны эдийн бүтцэд өөрчлөлт орж, ясны хэв гажилт үүсдэг. Учир нь АНУ-ын хүүхдүүд ундны ус, шүдний оо, боловсруулсан хоол, тэр ч байтугай зарим фтор агуулсан эм агуулсан наалддаггүй хайруулын таваг зэрэг хэд хэдэн эх үүсвэрээс фторыг авдаг.
Хүүхдийнхээ шүдэнд толбо байгааг анзаарсан бол үүнийг зүгээр л "гоо сайхны асуудал" гэж бодож болохгүй. Хэрэв та цаг тухайд нь анхаарал хандуулахгүй, энэ элементийн биед орохыг зогсоохгүй бол үр дагавар нь хамгийн аймшигтай байж болно.
6. Фторжуулсан ус нь нялх хүүхдэд ямар ч ашиггүй боловч эрүүл мэндэд ихээхэн аюул учруулдаг. Үнэн хэрэгтээ фтор нь бага насны хүүхдийн тархины үйл ажиллагаанд ноцтой нөлөөлдөг бөгөөд энэ нь IQ буурсантай холбоотой юм. Эрүүл мэндийн үндэсний хүрээлэнгийн хийсэн судалгаагаар фторжуулсан устай газар амьдардаг хүүхдүүд фторжуулсан бүтээгдэхүүн хэрэглэдэггүй орчинд өссөн хүүхдүүдээс оюуны чадамж муутай байдаг.
7. Фторын биед үзүүлэх сөрөг нөлөө нь гуравдагч ертөнцийн орнуудад амьдардаг, ялангуяа амьдралын нөхцөл нь тааламжгүй гэж нэрлэгдэх хүмүүсийн дунд ихээхэн нэмэгддэг. Бие дэх фторын хоруу чанар нь дараах тохиолдолд нэмэгддэг.
- шим тэжээлийн дутагдал;
- бөөрний өвчин;
- Чихрийн шижин
Та энэ нийтлэлээс химийн элементүүдийн нээлтийн талаархи сонирхолтой баримтуудыг олж мэдэх болно.
Химийн элементүүдийн нээлтийн талаархи сонирхолтой баримтууд
Байгальд мэдэгдэж байгаа химийн элементүүдийн ихэнхийг Швед, Англи, Франц, Германы эрдэмтэд нээсэн.
Химийн элементийн "анчдын" дунд рекорд эзэмшигч нь Шведийн химич К.Шээле гэж тооцогддог - тэрээр фтор, хлор, манган, молибден, бари, вольфрам гэсэн 6 химийн элемент байдгийг нээж, нотолсон.
Энэхүү эрдэмтний химийн элементүүдийг нээсэн ололт амжилтын хажуугаар долоо дахь элемент болох хүчилтөрөгчийг нэмж болох боловч тэрээр английн эрдэмтэн Ж.Престлитэй албан ёсоор нээлтийнхээ нэр хүндийг хуваалцаж байна.
Шинэ элементүүдийн нээлтийн хоёрдугаар байр нь Английн эсвэл бүр нарийн яривал Шотландын эрдэмтэн В.Рамсейд харьяалагддаг: тэрээр аргон, гели, криптон, неон, ксеноныг нээсэн.
1985 онд Америк, Английн хэсэг судлаачид молекулын нэгдлүүдийг нээсэн нүүрстөрөгч, энэ нь хөл бөмбөгийн бөмбөгтэй маш төстэй хэлбэртэй. Тэд нээлтээ түүний нэрээр нэрлэхийг хүссэн боловч эрдэмтэд хөл бөмбөг эсвэл хөл бөмбөг (АНУ-ын хөлбөмбөгийн нэр томъёо) гэж аль нэр томъёог ашиглах талаар санал нийлээгүй байна. Үүний үр дүнд тетраэдрээс бүрдсэн геодезийн бөмбөгөр зохион бүтээсэн архитектор Фуллерийн нэрэмжит уг цогцолборыг фуллерен гэж нэрлэжээ.
Францын химич, эм зүйч, эмч Николас Лемери (1645-1715) нэгэн цагт төмрийн аяганд 2 гр төмрийн үртэс, 2 гр нунтаг хүхэр холиод халуун шилэн саваагаар шүргэхдээ галт уултай төстэй зүйлийг ажиглажээ. Хэсэг хугацааны дараа бэлтгэсэн хольцоос хар тоосонцор нисч эхэлсэн бөгөөд хольц нь өөрөө их хэмжээгээр нэмэгдэж, маш халуун болж, гэрэлтэж эхлэв. Фторжуулсан бодисоос фторын хийг ялгах нь туршилтын хамгийн хэцүү асуудлуудын нэг болжээ. Фтор нь онцгой урвалд ордог; ихэвчлэн бусад бодисуудтай харилцан үйлчлэл нь гал асаах, дэлбэрэлт үүсдэг.
Иодыг 1811 онд Францын химич Б.Куртуа нээжээ.Иодын нээлтийн ийм хувилбар байдаг. Үүний дагуу Куртуагийн нээлтийн буруутан нь түүний хайртай муур байсан: тэрээр лабораторид ажиллаж байхдаа химичийн мөрөн дээр хэвтэж байжээ. Хөгжилтэй байхыг хүссэн муур ширээн дээр үсэрч, ойролцоо байсан савыг шалан дээр түлхэв. Тэдний нэг нь далайн байцааны үнсний спиртийн уусмал, нөгөө нь хүхрийн хүчил агуулсан байв. Шингэнүүдийг хольсны дараа иодоос өөр зүйлгүй хөх ягаан өнгийн уурын үүл гарч ирэв.
1898 онд Мари, Пьер Кюри нар хоёр шинэ цацраг идэвхт элемент нээсэн тухай зарлав. радий ба полони. Гэвч тэд шийдвэрлэх нотлох баримт өгөхийн тулд эдгээр элементүүдийн аль нэгийг нь тусгаарлаж чадаагүй. Хосууд шаргуу ажиллаж эхэлсэн: ураны хүдрээс шинэ элементүүдийг гаргаж авах шаардлагатай байв. Тэдэнд 4 жил зарцуулсан. Тухайн үед цацраг идэвхт туяа хүний биед ямар хор хөнөөлтэй болохыг хараахан мэдээгүй байсан бөгөөд тонн цацраг идэвхт хүдэр боловсруулах шаардлагатай болсон. 1902 онд тэд амжилтанд хүрсэн хэд хэдэн тонн хүдрээс радийн хлоридын аравны нэгийг тусгаарлах, мөн 1903 онд Мария Сорбоннад "Цацраг идэвхт бодисын судалгаа" сэдвээр докторын зэрэг хамгаалсан. 1903 оны 12-р сард Беккерел ба Кюри нар Нобелийн шагнал хүртэв.
Бромыг илрүүлэх
Францын химич Антуан Жером Балард лабораторийн туслах байхдаа бромды нээсэн. Давс намаг давсны уусмалд натрийн бромид агуулагддаг. Туршилтын үеэр Балар давсны уусмалд хадгалсан уусмалыг хлорт үзүүлэв. Харилцааны урвалын үр дүнд уусмал шар өнгөтэй болсон. Хэсэг хугацааны дараа Балар хар хүрэн шингэнийг ялгаж аваад мурид гэж нэрлэжээ. Хожим нь Гей-Луссак шинэ бодисыг бром гэж нэрлэжээ. 1844 онд Балард Парисын Шинжлэх Ухааны Академийн гишүүн болжээ. Бромыг нээхээс өмнө Баларыг шинжлэх ухааны хүрээлэлд бараг мэддэггүй байв. Бромыг нээсний дараа Балард Францын коллежийн химийн тэнхимийн эрхлэгч болжээ. Францын химич Чарльз Жерар хэлэхдээ: "Бромыг нээсэн нь Балард биш, харин Бром Балардыг нээсэн!"
Хлорын нээлт
Хлорыг тухайн үед зүгээр л эм зүйч байсан хүн нээсэн нь сонирхолтой юм. Энэ хүнийг Карл Вильгельм Шееле гэдэг. Тэр гайхалтай зөн совинтой байсан. Францын алдарт органик химич Шееле ямар нэгэн зүйлд хүрэх бүртээ нээлт хийдэг гэж хэлсэн байдаг. Scheele-ийн туршилт маш энгийн байсан. Тэрээр хар магнези болон мурик хүчлийн уусмалыг тусгай реторт аппаратаар хольсон. Ретортын хүзүүнд агааргүй бөмбөлөг нааж, халаасан. Удалгүй хөөс дотор хурц үнэртэй шар ногоон хий гарч ирэв. Ингэж хлорыг нээсэн юм.
MnO2 + 4HCl = Cl2 + MnCl2 + 2H2O
Хлорыг нээснийхээ төлөө Шееле нь Стокгольмын Шинжлэх Ухааны Академийн гишүүн цолоор шагнагджээ, гэхдээ өмнө нь тэр эрдэмтэн байгаагүй. Тэр үед Шееле дөнгөж 32 настай байжээ. Гэхдээ хлор нь зөвхөн 1812 онд л нэрээ авсан. Энэ нэрийн зохиогч нь Францын химич Гэй-Люссак юм.
Дэлхийн царцдас дахь хамгийн түгээмэл металл бөгөөд түүний нөөц асар их боловч хөнгөн цагааны үйлдвэрлэл зөвхөн өнгөрсөн зууны сүүлчээр хөгжиж эхэлсэн. Хөнгөн цагааны хүчилтөрөгчийн нэгдлүүд нь маш хүчтэй бөгөөд тэдгээрийг нүүрсээр багасгахад цэвэр металл гарахгүй. Электролизийн аргаар хөнгөн цагаан үйлдвэрлэхийн тулд түүний галоген нэгдлүүд, юуны түрүүнд хөнгөн цагаан, фтор агуулсан криолит шаардлагатай. Гэхдээ байгальд криолит бага байдаг бөгөөд үүнээс гадна "далавчтай металл" -ын агууламж бага байдаг - ердөө 13%. Энэ нь бокситоос бараг гурав дахин бага юм. Бокситыг дахин боловсруулах нь хэцүү боловч аз болоход энэ нь криолитэд уусдаг. Энэ нь бага хайлдаг, хөнгөн цагаанаар баялаг хайлмал үүсгэдэг. Түүний электролиз нь хөнгөн цагаан үйлдвэрлэх цорын ганц үйлдвэрлэлийн арга юм. Байгалийн криолитийн дутагдлыг устөрөгчийн фторыг ашиглан асар их хэмжээгээр үйлдвэрлэдэг хиймэл криолитоор нөхдөг.
Органофлуорины тухай хэдэн үг
Манай зууны 30-аад онд фторын нүүрстөрөгчтэй анхны нэгдлүүдийг нэгтгэсэн. Байгальд ийм бодисууд маш ховор байдаг бөгөөд тэдэнд онцгой давуу тал ажиглагдаагүй байна.
Гэсэн хэдий ч орчин үеийн технологийн олон салбар хөгжиж, шинэ материалын хэрэгцээ нь өнөөдөр фтор агуулсан олон мянган органик нэгдлүүд байдаг. Хөргөлтийн тоног төхөөрөмжийн хамгийн чухал материал болох фреонууд болон хуванцар цагаан алт гэж нэрлэгддэг фторопластик-4-ийг эргэн санахад хангалттай.
Фторын тухай
- ТАРХАЛТ. Энгийн хөрсөн дэх фторын дундаж агууламж 0.02% байна. Далайн усны литр тутамд 0.3 мг фтор агуулагддаг. Хясааны хясаанд үүнээс 20 дахин их байдаг. Шүрэн хад хэдэн сая тонн фтор агуулдаг. Амьд организм дахь фторын дундаж агууламж дэлхийн царцдастай харьцуулахад 200 дахин бага байдаг.
- ФЛОРИД ЯМАР БАЙДАГ ВЭ? Хэвийн нөхцөлд фтор нь цайвар шар өнгөтэй хий, -188 ° C-ийн температурт энэ нь канарын шаргал өнгөтэй шингэн бөгөөд -228 ° C-д фтор нь хөлдөж, цайвар шар талст болж хувирдаг. Хэрэв температурыг -252 ° C хүртэл бууруулвал эдгээр талстууд өнгө нь өөрчлөгдөнө.
- ФЛОРИД ЮУ ҮНЭРТЭЙ ВЭ? Таны мэдэж байгаагаар хлор, бром, иодын үнэрийг тааламжтай гэж ангилахад хэцүү байдаг. Энэ утгаараа фтор нь бусад галогенээс бага зэрэг ялгаатай. Хурц бөгөөд цочромтгой үнэр нь хлор, озоны үнэрийг хоёуланг нь санагдуулдаг. Агаар дахь фторын нэг саяны нэг нь хүний хамар байгаа эсэхийг илрүүлэхэд хангалттай.
- МЯНГАН УТААНЫ ХӨНДИЙД. Галт уулын гаралтай хий нь заримдаа фтор устөрөгч агуулдаг. Ийм хийн хамгийн алдартай байгалийн эх үүсвэр бол Мянган утааны хөндийн (Аляска) фумаролууд юм. Жил бүр 200 орчим мянган тонн фтор устөрөгчийг галт уулын утаатай хамт агаар мандалд хүргэдэг.
- ДЭВИ ГЭРЧИЛЖ БАЙНА. "Цэвэр фторын хүчлийн электролизийн туршилтыг би маш их сонирхон хийсэн, учир нь энэ нь фторын жинхэнэ мөн чанарыг шалгах хамгийн боломжит боломжийг олгосон юм. Гэвч үйл явцыг явуулахад ихээхэн бэрхшээл тулгарсан. Шингэн гидрофторын хүчил нь шил болон бүх амьтан, ургамлын материалыг тэр дор нь устгасан. Энэ нь металлын исэл агуулсан бүх биед үйлчилдэг. Зарим металл, нүүрс, фосфор, хүхэр, зарим хлорын нэгдлүүдийг эс тооцвол түүнд уусдаггүй нэг ч бодисыг би мэдэхгүй."
- ФЛОРИН БА АТОМЫН ЭРЧИМ ХҮЧ. Цөмийн түлш үйлдвэрлэхэд фтор ба түүний нэгдлүүдийн үүрэг онцгой юм. Фторгүй бол дэлхий дээр нэг ч атомын цахилгаан станц байхгүй, судалгааны реакторуудын нийт тоог нэг талаас тоолоход хэцүү биш гэж бид баттай хэлж чадна.
Бүх уран нь цөмийн түлш болж чаддаггүй, зөвхөн түүний зарим изотопууд, ялангуяа 235 U.
Зөвхөн цөм дэх нейтроны тоогоор бие биенээсээ ялгаатай изотопуудыг салгах нь тийм ч хялбар биш бөгөөд элемент нь хүнд байх тусам жингийн ялгаа бага мэдрэгддэг. Ураны изотопуудыг салгах нь орчин үеийн бараг бүх салгах аргуудыг хийн бодис эсвэл дэгдэмхий шингэнд зориулагдсан байдаг тул илүү төвөгтэй байдаг.
Уран 3500 градусын температурт буцалгана. Хэрэв бид ураны ууртай ажиллах шаардлагатай бол изотопыг ялгах багана, центрифуг, диафрагм хийхэд ямар материал ашиглах ёстой байсан бэ?! Ураны онцгой дэгдэмхий нэгдэл бол түүний гексафторид UF 6 юм. Энэ нь 56.2 хэмд буцалгана.
Иймээс ураны металл биш, уран-235, уран-238 гексафторидуудыг ялгаж авдаг. Мэдээжийн хэрэг, эдгээр бодисууд нь химийн шинж чанараараа бие биенээсээ ялгаатай биш юм. Тэдгээрийг салгах үйл явц нь хурдан эргэдэг центрифугуудад явагддаг.
Төвөөс зугтах хүчээр хурдасгасан ураны гексафторидын молекулууд нарийн сүвэрхэг хуваалтаар дамждаг: 235 U агуулсан "хөнгөн" молекулууд "хүнд" молекулуудаас арай хурдан дамждаг.
Салсны дараа уран гексафторидыг UF 4 тетрафторид болгон хувиргаж, дараа нь уран металл болгон хувиргадаг.
Ураны гексафторидыг ураны элемент фтортой урвалд оруулснаар олж авдаг боловч энэ урвалыг хянахад хэцүү байдаг. Ураныг фторын нэгдлүүдийг ClF 3, BrF, BrF 6 гэх мэт бусад галогентэй хамт боловсруулах нь илүү тохиромжтой. Уран тетрафлорид UF 4-ийн үйлдвэрлэл нь устөрөгчийн фторыг ашиглах явдал юм. 60-аад оны дундуур АНУ-д фтор устөрөгчийн бараг 10 хувийг ураны үйлдвэрлэлд зарцуулсан нь 20 орчим мянган тонн байв.
Торий, бериллий, циркони зэрэг цөмийн технологийн чухал материалыг үйлдвэрлэх процесст эдгээр элементүүдийн фторын нэгдлүүдийг олж авах үе шатууд орно.
- Хуванцар платинум. Арслан хааныг залгиж байна. Энэхүү тэмдэг нь алхимичдын дунд азотын болон давсны хүчлийн холимог дахь алтыг уусгах үйл явцыг илэрхийлдэг байв. Бүх үнэт металлууд химийн хувьд маш тогтвортой байдаг. Алт нь хүчил (селен ба селенидээс бусад) эсвэл шүлтлэгт уусдаггүй. Зөвхөн aqua regia л алт, тэр ч байтугай цагаан алтыг хоёуланг нь "залгидаг".
30-аад оны сүүлээр химичүүдийн арсенал дээр "арслан" хүртэл хүчгүй байсан бодис гарч ирэв. Aqua regia нь хуванцар, фторопластик-4, мөн Teflon гэж нэрлэгддэг хуванцард хэтэрхий хатуу байсан. Teflon молекулууд нь полиэтилен молекулуудаас ялгаатай нь үндсэн гинжийг тойрсон бүх устөрөгчийн атомууд (... -C- C-C- ...) фтороор солигддог.
Фторопласт-4 нь өнгөгүй, хоргүй хий болох тетрафторэтиленийг полимержих замаар үйлдвэрлэдэг.
Тетрафторэтиленийн полимержилтийг санамсаргүйгээр илрүүлсэн. 1938 онд энэ хийн цилиндрээс нийлүүлэх нь гадаадын лабораторийн нэгэнд гэнэт зогссон. Цилиндрийг онгойлгоход үл мэдэгдэх цагаан нунтагаар дүүргэсэн нь политетрафторэтилен болох нь тогтоогджээ. Шинэ полимерийг судлах нь түүний гайхалтай химийн эсэргүүцэл, өндөр цахилгаан тусгаарлагч шинж чанарыг харуулсан. Одоо энэ полимерээс онгоц, машин, машин хэрэгслийн олон чухал эд ангиудыг шахдаг.
Фтор агуулсан бусад полимерууд бас өргөн хэрэглэгддэг. Эдгээр нь политрифторохлорэтилен (фторопластик-3), поливинил фтор, поливинилиден фтор юм. Хэрэв анхандаа фтор агуулсан полимерууд зөвхөн бусад хуванцар болон өнгөт металлыг орлуулж байсан бол одоо тэд өөрсдөө орлуулшгүй материал болжээ.
Фтор агуулсан хуванцаруудын хамгийн үнэ цэнэтэй шинж чанарууд нь химийн болон дулааны тогтвортой байдал, хувийн жин бага, чийг нэвчих чадвар, цахилгаан тусгаарлагчийн сайн шинж чанар, маш бага температурт ч хэврэг чанаргүй байдаг. Эдгээр шинж чанарууд нь фторопластикийг хими, нисэх онгоц, цахилгаан, цөмийн, хөргөх, хүнс, эмийн үйлдвэр, түүнчлэн анагаах ухаанд өргөнөөр ашиглахад хүргэсэн.
Фтор агуулсан резин нь маш ирээдүйтэй материал гэж тооцогддог. Молекулууд нь фтор агуулсан хэд хэдэн төрлийн резинтэй төстэй материалыг янз бүрийн улс оронд аль хэдийн бүтээжээ. Үнэн бол тэдгээрийн аль нь ч нийт шинж чанарын хувьд фторопластик-4 нь ердийн хуванцараас давж гардаг шиг бусад каучукаас дээгүүр байдаггүй, гэхдээ тэдгээр нь олон үнэ цэнэтэй шинж чанартай байдаг. Ялангуяа тэдгээр нь азотын хүчлээр утаагаар устдаггүй бөгөөд өргөн температурт уян хатан чанараа алддаггүй.
ФЛОРИДЫН ТЕХНОЛОГИЙН ТУХАЙ ДЭЛГЭРЭНГҮЙ. ЗХУ-ын Шинжлэх Ухааны Академийн Физик Химийн Хүрээлэнгийн ажилтнууд вольфрам үйлдвэрлэх шинэ аргыг боловсруулж, хэрэгжүүлэв. WF 2 дифторидоос вольфрамыг устөрөгчөөр багасгаснаар тэд нунтаг металлургийн аргаар гаргаж авсан вольфрамаас чанарын хувьд давуу металл олж авсан.
Хүүхэд шүдээ хавирах үед эцэг эхчүүд санаа зовж эхэлдэг: нялх хүүхдэд фтор хангалттай байдаг уу? Таны бяцхан үрс энэ микроэлементийг хэр их хэмжээгээр хүлээн авдаг талаар дор хаяж ойролцоогоор төсөөлөлтэй байхын тулд фторын талаар мэдэх хэрэгтэй.
Фторын дутагдлын шинж тэмдэг.
- цоорох өвчин.
- Шүдний шүдний өвчин.
Илүүдэл фторын шинж тэмдэг.
Фторыг хэтрүүлэн хэрэглэснээр флюороз үүсч болно - шүдний паалан дээр саарал толбо гарч ирдэг, үе мөч нь гажигтай, ясны эд устаж үгүй болдог өвчин юм.
Хүнсний фторын агууламжид нөлөөлөх хүчин зүйлс Хөнгөн цагаан нь хоолноос фторыг уусгадаг тул хөнгөн цагаан саванд хоол хийх нь хүнсний фторын агууламжийг эрс бууруулдаг.
Фторын дутагдал яагаад үүсдэг вэ?
Хүнсний бүтээгдэхүүн дэх фторын агууламж нь түүний хөрс, усанд агуулагдах агууламжаас хамаардаг.
Хүүхдийн хоол боловсруулах системд орж буй фтор нь цусны эргэлтийн системээр дамжин шүд рүү дамждаг. Тэнд энэ нь пааланг дотроос нь бэхжүүлж, цоорох өвчнөөс урьдчилан сэргийлэхэд тусалдаг. Шүдэнд гаднаас нь түрхдэг фтор нь шүдний оо доторх эсвэл шүдний эмчийн шүдэнд түрхсэн бодисоос үл хамааран шүдэнд үүссэн шинэ пааланг бэхжүүлэхэд тусалдаг. Үүнийг байгалийн нөхөн сэргээлт гэж нэрлэдэг.
Хүүхдийн байнгын шүдийг хөгжүүлэх, бэхжүүлэх ажил одоо ч эхэлж байна. Умайн дотор! Шүд нь бохьтой хэвээр байх үед. Хүүхдийн биед орж буй фтор шууд шүдэнд ордог.
Сонирхолтой нь, усанд фторын агууламж хангалттай байдаг газар амьдардаг хүмүүсийн шүд цоорох өвчин 50% бага байдаг.
Бэлэн худалдаалагдаж байгаа хүүхдийн сүүн тэжээлийг фтор агуулаагүй усаар хийдэг.
Фтор нь бусад витамин, эрдэс бодисуудаас ялгаатай нь ашиг тусаас хортой болж хувирдаг. Өөрөөр хэлбэл, дунд зэргийн хэмжээ нь шүдэнд сайн, харин хэтрүүлэн хэрэглэх нь хор хөнөөлтэй байдаг. Шүд нь сүйрч эхэлдэг - энэ өвчнийг флюороз гэж нэрлэдэг. Тиймээс хэрэв таны хүүхдэд фтор агуулсан эм бичиж өгсөн бол та өөрөө тунг нэмэгдүүлж болохгүй.
Шүдний оо, ам зайлагчийг залгихыг хатуу хориглоно гэдгийг хүүхэддээ мэдэгдээрэй. Тэд фторын өндөр агууламжтай байдаг. Шүдний сойз дээрээ вандуйны хэмжээтэй бага хэмжээний оо шахаж ав. Дашрамд хэлэхэд энэ нь хүүхдийн шүдний ооны багц дээр бичигдсэн байдаг. Харин хүүхдэд “Насанд хүрэгчид” шүдний оо хэрэглэх шаардлагагүй.
Тиймээс хүүхэд фтор агуулсан эм хэрэглэж байгаа бол фторгүй шүдний оо сонгох хэрэгтэй.
Хүүхдийн ууж буй усан дахь фторын агууламж, өөрөөр хэлбэл шөл, компот бэлтгэхэд ашигладаг усанд анхаарлаа хандуулаарай. Хэрэв энэ нь сая тутамд 0.3-аас доошгүй хэсэг (өөрөөр хэлбэл литр тутамд 0.3 мл) агуулдаг бол хүүхдэд фторын бэлдмэл хэрэглэх шаардлагагүй.
Хэрэв та хүүхэд тань хангалттай хэмжээний фторид авч чадахгүй байна гэж санаа зовсон хэвээр байгаа бол олон бүтээгдэхүүнд фтор агуулагдаж, их хэмжээгээр агуулагддаг гэдгийг санаарай.
Фтор агуулсан хоол хүнс.
Хоолны тусламжтайгаар та бие дэх фторын тэнцвэрийг барьж чадна. Хэрэв усанд энэ бүрэлдэхүүн хэсэг хангалтгүй байвал фтор агуулсан бүтээгдэхүүнээс хоолны дэглэмээ зөв тохируулах хэрэгтэй.
Далайн хоол.
Эдгээр нь фтор зэрэг олон тооны микроэлементүүдийг агуулдаг. Сам хорхой, хавч, загас, түүний түрс, түүнчлэн далайн ургамал идэх талаар бодох нь зүйтэй.
Хар ба ногоон цай.
Хүнсний ногоо, жимс жимсгэнэ. Төмс, алим, бэрсүүт жүрж нь фтороор баялаг юм.
Үр тариа: Oatmeal, будаа, Сагаган. Бусад үр тариа нь бага хэмжээний фтор агуулдаг.
Хөхөөр хооллож буй хүүхдэд фтор агуулсан эм хэрэглэх шаардлагатай талаар эмч нар зөвшилцөлд хүрээгүй байна. Зарим нь эхийн сүүнд агуулагдах фтор хангалттай гэж маргадаг бол зарим нь тэнд маш бага ул мөр элемент байдаг гэж маргадаг. Гэхдээ нэг зүйл тодорхой байна: хөхний сүүнд агуулагдах фторын агууламж өөрчлөгдөөгүй хэвээр байгаа бөгөөд эхийн хоолны дэглэмийн өөрчлөлтөд ямар ч байдлаар нөлөөлдөггүй. Эрүүл өсөх!
Үелэх системийн хамгийн идэвхтэй элемент бол фтор юм. Фтор нь тэсрэх шинж чанартай ч хүн амьтанд амин чухал элемент бөгөөд ундны ус, шүдний оо зэрэгт агуулагддаг.
Зүгээр л баримт
- Атомын дугаар (цөм дэх протоны тоо) 9
- Атомын тэмдэг (элементүүдийн үечилсэн системд) Ф
- Атомын жин (атомын дундаж масс) 18.998
- Нягт 0.001696 г/см3
- Өрөөний температурт - хий
- Хайлах цэг нь хасах 363.32 градус Фаренгейт (- 219.62 ° C)
- Буцлах цэг хасах 306.62 хэм (- 188.12 ° C)
- Изотопын тоо (өөр өөр тооны нейтронтой ижил элементийн атомууд) 18
- Хамгийн элбэг F-19 изотопууд (100% байгалийн элбэг дэлбэг)

Флюорит болор
Химичид олон жилийн турш фторын элементийг янз бүрийн фтороос ангижруулахыг хичээж ирсэн. Гэсэн хэдий ч фтор нь байгальд чөлөөтэй байдаггүй: ямар ч химийн бодис нь реактив шинж чанартай тул фторыг нэгдлүүдээс нь чөлөөлөх чадваргүй байдаг.
Ашигт малтмалын хайлуур жоншийг олон зууны турш металл боловсруулахад ашиглаж ирсэн. Кальцийн хайлуур жоншийг (CaF 2) хүдэр дэх хэрэгцээгүй эрдсээс цэвэр металлыг ялгахад ашигласан. "Fluer" (Латин "fluere" гэсэн үг) нь "урсгах" гэсэн утгатай: жоншны шингэний шинж чанар нь метал хийх боломжийг олгосон. Шилэн сийлбэр хийхэд ашигт малтмалыг чехийн маргад гэж нэрлэдэг байв.
Олон жилийн турш фторын давс эсвэл фторыг гагнах, шиллэгээ хийхэд ашигладаг байсан. Жишээлбэл, гэрлийн чийдэнгийн шилийг сийлэхэд фторын хүчил ашигласан.
Эрдэмтэд жонштой туршилт хийж, түүний шинж чанар, найрлагыг олон арван жилийн турш судалжээ. Химичид ихэвчлэн фторын хүчил (фторын хүчил, HF) үйлдвэрлэдэг байсан бөгөөд энэ нь гайхалтай идэвхтэй, аюултай хүчил юм. Энэ хүчил арьсан дээр бага зэрэг цацагдах нь үхэлд хүргэж болзошгүй юм. Туршилтын үеэр олон эрдэмтэд гэмтэж, сохорч, хордож, нас барсан.
- 19-р зууны эхээр Францын Андре-Мари Ампер, Английн Хамфри Дэви нар 1813 онд шинэ элемент нээснээ зарлаж, Амперын санал болгосны дагуу фтор гэж нэрлэжээ.
- Францын химич Анри Мойсан эцэст нь 1886 онд хуурай калийн фтор (KHF 2) ба хуурай фторын хүчлийг электролизээр ялган авч, 1906 онд Нобелийн шагнал хүртжээ.
Одооноос эхлэн фтор нь цөмийн энергийн амин чухал элемент юм. Энэ нь ураны изотопыг ялгахад шаардлагатай уран гексафторидыг үйлдвэрлэхэд хэрэглэгддэг. Хүхрийн гексафторид нь өндөр чадлын трансформаторыг тусгаарлахад ашигладаг хий юм.
Хлорфтор нүүрстөрөгчийг (CFCs) нэг удаа аэрозол, хөргөгч, агааржуулагч, хөөсөн бүтээгдэхүүний савлагаа, гал унтраагч зэрэгт ашиглаж байсан. Эдгээр хэрэглээг 1996 оноос хойш хориглосон байдаг, учир нь тэдгээр нь озоны давхаргад нөлөөлдөг. 2009 он хүртэл CFC-ийг астма өвчнийг дарах зорилгоор ингаляторт хэрэглэдэг байсан бол 2013 онд эдгээр төрлийн амьсгалын аппаратыг мөн хориглосон.
Фторыг олон тооны фторжуулсан бодис, түүний дотор уусгагч, өндөр температурт хуванцар, тухайлбал тефлон (поли-тетрафторэтен, PTFE) зэрэгт ашигладаг. Teflon нь наалддаггүй шинж чанараараа алдартай бөгөөд хайруулын тавган дээр хэрэглэдэг. Фторыг мөн кабелийн дулаалга, сантехникийн соронзон хальс, ус нэвтэрдэггүй гутал, хувцасны суурь болгон ашигладаг.
Жефферсоны лабораторийн мэдээлснээр шүд цоорохоос сэргийлэхийн тулд фторыг хотын усан хангамжид сая тутамд нэг хувь хэмжээгээр нэмдэг. Шүд цоорохоос сэргийлж шүдний оонд хэд хэдэн фторын нэгдлүүдийг нэмдэг.
Хэдийгээр бүх хүн, амьтад фторын хордлого, хэрэгцээтэй байдаг ч фторын элемент нь хангалттай их тунгаар хэрэглэхэд маш хортой бөгөөд аюултай байдаг. Фтор нь байгалийн жамаар ус, агаар, ургамал, амьтны эдэд бага хэмжээгээр ялгарч болно. Цай, хясаа зэрэг зарим хоолонд их хэмжээний фтор агуулагддаг.
Фтор нь бидний яс, шүдийг бат бөх байлгахад зайлшгүй шаардлагатай байдаг ч хэт их хэрэглэх нь эсрэгээрээ ясны сийрэгжилт, шүд цоорох өвчнийг үүсгэж, бөөр, мэдрэл, булчинг гэмтээдэг.
Хийн хэлбэрээр фтор нь маш аюултай. Бага хэмжээний фторын хий нь нүд, хамар цочроох шалтгаан болдог ч их хэмжээгээр үхэлд хүргэдэг. Усны фторын хүчил нь арьсанд бага зэрэг хүрсэн ч үхэлд хүргэдэг.
Фтор, дэлхийн царцдасын 13 дахь хамгийн элбэг элемент; энэ нь ихэвчлэн хөрсөнд суурьшиж, элс, хайрга, нүүрс, шавартай амархан нийлдэг. Өндөр концентраци нь ургамлын үхэлд хүргэдэг хэдий ч ургамал хөрсөөс фторыг шингээж чаддаг. Жишээлбэл, эрдэнэ шиш, чангаанз нь фторын өндөр агууламжтай үед хамгийн их гэмтдэг ургамлын нэг юм.

Хэн мэдсэн бэ? Фторын тухай сонирхолтой баримтууд
- Натрийн фторид нь хархны хор юм.
- Фтор бол манай гаригийн хамгийн идэвхтэй элемент юм; хүчилтөрөгч, гели, неон, криптоноос бусад ямар ч элементтэй харьцах үед дэлбэрч болно.
- Фтор нь мөн хамгийн цахилгаан сөрөг элемент юм; энэ нь электронуудыг бусад ямар ч элементээс илүү амархан татдаг.
- Хүний биед агуулагдах фторын дундаж хэмжээ гурван миллиграмм байдаг.
- Фторыг ихэвчлэн Хятад, Монгол, Орос, Мексик, Өмнөд Африкт олборлодог.
- Фтор нь нарны оддын амьдралын төгсгөлд үүсдэг (“Astrophysical Journal in Letters” 2014). Элемент нь одны доторх хамгийн өндөр даралт, температурт үүсдэг бөгөөд энэ нь улаан аварга том болж томордог. Оддын гаднах давхаргууд асгарч, гаригийн мананцар үүсгэх үед фтор нь бусад хийтэй хамт од хоорондын орчинд шилжиж, улмаар шинэ од, гаригуудыг үүсгэдэг.
- Хорт хавдар, төв мэдрэлийн систем, зүрх судасны систем зэрэг эм, эмийн 25 орчим хувь нь фторын зарим хэлбэрийг агуулдаг.
Шүлтлэг металлын янз бүрийн урвал бүхий gif-г нийтлүүлснээр тайлбарт хангалттай тооны хүмүүс Францыг энэ талаар сонирхож байв.
Одоо i-г цэглэхийн тулд... Харамсалтай нь Францтай gif байхгүй. Үүний оронд би түүний тухай шууд ярих болно, тэр үед яагаад gif байхгүй байна.
Франци бол шүлтлэг металлын бүлгийн хамгийн сүүлчийн элемент юм (хэдийгээр таамаглалаар дараагийн шүлтлэг металл (119-р элемент) нь унунениум боловч хараахан олдоогүй байна).
Франциумыг 1870-аад оны үед нээхээс өмнө таамаглаж байсан. Үүний зэрэгцээ, францийг нээх хүртлээ "эка-цезий" гэж нэрлэдэг байв. 20-р зууны эхэн үед аль хэдийн мэдэгдэж байсан шүлтлэг металлын цацраг идэвхт изотопуудыг андуурч байсан тул үүнийг илрүүлэх олон оролдлого амжилтгүй болсон. Гэсэн хэдий ч 1939 онд Парисын Кюри хүрээлэнгийн ажилтан Маргерит Перей тэр үед үл мэдэгдэх элементийг Настуран эрдэст агуулагдах актини-227-ийн альфа задралын бүтээгдэхүүн болохыг анзаарчээ.
Хожим нь 1946 онд уг элементийг нээсэн эх орноо хүндэтгэн "Франциум" гэж нэрлэжээ.

Сонирхолтой баримт бол энэ элемент нь хамгийн цахилгаан эерэг катионтой тул түүнийг кати гэж нэрлэхийг Перей өөрөө санал болгосон боловч катионоос илүү мууртай илүү холбоотой байсан тул саналыг няцааж, тэд францийн сонголт дээр тогтжээ.

Одоогийн байдлаар францийн 34 изотопыг мэддэг. Тэдгээрийн хамгийн тогтвортой нь франций-223 ба франций-221 юм. Франциум-223 нь пичблендээс олддог бөгөөд энэ нь хэд хэдэн актиний задралын бүтээгдэхүүн юм. Үүний зэрэгцээ бета задралын дараах бүтээгдэхүүн нь радий-223 юм. Франци-221 нь актиниум 225-аас үүссэн нептуний задралын цувралын бүтээгдэхүүн бөгөөд өөрөө астатин-217 болж задардаг. Тэдний хагас задралын хугацаа 22 минут (Франц-223) ба 5 минут (Франц-221-ийн хувьд) байдаг тул Перейгийн олсон изотоп нь хамгийн тогтвортой нь юм.
(доорх нь 300к атом бүхий соронзон-оптик урхинд зохиомлоор үйлдвэрлэсэн франций-223-ийн зураг юм)

"Гэхдээ хамгийн тогтвортой изотопын амьдрах хугацаа 22 минут бол байгальд яаж оршин тогтнох вэ?" - Та асуух. Энэ бүхэн цацраг идэвхт ашигт малтмалын тасралтгүй задралын тухай юм. Доорх pitchblende-ийн жишээнд франц хэзээд 3.3 × 10^-20 грамм байна, учир нь "22 минутын өмнө тэнд байсан франций" радий болж хувирсан ба 22 минутын өмнө байсан зарим актиниум франций болж хувирсан тул энэ нь үргэлж ижил хэмжээтэй байдаг.

Дэлхий дээрх ураны ашигт малтмалын агууламж, тэдгээрийн францийн агууламжийг мэдсэнээр та дэлхийн царцдас дахь нийт францийн хэмжээг ямар ч үед тооцоолж болно - энэ нь ойролцоогоор 30 грамм юм. Чухамдаа энэ бол яагаад түүнтэй хамт GIF байхгүй байна вэ гэсэн асуултын хариулт юм.
Хэт ховор боловч энэ металлын зарим шинж чанарууд, тухайлбал изотопуудын дундаж шинж чанарууд нь мэдэгдсээр байна ...
Ерөнхийдөө францийн химийн шинж чанар нь цезийнхтэй төстэй байх болно, зөвхөн тэдгээр нь илүү хүчтэй байх болно. Бүх шүлтлэг металлын нэгэн адил франц нь агаар дахь хүчилтөрөгчтэй урвалд орж исэл ба хэт исэл, устай шүлт үүсгэдэг.
Францийн нягт нь 1.87 г/см³ (литийнхээс 3.5 дахин их, харин хөнгөн цагаанаас 1.4 дахин бага).
Хайлах цэг нь 20С бөгөөд энэ нь орчны нөхцөлд гурав дахь шингэн болно. мөнгөн ус, бромоос бусад элемент (галли ба цезий нь 28 градусын хайлах цэгтэй тул тэдгээрийг стандарт 298К (25С) хатуу гэж үздэг)
Франци нь хамгийн бага цахилгаан сөрөг нөлөөтэй бөгөөд хэрэв үүнийг химийн салбарт ашигласан бол энэ нь хамгийн хүчтэй бууруулагч байх болно.
Сүүлийн жилүүдэд батлагдсан батлагдаагүй, гэхдээ хүчинтэй хэвээр байгаа таамаглал нь онолын хувьд метал франц нь алтан (цезий гэх мэт) -ээс бүрэн улаан өнгөтэй байж болно.
Франци нь 0.54 нм хэмжээтэй атомын хамгийн том хэмжээтэй. Энэ нь ураны атомаас 2 дахин, хүчилтөрөгчийн атомаас 4.5 дахин, устөрөгчийн атомаас 8.5 дахин их юм.
Харамсалтай нь тодорхой шалтгааны улмаас франц нь практик хэрэглээг олж чадаагүй боловч хорт хавдрын эмчилгээнд хэрэглэх төсөл байсан боловч ховор тохиолддог тул төслийг зохисгүй гэж үзсэн.
Иод бол иоджуулсан давс, өдөр тутмын хоол хүнсэнд байдаг химийн элемент юм. Хүний хоол тэжээлд иод бага хэмжээгээр шаардлагатай байдаг.Иодын тухай сонирхолтой баримтуудыг сонгон авах нь хүн бүрт ашигтай байх болно. Зарим хүмүүс иодын бие даасан үл тэвчих шинжтэй байдаг бөгөөд түүний биед илүүдэл нь иодын дутагдалтай бараг ижил үр дагаварт хүргэдэг гэдгийг мартаж болохгүй. Гэртээ иодын эмийн уусмалыг ашиглан та "иодын цаг" гэсэн сонирхолтой урвалыг ажиглаж болно.
 Нэгдүгээрт, иодын тухай есөн баримт. Энэхүү сонирхолтой баримтуудын цуглуулгыг Шинжлэх ухааны доктор Анне Мари Хелменштейн About.com сайтын химийн хэсгийн хуудсан дээр тавьсан материалд үндэслэсэн болно.
Нэгдүгээрт, иодын тухай есөн баримт. Энэхүү сонирхолтой баримтуудын цуглуулгыг Шинжлэх ухааны доктор Анне Мари Хелменштейн About.com сайтын химийн хэсгийн хуудсан дээр тавьсан материалд үндэслэсэн болно.
1. Иод гэдэг нэр нь нил ягаан, нил ягаан гэсэн утгатай грек үгнээс гаралтай. Баримт нь хийн хэлбэрийн иод яг ийм өнгөтэй байдаг.
2. Иодын олон изотопууд мэдэгдэж байна. I-127 изотопоос бусад нь бүгд цацраг идэвхт бодис юм.
3. Хатуу төлөвт иод нь хар өнгөтэй, цэнхэр өнгөтэй, гялалзсан байдаг. Хэвийн температур, даралттай үед иод нь хийн төлөвт шилждэг. Энэ элемент нь шингэн хэлбэрээр олддоггүй.
4. Иод бол галоген, металл бус бодис юм. Үүний зэрэгцээ энэ нь металлын шинж чанартай зарим шинж чанартай байдаг.
5. Бамбай булчирхай нь тироксин, трийодтиронин гормоныг үйлдвэрлэхэд иод хэрэгтэй. Иодын дутагдал нь бамбай булчирхайг хавдахад хүргэдэг. Иодын дутагдал нь оюун ухааны хомсдолын гол шалтгаан гэж тооцогддог. Илүүдэл иодын шинж тэмдэг нь энэ элементийн дутагдалтай үед тохиолддог шинж тэмдгүүдтэй төстэй байдаг. Иод нь селенийн дутагдалтай хүмүүст илүү хортой байдаг.
6. Иод нь I2 химийн томьёотой хоёр атомт молекулуудыг үүсгэдэг.
7. Иодыг анагаах ухаанд идэвхтэй ашигладаг. Зарим хүмүүс иодод химийн мэдрэмтгий байдаг. Арьсанд иодыг түрхэхэд тууралт үүсч болно. Ховор тохиолдолд иодын хэрэглээ нь анафилаксийн (харшлын) шоконд хүргэдэг.
8. Хүний хоол тэжээл дэх иодын байгалийн эх үүсвэр нь иодоор баялаг далайн усанд ургадаг далайн хоол, бор замаг (далайн байцаа) юм. Хоолны давсанд калийн иодыг ихэвчлэн нэмдэг. Олон тогооч нарын мэддэг иоджуулсан давсыг ингэж гаргаж авдаг.
9. Иодын атомын дугаар 53. Энэ нь иодын атом бүр 53 протон агуулдаг гэсэн үг юм.
Британника нэвтэрхий толь бичигт иодыг хүн төрөлхтөн хэрхэн нээсэн тухай өгүүлдэг. 1811 онд Францын химич Бернар Куртуа далайн ургамлын үнсийг хүхрийн хүчилд халаахдаа нил ягаан уурыг олж харжээ. Энэ уур нь өтгөрч, "X бодис" хэмээх хар талст бодис болжээ. 1813 онд Британийн химич Сэр Хамфри Дэви Итали руу явах замдаа Парис хотоор дайран өнгөрөхдөө "Х бодис" нь хлортой төстэй химийн элемент гэж таамаглаж, нил ягаан өнгөөр нь иод (англиар "iodine") гэж нэрлэхийг санал болгов. түүний хийн хэлбэрийн өнгө.
Иод нь байгальд хэзээ ч чөлөөт төлөвт байдаггүй бөгөөд бие даасан ашигт малтмал үүсгэхэд хангалттай хэмжээгээр төвлөрдөггүй. Иод нь далайн усанд агуулагддаг боловч бага хэмжээгээр гидроиод хүчлийн давс (иодид) дахь I- ион хэлбэрээр байдаг. Иодын агууламж нэг метр тонн (1000 кг) далайн усанд ойролцоогоор 50 миллиграмм байдаг. Энэ нь давстай усны оршин суугчид далайн байцаа, далайн хясаа, сагамхай элэгнээс олддог. Хүний бие нь бамбай булчирхайгаар үүсгэгддэг тироксин даавар дахь иодыг агуулдаг.
Иодын цорын ганц байгалийн изотоп бол тогтвортой иод-127 юм. Найман хоногийн хагас задралын хугацаатай цацраг идэвхт иод-131 изотопыг идэвхтэй ашиглаж байна. Анагаах ухаанд бамбай булчирхайн үйл ажиллагааг шалгах, бамбай булчирхай, бамбай булчирхайн хорт хавдрыг эмчлэхэд ашигладаг. Мөн тархи, элэгийг нутагшуулах зориулалттай.
Иодоор баялаг ямар далайн хоолыг та мэдэх вэ? Та далайн хоолыг зөвхөн эрүүл төдийгүй амттай гэж үздэг үү? Суши хийхэд хэрэглэдэг нори далайн замаг хэт их иод агуулдаг тул хүний биед хортой гэж үздэг. Энэ мэдээлэл нь таны одоогийн загварлаг Японы хоолонд хандах хандлагад хэрхэн нөлөөлж байна вэ?
 Хлор нь галоген бүлэгт агуулагддаг хий бөгөөд олон сонирхолтой шинж чанар, хэрэглээтэй байдаг.
Хлор нь галоген бүлэгт агуулагддаг хий бөгөөд олон сонирхолтой шинж чанар, хэрэглээтэй байдаг.
Хлорыг усан сангийн ус цэвэршүүлэх бүтээгдэхүүн болгон ашиглах, цайруулагч гэх мэт өргөн хэрэглээний бүтээгдэхүүнүүдийн талаар илүү ихийг мэдэж аваарай. Илүү олон сонирхолтой хлорын баримтуудыг үргэлжлүүлэн уншаарай.
Хлор химийн элемент нь C1 тэмдэгтэй, атомын дугаар 17.
Тогтмол хүснэгтэд хлор нь галоген бүлэгт багтдаг бөгөөд фторын дараа ордог хамгийн хөнгөн галоген хий юм.
Стандарт хэлбэрээр хлор нь шар-ногоон хий боловч нийтлэг нэгдлүүд нь ихэвчлэн өнгөгүй байдаг. Хлор нь гэр ахуйн цайруулагчтай төстэй хүчтэй, өвөрмөц үнэртэй байдаг.
Хлор гэдэг нэр нь Грекийн хлорос гэдэг үгнээс гаралтай бөгөөд энэ нь ногоон шар гэсэн утгатай.
Хлор нь хайлах цэг нь -150.7 ° F (-101.5 ° C), буцлах цэг нь -29.27 ° F (-34.04 ° C) байна.
Чөлөөт хлор нь дэлхий дээр ховор байдаг. Хлор нь бараг бүх элементүүдтэй нэгдэж хлорид гэж нэрлэгддэг хлорын нэгдлүүдийг үүсгэдэг бөгөөд энэ нь илүү түгээмэл байдаг.
Байгалийн гаралтай 2000 гаруй органик хлорын нэгдлүүд байдаг.
Хамгийн түгээмэл хлорын нэгдэл нь эрт дээр үеэс мэдэгдэж байсан натрийн хлорид бөгөөд үүнийг бид "энгийн давс" гэж илүү сайн мэддэг.
Шведийн химич Карл Вильгельм Шееле 1774 онд хлорыг хүчилтөрөгч агуулсан гэж үзэн нээсэн. 1810 онд Сэр Хамфри Дэви ижил туршилт хийж, хлор нь нэгдэл биш элемент гэсэн дүгнэлтэд хүрчээ.
Хлор нь дэлхийн далай дахь гурав дахь хамгийн элбэг (далайн усны массын 1.9% орчим нь хлоридын ионууд) бөгөөд дэлхийн царцдасын 21 дэх хамгийн элбэг химийн элемент юм.
Хлорын өндөр исэлдүүлэх шинж чанар нь түүнийг 1918 онд АНУ-д ус цэвэршүүлэхэд ашиглаж байсныг харуулж байна. Өнөөдөр дэлхийн ихэнх усан сангуудад хлор болон түүний төрөл бүрийн нэгдлүүдийг цэвэр байлгахын тулд болон ариутгагч бодис, цайруулагч зэрэг ахуйн цэвэрлэгээний олон бүтээгдэхүүнд ашигладаг.
Хлорыг хуванцар, нэхмэлийн цайруулах, эм, хлороформ, шавьж устгах бодис, цаасан бүтээгдэхүүн, уусгагч, будагч бодис, будаг гэх мэт бусад үйлдвэрлэлийн болон өргөн хэрэглээний бүтээгдэхүүнүүдэд ашигладаг.
Өндөр концентрацид хлор нь маш аюултай бөгөөд хортой байдаг. Энэ нь мөн агаараас хүнд тул хязгаарлагдмал орон зайг дүүргэж чаддаг. Эдгээр баримтуудаас болж хлор нь дайнд зэвсэг болгон ашигласан анхны хийн химийн бодис байсан бөгөөд дэлхийн 1-р дайны үед аль аль тал нь түүнийг нам дор суваг, шуудуунд үе үе тарааж байв.
Химийн түүхийн талаархи сонирхолтой баримтууд. Химийн талаархи сонирхолтой баримтууд
Хими бол сургуулийн танил хичээл юм. Хүн бүр урвалжуудын хариу үйлдлийг үзэх дуртай байв. Гэхдээ цөөхөн хүн химийн талаар сонирхолтой баримтуудыг мэддэг бөгөөд бид энэ нийтлэлд хэлэлцэх болно.
- 1. Орчин үеийн зорчигч тээврийн онгоцууд есөн цагийн нислэгт 50-75 тонн хүчилтөрөгч хэрэглэдэг. Үүнтэй ижил хэмжээний бодисыг фотосинтезийн явцад 25000-50000 га ойд үйлдвэрлэдэг.
- 2. Нэг литр далайн усанд 25 грамм давс агуулагддаг.
- 3. Устөрөгчийн атомууд маш жижиг тул тэдгээрийн 100 саяыг гинжин хэлхээнд дараалан байрлуулахад урт нь ердөө нэг сантиметр болно.
- 4. Дэлхийн далай дахь нэг тонн усанд 7 миллиграмм алт агуулагддаг. Далайн усанд байгаа энэ үнэт металлын нийт хэмжээ 10 тэрбум тонн байдаг.
- 5. Хүний биед ойролцоогоор 65-75% ус агуулагддаг. Энэ нь шим тэжээлийг зөөвөрлөх, температурыг зохицуулах, шим тэжээлийн нэгдлүүдийг уусгахад эрхтэн тогтолцоонд ашиглагддаг.
- 6. Химийн тухай сонирхолтой баримтууд манай Дэлхий гаригт хамаатай. Жишээлбэл, сүүлийн 5 зууны хугацаанд түүний масс нэг тэрбум тонноор нэмэгджээ. Сансрын бодисууд ийм жин нэмсэн.
- 7. Савангийн бөмбөлөгний хана нь хүний нүдээр харж чадах хамгийн нимгэн материал байж магадгүй юм. Жишээлбэл, цаас эсвэл үсний зузаан нь хэдэн мянга дахин зузаан байдаг.
- 8. Савангийн хөөс хагарах хурд 0,001 секунд. Цөмийн урвалын хурд нь 0.000 000 000 000 000 001 секунд юм.
- 9. Хэвийн төлөвтөө маш хатуу, удаан эдэлгээтэй материал болох төмөр нь 5 мянган градусын температурт хий болж хувирдаг.
- 10. Нар ганцхан минутын дотор манай гарагийн бүтэн жилийн зарцуулснаас илүү их энерги үйлдвэрлэдэг. Гэхдээ бид үүнийг бүрэн ашиглаж чаддаггүй. Нарны энергийн 19% нь агаар мандалд шингэж, 34% нь сансарт буцаж, ердөө 47% нь дэлхийд хүрдэг.
- 11. Хачирхалтай нь боржин чулуу нь дуу чимээг агаараас илүү сайн дамжуулдаг. Тэгэхээр хүмүүсийн хооронд боржин чулуун хана (хатуу) байсан бол тэд нэг километрийн зайд дуу чимээ сонсох болно. Энгийн амьдралд ийм нөхцөлд дуу чимээ ердөө зуун метр л явдаг.
- 12. Шведийн эрдэмтэн Карл Шелле химийн элементүүдийн тоогоороо дээд амжилтыг эзэмшдэг. Энэ нь хлор, фтор, бари, вольфрам, хүчилтөрөгч, манган, молибден агуулдаг.
- Хоёрдугаар байрыг Швед Жакоб Берзелиус, Карл Монсандер, Английн Хамфри Дэви, Францын Пол Лекок де Бойсбордант нар хуваалаа. Тэд орчин үеийн шинжлэх ухаанд мэдэгдэж байгаа бүх элементийн дөрөвний нэгийг (өөрөөр хэлбэл тус бүр 4) нээх үүрэгтэй.
- 13. Хамгийн том цагаан алтны бөөм бол "Уралын аварга" гэгддэг. Түүний жин нь 7 кг 860.5 грамм юм. Энэхүү аварга биетийг Москвагийн Кремлийн Очир эрдэнийн санд хадгалдаг.
- 14. НҮБ-ын Ерөнхий Ассамблейн зарлигаар 1994 оноос хойш 9-р сарын 16-ны өдрийг озоны давхаргыг хамгаалах олон улсын өдөр болгон тэмдэглэдэг.
- 15. Орчин үеийн хийжүүлсэн ундаа үйлдвэрлэхэд өргөн хэрэглэгддэг нүүрстөрөгчийн давхар ислийг Английн эрдэмтэн Жозеф Пристли 1767 онд нээжээ. Дараа нь Пристли шар айраг исгэх явцад үүссэн бөмбөлгийг сонирхож эхлэв.
- 16. Бүжиглэх далайн амьтан - энэ бол Японы гайхалтай хоолны нэр юм. Шинээр баригдаж устгасан далайн амьтаныг аяга будаатай саванд хийж, үйлчлүүлэгчийн өмнө шар буурцагтай цуу дуслуулдаг. Шар буурцагны соусанд агуулагддаг натритай харилцан үйлчлэхэд үхсэн далайн амьтан ч мэдрэлийн төгсгөлүүд хариу үйлдэл үзүүлж эхэлдэг. Энэхүү химийн урвалын үр дүнд нялцгай биетүүд хавтан дотор "бүжиглэж" эхэлдэг.
- 17. Скатол нь өтгөний өвөрмөц үнэрийг хариуцдаг органик нэгдэл юм. Сонирхолтой баримт бол их тунгаар хэрэглэхэд энэ бодис нь хүнсний үйлдвэр, үнэртэй ус үйлдвэрлэхэд хэрэглэгддэг тааламжтай цэцгийн үнэртэй байдаг.
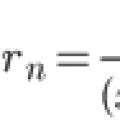 Тейлорын цувралын өргөтгөл Энгийн хувьд Кошигийн асуудлын ойролцоо шийдэл
Тейлорын цувралын өргөтгөл Энгийн хувьд Кошигийн асуудлын ойролцоо шийдэл Сургуульд юу заадаггүй вэ, юуг сургадаггүй вэ гэж асуу
Сургуульд юу заадаггүй вэ, юуг сургадаггүй вэ гэж асуу Мөнгө бодох томъёо (А
Мөнгө бодох томъёо (А