Химийн хичээлийн сургуулийн олимпиад. Сургуулийн сурагчдад зориулсан бүх Оросын химийн олимпиад
Сургуулийн үе шатБүх Оросын химийн олимпиад 2016.
9-Р АНГИ
1-р ХЭСЭГ (туршилт)
Даалгавар бүрийн хувьд хэд хэдэн хариулт өгсөн бөгөөд тэдгээрийн зөвхөн нэг нь зөв байна. Зөв хариултыг сонго. Даалгаврын дугаарыг бичиж, сонгосон хариултын дугаарыг оруулна уу.
1. Хамгийн их молекул жинтэй
1) BaCl 2 2) BaS0 4 3) Ba 3 (P0 4) 2; 4) Ba 3 R 2. (1 оноо)
2. Гурван элементийн бодис нь...
1) хүхрийн хүчил; 2) шохойн шохой (кальцийн исэл);
3) төмрийн (III) хлорид; 4) зэсийн сульфат. (1 оноо)
З.Молекулын урвалын тэгшитгэл дэх коэффициентүүдийн нийлбэр
(CuOH) 2 C0 3 + HC1 = CuC1 2 + C0 2 + ... (2 оноо)
1)10: 2)11; 3)12; 4)9.
4. 6.255 г фосфор (V) хлорид агуулагдах бодисын хэмжээ (моль) (2 оноо)
1)0,5; 2)0,3; 3)0,03; 4)0,15.
5. 3.612∙10 23 азотын атом агуулсан хөнгөн цагаан нитратын дээжийн масс (грамаар)
1)127,8; 2)42,6; 3)213; 4)14,2. (2 оноо)
6. 40 К изотопын цөм дэх протон ба нейтроны тоо
1) p = 20, n = 19; 2) p = 40, n = 19; 3)p= 19,n=21: 4)p=21,n=19. (2 оноо)
7. Тунадас үүсэхэд хүргэдэг урвал
1) KOH + HC1; 2) K 2 C0 3 + H 2 S0 4; 3) Cu(OH) 2 + HNO 3; 4) Na 2 S + Pb(N0 3) 2. (2 оноо)
8. Цайр (5.2 гр) ба цайрын карбонат (5.0 гр) холимог нь давсны хүчилтэй урвалд ороход хийнүүд (n.s.) хэмжээгээр ялгардаг. (2 оноо)
1) 0.896 л; 2) 1.792 л; 3) 2.688 л: 4) 22.4 л.
9. 150 г кальцийн хлоридыг 250 мл усанд уусгана. Уусмал дахь давсны массын хувь (хувиар) дараахтай тэнцүү байна.
1) 60; 2) 37,5; 3) 75; 4) 62,5 (2 оноо)
10. 672 мл эзэлхүүнтэй 0.84 г жинтэй хийн молийн масс нь тэнцүү байна.
1)44; 2)28; 3)32; 4)16. (2 оноо)
Нийт 18 оноо
2-р ХЭСЭГ (хувиргах гинж)
Текстийг унших.
Нэг цэрэг хээрийн хажуугаар алхаж байсан бөгөөд тэр зогсоод гэр бүлийнхэндээ захидал бичихээр шийдсэн боловч түүнд ямар ч хамаагүй. Тэгээд хар хайрга олж үзээд зурсан. Би энэ чулуугаар захидал бичээд унтахаар шийдсэн. Тэр гал руу хайрга шидсэн - тэр шатаж, зөвхөн утаа гарч ирэв. Утаа бороог зогсоож, газарт хадаж; Ус нь хүнд, шохойтой урсаж байв. Ус хатаж эхэлж, зарим газар хэвээр үлдэж, хатсан газарт аль хэдийн цагаан хайрга хэвтэж байв. Цэрэг сэрж, бороо хар хайрга чулууг хэрхэн цагаан болгож байгааг гайхав. Тэр цагаан хайрга авч, цагаан чулуун дээгүүр гүйж харвал тэр зурж байв. Цэрэг гайхан цааш явав.
Өөрчлөлтийн гинжин хэлхээ үүсгэж, түүнийгээ шийдээрэй. (8 оноо )
(10 оноо)
3-Р ХЭСЭГ (даалгавар)
Анхны дизайнерууд сансрын хөлөгболон шумбагч онгоцнууд асуудалтай тулгарсан: хөлөг онгоц эсвэл сансрын станц дээр агаарын тогтмол найрлагыг хэрхэн хадгалах вэ, i.e. илүүдэл нүүрстөрөгчийн давхар ислийг хэрхэн арилгах, хүчилтөрөгчийн хангамжийг сэргээх вэ? Гоёмсог шийдэл олдсон - бид CO 2-ыг O 2 болгох хэрэгтэй! Үүний тулд хүчилтөрөгч дэх калийг шатаах явцад үүсдэг калийн хэт ислийг (KO 2) ашиглахыг санал болгов. Калийн хэт исэл нь нүүрстөрөгчийн давхар исэлтэй урвалд ороход чөлөөт хүчилтөрөгч ялгардаг (хүчилтөрөгчийн атомууд нь нэгэн зэрэг исэлдүүлэгч ба бууруулагч бодис юм). Текстэнд хэлэлцсэн урвалын тэгшитгэлийг бич. Хүн өдөрт дунджаар 0.51 м 3 нүүрсхүчлийн хий ялгаруулна гэдгийг мэдсээр байж нэг сарын (30 хоног) гурван хүний бүрэлдэхүүнтэй багийн амьжиргааг хангахын тулд сансрын станцад хэр хэмжээний калийн хэт исэл байх ёстойг тооцоол. (24 оноо)
Залуу химич багшаасаа калийн гидроксид, цайрын хлорид, барийн хлорид, калийн сульфидын уусмал агуулсан шошгогүй дөрвөн шил авчээ. Ууссан уусмал тус бүр дэх бодисын концентраци 0.1 моль/л байна. Нэмэлт урвалж хэрэглэхгүйгээр зөвхөн фенолфталеины цаас (фенолфталеины спиртийн уусмалд дэвтээсэн цаас)гүйгээр лонхны агуулгыг хэрхэн тодорхойлох вэ? Залуу химичдэд хийх дарааллыг санал болго. Гарах урвалын тэгшитгэлийг бич. ( 40 оноо)
Бүх Оросын химийн олимпиадын сургуулийн үе шат ХАРИУ
9-Р АНГИ
ХЭСЭГ 1 Туршилт.
| Ажлын дугаар | Боломжит хариулт | Онооны тоо |
| Нийт 18 оноо |
||
ХЭСЭГ 2 Өөрчлөлтийн гинж.
Даалгавар 11
| Онооны тоо |
||
| Гинж бий болсон | C-CO 2 -H 2 CO 3 -CaCO 3 | |
| 1 тэгшитгэл | ||
| 2 тэгшитгэл | CO 2 +H 2 O=H 2 CO 3 | |
| 3 тэгшитгэл | H 2 CO 3 + CaO = CaCO 3 + H 2 O | |
| Нийт 8 оноо |
||
Даалгавар 12
| урвалын тэгшитгэл 1 бичигдсэн байна | CuSO 4 + 2KOH = Cu(OH) 2 ↓ + K 2 SO 4 | 2 оноо |
| урвалын 2-р тэгшитгэлийг бичнэ | Cu(OH) 2 = CuO + H 2 O (халаалт) | 2 оноо |
| урвалын 3-р тэгшитгэлийг бичнэ | CuO + H 2 = Cu + H 2 O | 2 оноо |
| урвалын 4-р тэгшитгэлийг бичнэ | Cu + HgSO 4 = CuSO 4 + Hg | 2 оноо |
| урвалын 5-р тэгшитгэлийг бичнэ | CuSO 4 + Ba(NO 3) 2 = BaSO 4 ↓ +Cu(NO 3) 2 | 2 оноо |
| Нийт 10 оноо |
||
ХЭСЭГ 3 Даалгаврууд.
Даалгавар 13.
| Хүчилтөрөгч дэх калийн шаталтын урвалын тэгшитгэлийг бичнэ | 5 оноо |
|
| Калийн хэт исэл ба нүүрстөрөгчийн давхар ислийн харилцан үйлчлэлийн урвалын тэгшитгэлийг бичсэн. | 4KO 2 + 2CO 2 = 2K 2 CO 3 + 3O 2 | 5 оноо |
| Усан онгоцонд байх ёстой калийн хэт ислийн хэмжээг тооцоолно. | Хүн өдөрт 0.51 м 3 = 510 л нүүрстөрөгчийн давхар исэл ялгаруулдаг бөгөөд энэ нь 510 л: 22.4 л / моль = 22.77 моль, үүнийг ашиглахын тулд 2 дахин их калийн хэт исэл шаардагдана, өөрөөр хэлбэл. 45.54 моль буюу 3.23 кг. | 14 оноо |
| Нийт 24 оноо |
||
Даалгавар 14
| Фенолфталеин нь шүлтлэг орчинд час улаан өнгөтэй болдог. Өнгө нь калийн гидроксид ба калийн сульфидын уусмалд илэрдэг. Бид аль лонхыг калийн гидроксид, калийн сульфид агуулсан болохыг тодорхойлдог. | |
| Хэрэв урвалжаас илүү хэмжээгээр уусдаг желатин тунадас үүсвэл нэмсэн уусмалд калийн гидроксид, задлан шинжилж буй уусмалд цайрын хлорид орно. | |
| Дээжинд K 2 S ба KOH уусмал нэмэхэд харагдахуйц өөрчлөлт гардаггүй колбонд барийн хлорид агуулагддаг. | |
| Нийт 40 оноо |
|
Энэхүү олимпиад нь хүн бүрт нээлттэй!
Химийн чиглэлээр суралцах сонирхолтой хүн бүрт зориулан олон улсын шинэ олимпиадыг эхлүүлж байна. Ерөнхий боловсролын сургуулийн 8-11-р ангийн сурагчид болон ерөнхий боловсролын сургуулийн нэг, хоёрдугаар дамжааны сурагчдыг мэдлэгээ сорьж, хичээл зүтгэл, онолын үндэслэлээрээ зохих шагналаа авахыг урьж байна.
Mega Talent төвд химийн хичээл хэрхэн заадаг вэ?Янз бүрийн насны ангиллын оролцогчдод зориулж онолын асуулт, даалгавар, диаграмм, дүрслэл бүхий даалгавар зэрэг тусдаа багц даалгавруудыг бэлтгэсэн.
Энэ улиралд бид ямар сэдвүүдийг давтаж байна вэ?
- Химийн түүх, химийн нээлтүүд
- Металл ба металл бус бодисын химийн шинж чанар
- Нүүрс устөрөгч
- Тарсан хэвлэл мэдээллийн хэрэгсэл болон бусад сэдвүүд
Оролцогчид янз бүрийн төрлийн 15 тестийн асуулт хүлээн авна.
- Нэг буюу хэд хэдэн зөв хариулттай асуултууд.
- Хоёр өгөгдлийн цувралыг уялдуулах, харьцуулах даалгавар.
- Тайлбарлах эх сурвалжтай ажиллах шаардлагатай даалгаварууд.
- Эхний цуврал өгөгдлүүдтэй холбоотой асуудлыг шийдвэрлэх даалгавар.
Олимпиадын даалгавар нь Холбооны улсын боловсролын стандартад нийцэж байгаа бөгөөд дараахь байдлаар тусалдаг.
- Химийн ойлголтын аппарат, бэлгэдлийн хэлийг эзэмш.
- Бодис, тэдгээрийн хувирал, практик хэрэглээний талаархи анхны системчилсэн санааг бий болгох.
- Химийн шинжлэх ухааны үндэс суурь нь орчин үеийн байгалийн шинжлэх ухааны салбар болох объектив ач холбогдлыг ухамсарлах.
Зохион байгуулагч болон эцэг эхчүүдийг тусдаа шагналууд хүлээж байна
Бид мөн тусгай талархал илгээх болно
Танай боловсролын байгууллагад
Та бас хүлээн авах болно
Бүх оролцогчдод зориулсан бэлэг Бүх оролцогчид "Амжилтын хүснэгт"-ийг хүлээн авдаг бөгөөд үүнд манай арга хэмжээнд оролцсоны үр дүн, хувийн амжилтын талаархи мэдээллийг оруулах боломжтой.
Инфографик 10 ба түүнээс дээш оролцогчийн хүсэлт гаргасан багш нар ангиллын хувийн үнэлгээг инфографик хэлбэрээр авах боломжтой.
Мэдээллийн постер зарлал Мэдээллийн постерын тусламжтайгаар та өөрийн боловсролын байгууллагад манай арга хэмжээг хялбархан зохион байгуулж эхлэх боломжтойМэдээллийн постер татаж авах
- Сайтын вэбсайтад бүртгүүлнэ үү.
- Оролцогчдын тоог зааж, оролцох хүсэлтээ өгнө үү.
- Өөрт тохирсон хэлбэрээр төлбөрөө төлж өргөдлөө баталгаажуулна уу.
- Нэг өргөдөлд зөвхөн нэг олимпиадын кураторын нэр, нэг цол байж болно боловсролын байгууллага, энэ нь оролцогчид болон кураторын шагналын материалд тусгагдах болно. Шаардлагатай бол та үйл явдалд олон бичлэг оруулах боломжтой.
- Хүлээн авсан арга зүйн материалыг олимпиад явуулахад ашиглах (арга зүйн зөвлөмж, оролцогчдын ангилал тус бүрийн даалгавар, хариултын маягт).
- Товч танилцуулга эхлэхээс өмнө оюутны ажлыг байршуулна уу.
- Үр дүн нийтлэгдсэн өдрийн дараа бөглөсөн өргөдлөөсөө шагналын материалыг татаж авна уу.
- Оюутнууд гадны тусламжгүйгээр бүх даалгавраа бие даан гүйцэтгэх ёстой.
- Хариултын хүснэгтийг бөглөхдөө хариуцлагатай байгаарай - оролцогчийн үр дүн үүнээс хамаарна!
- Шаардлагатай бүх талбарыг зөв бөглөнө үү. Оруулсан өгөгдлийг өөрчлөх хугацаа хязгаарлагдмал.
- Оролцогчдын бүтээлийг хугацаанд нь нэмээгүй тохиолдолд бүртгэлийн хураамжийг буцаан олгохгүй гэдгийг санаарай!
Олимпод хэн түрүүлэх вэ?
Манай арга зүйчид сургуулийн сургалтын хөтөлбөрт тохирсон даалгавруудыг хийдэг. Эдгээр нь бүсийн олимпиадуудаас илүү энгийн боловч сургуулийн шалгалтаас илүү сонирхолтой, олон янз байдаг. Манай даалгаврыг онц сурлагатан, материалыг хангалттай түвшинд мэддэг оюутнууд гүйцэтгэдэг. Гэсэн хэдий ч, олимпиадад оролцсон туршлага нь хангалттай мэдлэгтэй оюутнуудад сонирхолтой байдаг.
Бид өнгөрсөн улиралд олимпод оролцсон. Энэ олимпиадын даалгавар ижил үү?
Үгүй ээ, бид улирал бүрт шинэ даалгавар бэлддэг. Янз бүрийн улирлын даалгаварууд нь өөр өөр хэсгүүдэд тулгуурладаг сургалтын хөтөлбөр. Та дахин олимпиадад оролцох боломжтой.
Олимпиадын багц даалгаврууд ямар харагдаж байна вэ?
Даалгавар гарсан өдөр төлбөрөө төлсөн бүх багш нар олимпиадад зориулсан багц материалыг татаж авах боломжтой. Үүнд:
- УдирдамжОлимп зохион байгуулсны төлөө.
- Мега-Авьяас МХЗЭ-ийн захирлаас оролцогчид урам зориг өгөх захидал.
- Төрөл бүрийн 15 даалгаврын багц.
- Удахгүй болох үйл явдлын хуанли.
Олимпиадын дүнг хэрхэн үнэлж байна вэ?
Хариултуудыг вэб сайтын тусгай хүснэгтэд оруулсны дараа тэдгээрийг баталгаажуулахаар илгээнэ.Зөв хариулт бүрт оюутан 2 оноо авна. Хэрэв тестийн асуулт нь хоёр хариултын сонголттой бөгөөд оюутан зөвхөн нэг хувилбарыг зөв зааж өгсөн бол 1 оноо авна.
Шагналыг хэрхэн хуваарилдаг вэ?
- 30 оноо авсан олимпиадын оролцогчийг хамгийн дээд шагнал болох ялагчийн дипломоор шагнана.
- 26-29 оноо авсан оролцогчид 2,3-р байр, ялагчдын диплом олгоно.
- Бусад бүх оролцогчид хувийн гэрчилгээ авдаг.
Шагналыг дүгнэх өдөр татаж авах боломжтой.
Олимпиадад оролцох төлбөрийг хэрхэн төлөх вэ?
Төлбөрийн хувьд санал болгож буй аргуудын аль нэгийг ашиглана уу:
- Банкны карт VISA/MasterCard/Maestro
- QIWI түрийвч
- Yandex.Money Wallet
- Банк эсвэл Оросын шуудангийн салбараар дамжуулан шилжүүлэх
- Өөртөө үйлчлэх терминал дээр бэлэн мөнгө
Үйл явдал бүрт тус тусад нь төлбөр төлөхгүй, бүх төлбөрийн мэдээллийг дахин бөглөхгүйн тулд та хувийн дансаа цэнэглэх боломжтой.
Олимпиадад оролцох мөнгөө хэрхэн хэмнэх вэ?
Олимпиад зохион байгуулах зардлыг бид нөхөн төлнө. Өргөдөлд хэдий чинээ олон оюутан тусгана, төдий чинээ багшийн зардлын нөхөн олговрын хувь өндөр байна.
Мөн та сайт дээрх үлдэгдлээ нөхөх замаар хэмнэх боломжтой. Та үлдэгдлээ нөхөхөд нөхөн төлбөрийн хэмжээнээс хамааран 7-20% урамшуулал авах болно.
Багш нар яагаад Мега-Авьяаслаг олимпиадуудыг сонгодог вэ?
- Энгийн өргөдлийн маягт
- Тохиромжтой нэвтрэх арга зүйн материалболон шагналууд
- Хариултаа өөрөө оруулж, алдаан дээрээ ажиллана
- Даалгавар, шагналын материалыг хэвлэх зардлын нөхөн төлбөр
- Өвөрмөц, олон янзын даалгаварууд
Оролцогчдын зураг







Сэтгэл хангалуун багш нарын 1000 гаруй шүүмж
Бид анх удаа олимпод оролцож байгаа юм биш, үнэхээр их таалагдаж байна. Даалгаврын хэлбэр нь сонирхолтой бөгөөд тав тухтай орчинд хийж, түвшингээ шалгах боломжтой. Оюутнуудад үнэхээр таалагдаж байна. Баярлалаа...
Ольга Ружина
МАОУ "56-р дунд сургууль"
-д маш их баярлалаа чөлөөт өрсөлдөөн By дүрслэх урлаг"Намрын симфони". 1-р ангийн хүүхдүүд өөрсдийн гараар гар урлал хийх дуртай байсан. Дипломууд надад үнэхээр таалагдсан.
Ирина Романова
FGKOU "140-р дунд сургууль"
Бид анх удаа 1-р ангийн сурагчидтай хийсэн арга хэмжээнд оролцож маш их баяртай байлаа. Хүүхдүүдэд авъяаслаг гэдгийг нь мэдрүүлэх боломжийг олгосон зохион байгуулагчдад баярлалаа!
Ольга Кусакина
Магнитогорск хотын "Б.Ручёвын нэрэмжит 64-р дунд сургууль" хотын боловсролын байгууллага
Эрхэм хүндэт хамт олон, энэхүү тэмцээнийг зохион байгуулсанд баярлалаа! Даалгавруудыг тэмдэглэлийн хамт маш сонирхолтой байдлаар сонгосон ардын соёл(орчны ертөнц). Хүүхдүүд бид хоёр тэмцээнд маш их сэтгэл хангалуун байсан бөгөөд хамгийн гол нь...
Ирина Обрезкова
Хотын боловсролын байгууллага Игнатовская дунд сургууль
Хүндэт мэргэжил нэгтэнгүүдээ! Mega Talent Олимпод үнэхээр дуртай, даалгаварууд нь сонирхолтой, хүүхдүүд оролцохдоо баяртай байна. Энэхүү арга хэмжээ нь багш нарт гэрчилгээ олгоход бэлтгэхэд тусалдаг. Баярлалаа....
Наталья Подкина
GAPOU SO Хүнс, Үйлчилгээний Үйлдвэрлэлийн Техникийн Коллеж "Хоолны"
Олимпиадыг зохион байгуулсан зохион байгуулагчдад баярлалаа. Даалгаврууд нь сонирхолтой бөгөөд сургамжтай байв. Миний шавь нар үүнийг хийх дуртай байсан.
Татьяна Мясникова
Олимпийг зохион байгуулагчдад маш их баярлалаа. Энэ бол бидний анх удаа оролцож байгаа явдал юм. Хүүхдүүд мэдлэгээ сорих сонирхолтой байсан. Цаашдын амжилт хүсье!!! Ганц асуулт асуухад уучлаарай - оюутнууд...
Корженко
Хүүхдийн олимпийг зохион байгуулсанд маш их баярлалаа. Охин чинь таны асуудлыг шийдэхэд маш их баяртай байна!!!
Дарья Новикова
FTS-лицей
Хүүхдүүдийг ийм сайхан, сонирхолтой арга хэмжээнд оролцох боломжийг олгосон зохион байгуулагчдад маш их баярлалаа. Бид анх удаа оролцож байгаа бөгөөд илүү чухал үр дүнд хүрнэ гэж найдаж байна...
Виктор Пермитин
МАОУ-ын 6-р дунд сургууль
Оролцох боломж олгосон зохион байгуулагчдад баярлалаа.
Анатолий Князков
Өдрийн мэнд Шавь нар маань математикийн олимпиадад анх удаа оролцож, сайн туршлага хуримтлуулж, үр дүндээ сэтгэл хангалуун байна. Зохион байгуулагчдад баярлалаа!
Анатолий Князков
Би болон шавь нар маань энэхүү асуулт хариултын уралдаанд анх удаа оролцож байна. Маш их баярлалаа. Миний сурагчид асуулт хариултын уралдаанд маш их таалагдсан!!!
Лилит Варданян
Хотын боловсролын байгууллага Раменская 9-р дунд сургууль
Зохион байгуулагчдад маш их баярлалаа. Танай вэбсайт дээр сургуулийн сурагчид, багш нарт зориулсан олон янзын арга хэмжээ байдаг. Бид тантай дахин хамтран ажиллаж, арга хэмжээнд тань оролцохдоо баяртай байх болно. Шандараев С.А.МБОУ "Гусев...
Сергей Шандараев
Өдрийн мэнд Хүүхдүүдийг олимпиадад оролцох боломжийг олгосон зохион байгуулагчдад баярлалаа. Олимпиад оюутнуудын дунд ихээхэн сонирхлыг төрүүлэв. Бид анх удаагаа оролцсон. Маш сонирхолтой, эрхэм ээ...
Анатолий Князков
Арга хэмжээг зохион байгуулагчдад маш их баярлалаа! Кроссворд хийх сонирхолтой асуултуудыг сонгосон. Залуус даалгавраа баяртайгаар гүйцэтгэсэн!
Татьяна Коробейникова
MBOU "1-р лицей" МО "Бугуруслан"
Хүүхдэд зориулсан олимпиад, асуулт хариулт, уралдаан тэмцээн, төрөл бүрийн арга хэмжээ зохион байгуулахыг хичээсэн та бүхэндээ маш их баярлалаа. Таны үйл ажиллагаа нь хүүхдүүдэд илүү гүнзгий суралцах хүслийг төлөвшүүлэхэд хувь нэмэр оруулдаг ...
Сергей Астраханцев
МАОУ" ахлах сургууль№24, Баатрын нэрэмжит Зөвлөлт Холбоот УлсМ.В. Водопянова". Красноярск.
"Дидактикийн мэдлэг" асуулт хариултын тэмцээнд оролцов. Мэдлэгээ шалгах боломж олгосон танд баярлалаа! Би "хөөрөх" хэрэгтэй байсан ч бүх даалгавраа биелүүлсэндээ маш их баяртай байна.
Людмила Бердникова
FKOU "ОХУ-ын Свердловск муж дахь Холбооны хорих газрын дунд сургууль"
Манай “онцгой” оюутнуудад оролцох боломж олгосон зохион байгуулагчдад маш их баярлалаа! Маш сонирхолтой даалгавар, сайтар бодож боловсруулсан зохион байгуулалт. KOGOBU VSSH тосгон Лесной Верхнекамск дүүрэг.
Анастасия Кузнецова
KOGOBU VSSH тосгон Лесной Верхнекамск дүүрэг
Бид сургуулийн сурагчид, оюутнууд оролцдог бүх Оросын болон олон улсын олимпиадуудыг зохион байгуулдаг. Химийн чиглэлээр "Мега-Авьяас" олимпиадыг ерөнхий боловсролын сургуулийн 8-11-р ангийн сурагчид болон ерөнхий боловсролын сургуулийн нэг, хоёрдугаар курсын сурагчдын дунд зохион байгуулдаг. Бид бүх оролцогчдыг диплом, сертификатаар шагнаж урамшуулдаг. Олимпиадыг зохион байгуулсан багш нар биднээс сертификат, талархал хүлээн авдаг.
МХЗ “Мега-Авьяас” статистикийн нүдээр:
- Бид 400 гаруй олимпиад зохион байгуулж, хичээлийн жагсаалтыг 47 төрөл болгон өргөжүүлсэн.
- Химийн олимпиадад 12 орны 11000 сурагч оролцжээ.
- Бид зохион байгуулалтын зардлыг нөхөхийн тулд багш нарт 2,500,000 рубль төлсөн.
- Олимпиадад оролцсон багш нарын 98 хувь нь нэг удаа байнгын зохион байгуулагч болдог.
Багш руу 5 алхам
Бидэнтэй хамтран ажиллах нь тохиромжтой бөгөөд ашигтай, учир нь бид үргэлж 5 алхмыг дагаж, багш бүрийг бодож, түүний санаа зовоосон асуудлуудыг анхаарч үздэг.
- Бид бүх ангиудын бие даалтанд нэг дор нэвтэрч, олимпиад явуулах арга зүйн зөвлөмжийг бэлтгэж байна.
- Улирал бүр бид таны багцыг төрөлжүүлэхийн тулд гэрчилгээ, талархлын загварыг өөрчилдөг.
- Бид хэвлэх даалгавар, шагналын зардлыг нөхөж таны мөнгийг хэмнэнэ.
- Сар бүр бэлэг өгч, хамгийн идэвхтэй багшийг мэргэжил дээшлүүлэх курст үнэ төлбөргүй явуулдаг.
- Бид онлайн чат, имэйл болон Skype-аар дамжуулан таны асуултанд цаг алдалгүй хариу өгдөг.
Оюутнууд химийн чиглэлээр Мега-Авьяаслаг олимпиадад дуртай
Зайны олимпиадыг сурагчдад танил, тохь тухтай нөхцөлд, төрөлх сургуулийнхаа ханан дотор зохион байгуулдаг. Танил орчин нь тэдэнд шаардлагагүй түгшүүрээс ангижрах, гол зүйл болох даалгавраа биелүүлэхэд анхаарлаа төвлөрүүлэхэд тусалдаг. Тиймээс Мега-Авьяаслаг олимпиадууд нь чадвардаа эргэлзэж буй оюутнуудын хувьд өөрийгөө илэрхийлэх боломж болдог.
Олимпиадын амжилтаас үл хамааран хүн бүр оролцох нөхцөлийг бүрдүүлдэг. Манай олимпиадын даалгавруудыг сургуулийн сургалтын хөтөлбөрийн дагуу эмхэтгэсэн бөгөөд Холбооны улсын боловсролын стандартын шаардлагыг хангасан болно. Бид зөвхөн оюутнуудын олимпиадын үеэр дуусгаж чадсан сэдвүүдийг багтаасан болно.
Анги тус бүрийн даалгавар нь янз бүрийн төрлийн 15 асуултаас бүрдэнэ.
- Нэг буюу хэд хэдэн зөв хариулттай асуултууд.
- Хоёр өгөгдлийн цувралыг уялдуулах даалгавар.
- Тайлбарлах эх сурвалжтай ажиллах шаардлагатай даалгаварууд.
- Эхний цуврал өгөгдлөөр асуудлыг шийдвэрлэх даалгавар.
Олимпиадад оролцох зардал, нөхөн төлбөрийн хэмжээ
Олимпиадын материалыг авахын тулд та бүртгэлийн хураамж төлөх шаардлагатай. Олимпиадын хуудсан дээр нэг оролцогчийн бүртгэлийн хураамжийн хэмжээг зааж өгсөн болно. Бид энэ дүнгийн 30 хүртэлх хувийг багшид даалгавар, шагналын материалыг хэвлүүлэхээр буцааж өгдөг.Нөхөн төлбөрийн хэмжээ нь олимпиадад оролцогчдын тооноос хамаарна. Дараа нь нөхөн олговрын нөхцлийн талаар илүү ихийг мэдэх болносайт дээр бүртгүүлэх.
Олимпиадыг зохион байгуулагчид автоматаар орнобагшийн үнэлгээ , сар бүр шинэчлэгддэг. Үнэлгээний тэргүүлэгчид үнэ цэнэтэй бэлэг авдаг.
Хичээлийн жилд бид химийн чиглэлээр 7 олимпиад зохион байгуулдаг
Манай төвд жил бүр Бүх Оросын 3, олон улсын 4 олимпиад болдог. Олимпиадын хуваарийг тэмцээнүүдийн хооронд завсарлага авахгүй байхаар зохион байгуулдаг.
Та сайтад зочлох бүртээ манай олимпиадад оролцох хүсэлтээ гаргаж болно. Бид олимпиад бүрт шинэ даалгавар бэлддэг тул хүмүүс манай олимпиадад жилд 2-3, заримдаа 7 удаа оролцдог.
Ажлыг автоматаар баталгаажуулах, үр дүнг нийтлэх
Тестийн даалгаврыг оюутнуудын хариултыг тусгай хүснэгтэд оруулсны дараа шууд автоматаар үнэлнэ Хувийн бүс. Дүн гарсан өдөр та өөртөө болон олимпиадад оролцсон бүх сурагчдын шагналыг татаж авах боломжтой.
Хэрхэн химийн олимпиад зохион байгуулагч болохыг мэдэхгүй хэвээр байна уу?
- Вэбсайтад бүртгүүлнэ үү.
- Хуваарь руу оч мөн химийн олимпиадыг сонго.
- Өргөдөл гаргаж, олимпиадад оролцогчдын тоог зааж өгнө үү.
- Даалгавар, удирдамжийг татаж авахын тулд өргөдлөө баталгаажуулна уу.
- Хүлээн авсан материалыг хэвлэж, олимпиад явуулна.
- Өөрийн хувийн дансанд оролцогчдын хариултыг нэмнэ үү.
- Дүгнэлт хийх өдөр үр дүнг шалгаж, зохих шагналаа татаж аваарай
Химийн олимпиадад оролцох төлбөрийг хэрхэн төлөх вэ?
Та бүртгэлийн хураамжийг дараах аргуудын аль нэгээр төлж болно.
- Банкны картаар төлбөр хийх (онлайн);
- ОХУ-ын шуудангийн газарт төлбөрийн баримтаар төлөх;
- Цахим төлбөрийн систем ашиглан төлбөр хийх (онлайн).
Олимпиадад ОХУ-аас гадна сургуулийн сурагчид, оюутнууд оролцох боломжтой юу?
Манай бүх олимпиадад дэлхийн аль ч орны сурагч, оюутнууд оролцох боломжтой. Бүх даалгавар орос хэл дээр бичигдсэн тул оюутнуудад тавигдах цорын ганц шаардлага бол орос хэлийг чөлөөтэй эзэмшсэн байх явдал юм. Биднээс байнга асуудаг бусад асуултын хариултыг цуглуулсан .
Бичлэг
1 1 ХИМИЙН СУРГУУЛИЙН ХҮҮХДҮҮДИЙН БҮХ ОРОСЫН ОЛИМПИАД ХОТЫН ШАТ. 9 АНГИ Олимпиадын даалгаврыг үнэлэх шийдэл, шалгуурууд Оролцогч хамгийн их оноо авсан таван шийдлийг санал болгож буй зургаан бодлогын эцсийн үнэлгээнд тооцно. Хамгийн бага оноотой асуудлуудын нэгийг тооцдоггүй. 1. Хүчиллэг ислийн шинж чанарууд Хүчиллэг исэл нь өөр бодистой молийн харьцаатай урвалд орох урвалын тэгшитгэлийг бич: a) 1: 1, b) 1: 2, c) 2: 1, d) 1: 3, e) 1 : 6 (Уурвал бүрд та хүчиллэг ислийг өөрөө сонгож болно.) a) SO 3 + H 2 O = H 2 SO 4 b) CO 2 + 2KOH = K 2 CO 3 + H 2 O c) 2SO 2 + O 2 = 2SO 3 d) P 2 O 5 + 3H 2 O = 2H 3 PO 4 e) P 2 O 5 + 6KOH = 2K 3 PO 4 + 3H 2 O 2 тэгшитгэл бүрт оноо. Аль ч тохиолдолд хэд хэдэн сонголт хийх боломжтой бөгөөд нөхцөлийг хангасан үндэслэлтэй хариултуудыг хүлээн авна. 2. Эзлэхүүнийг багасгах урвал Устөрөгч ба хүчилтөрөгчийн холимог байдаг. Энэ хольц нь цахилгаан очоор асдаг. Очлуур өнгөрсний дараа хийн эзлэхүүний харьцаа ямар байх үед хольцын хэмжээ яг дөрөвний нэгээр (тогтмол температур ба даралт) буурах вэ? Үүссэн усны хэмжээг үл тоомсорлож болно. Хариултын хоёр хувилбарыг өгч, тэдгээрийг тооцоогоор дэмжээрэй. 2H 2 (g) + O 2 (g) = 2H 2 O (l) Урвалын тэгшитгэлийн дагуу 3 моль хийнээс 2 моль ус үүсдэг. Үүний үр дүнд хий дэх бодисын хэмжээ 3 моль-оор буурдаг
2 нь анхны хэмжээний дөрөвний нэг, өөрөөр хэлбэл урвал эхлэхээс өмнө 12 моль хий байсан. Хоёр сонголт боломжтой: 1) илүүдэл устөрөгч: 11 моль H 2 ба 1 моль O 2, эзлэхүүний харьцаа H 2: O 2 = 11: 1 2) илүүдэл хүчилтөрөгч: 2 моль H 2 ба 10 моль O 2, эзлэхүүний харьцаа H 2: O 2 = 1: 5 Үнэлгээний систем: урвалын тэгшитгэл 1 оноо, "илүүдэл дутагдал" гэсэн санааг дурдах 1 оноо, хариултын сонголт бүр 4 оноо, үүнээс хольцын найрлагыг тооцоолоход 3 оноо. моль, эзлэхүүний харьцаа 1 оноо. 3. Нүүрстөрөгчийн давхар ислийн нэгдлээс үүсэх хүчилтөрөгч шүлтлэг металлХүчилтөрөгчтэй бол X бодис нь нүүрстөрөгчийн давхар исэлтэй урвалд ордог. Цорын ганц урвалын бүтээгдэхүүн нь металл карбонат ба хүчилтөрөгч юм молийн харьцаа 2: 3, массын харьцаа 23: 8. Х-ийн томъёог гаргаж, нүүрстөрөгчийн давхар исэл ба устай урвалын тэгшитгэлийг бич. Металлыг массын харьцааг молийн харьцаатай харьцуулж тодорхойлж болно: m(m2co 3) 2 M (M2CO 3) 2 M (M2CO 3) 23 = = =, m(o) 3 M (O) эндээс М( M 2 CO 3) = 138 г / моль, энэ нь K 2 CO 3, металл K. Формула X нь урвалын тэгшитгэлээр тодорхойлогддог. X K a O b томьёог тэмдэглээд эхлээд диаграммыг, дараа нь урвалын тэгшитгэлийг зуръя. Схем: K a O b + CO 2 2K 2 CO 3 + 3O 2. Тэгшитгэл: 4KO 2 + 2CO 2 = 2K 2 CO 3 + 3O 2. X KO бодис 2. Устай хийх урвалын тэгшитгэл: 4KO 2 + 2H 2 O = 4KOH + 3O 2. (H 2 O 2 үүсэх урвалын тэгшитгэлийг мөн хүлээн зөвшөөрнө: 2KO 2 + 2H 2 O = 2KOH + H 2 O 2 + O 2.) 2
3 3 Үнэлгээний систем: металл тодорхойлох 2 оноо, X томьёо тогтоох 4 оноо, урвалын тэгшитгэл, 4 оноо тус бүр 2 оноо. 4. Электронууд ч гэсэн масстай 2 Хоёр элементээс бүрдэх ямар бодис электроны массын хувьд хамгийн их байдаг вэ? Тооцоолол эсвэл үндэслэлтэй аргументуудыг ашиглан хариултаа товч тайлбарла. Атом нь протон, нейтрон, электронуудаас бүрддэг. Атом дахь электронуудын тоо серийн дугаарэлемент Z. Протон ба нейтроны массыг ойролцоогоор тэнцүү гэж үзээд электроны массын хувийг илэрхийлэх илэрхийллийг бичнэ үү: N(e) m(e) N(e) m(e) ω(e) = = = N(e) m( e) N(p) m(p) N(n) m(n) N(e) m(e) N(p) N(n) m(p) Zm(e) ) 1 = = Zm(e) Am (p) A m(p) 1 Z m(e) Энд N нь атом дахь өгөгдсөн төрлийн бөөмсийн тоог, A нь массын тоо юм. Электрон массын фракц хамгийн их байхын тулд A/Z харьцаа хамгийн бага байх ёстой. Энэ нь 1 H атомын хувьд 1-тэй тэнцүү, бусад бүх атомын хувьд энэ нь 2 ба түүнээс дээш байна. Тиймээс нэгдэл нь хамгийн бага (боломжтой бол) A / Z харьцаатай H атом ба өөр элементийн атомыг агуулсан байх ёстой Энэ тохиолдолд аль болох их устөрөгч байх ёстой. Бүгдээс устөрөгчийн нэгдлүүд CH дахь устөрөгчийн хамгийн том массын хувь 4. Нүүрстөрөгчийн атом 12 С нь A / Z = 2 тул хоёр дахь элемент болоход тохиромжтой. Хариулт: CH 4. Үнэлгээний систем: нэгдэл нь H атомыг агуулсан байх ёстой гэсэн бодол, 4 оноо, CH 4-ийн талаархи бодол 6 оноо (устөрөгчийн бага масстай нэгдэл, жишээ нь NH 3, H 2 O, 6 биш 3 оноо), хэрэв зөвхөн зөв хариултыг үндэслэлгүйгээр өгсөн бол 0 оноо.
4 4 5. Хар нунтгийн судалгаа Залуу химич өөрт байгаа хэрэгслээр хар нунтаг шинжилжээ. Нунтаг нь агаарт, хүчилтөрөгчийн урсгалд удаан хугацаанд шохойжсон үед бодисын өнгө нь бараан болж, шатаж буй шүдэнзний үнэртэй төстэй хурц үнэртэй хий ялгардаг. Бодисын масс нь кальцинжуулах явцад өөрчлөгдөөгүй. Цаашдын судалгаагаар анхны туршилтын бодис нь халсан ч шингэрүүлсэн хүхрийн хүчилд уусдаггүй, харин кальцинжуулах бүтээгдэхүүн нь хүчилд сайн уусч, уусмал үүсгэдэг. цэнхэр өнгө. Залуу химич эдгээр ажиглалтын үндсэн дээр уг бодис нь хоёр элементээс бүрддэг гэсэн зөв дүгнэлтэд хүрчээ. a) Судалж буй бодисын найрлагад ямар элементүүд багтдаг вэ? б) Судалж буй бодисын томъёо юу вэ? в) Хүчилтөрөгчийн оролцоотой бодисыг шохойжуулах үед үүсэх урвалын тэгшитгэлийг бич. г) Массын яагаад гэдгийг тооцоолол ашиглан тайлбарла хатуухалаахад өөрчлөгддөггүй. a) Судалгаанд хамрагдаж буй бодисын найрлагад зэс, хүхэр (элемент тус бүрд 1.5 оноо, нийт 3 оноо) орно. b) Cu 2 S бодисын томъёо (3 оноо; CuS 0 оноо). в) Cu 2 S + 2O 2 = 2СuO + SO 2 (3 оноо; CuS-ийн шаталтын зөв тэгшитгэлийг өгсөн бол мөн 3 оноо өгнө). d) 1 моль Cu 2 S (160 гр) масс нь SO 2 урвалын бүтээгдэхүүн болох 2 моль CuO-ийн масстай тэнцүү байна. хийн бодис(1 оноо).
5 5 6. Химийн усан оргилуур Химийн хичээл дээр дараах туршилтыг хийв. Цагаан талст бодисыг Wurtz колбонд 1 (1-р зургийг үз) хийж, дөлийг шар өнгөтэй болгосон. Дусал юүлүүр 2-ыг ашиглан баяжуулсан хүхрийн хүчил 1-р колбонд асгаж, агаараас 1.26 дахин хүнд өнгөгүй хий тэр даруй үүсч эхлэв. Үүссэн хийг дугуй ёроолтой колбонд цуглуулсан 3. 1) Зурагт үзүүлсэн төхөөрөмжид ямар хий гарсан бэ. 1? Хариултаа зөвтгөж, тооцоолол, урвалын тэгшитгэлээр баталгаажуулна уу. 2) Энэ хий яагаад ус биш харин агаарыг нүүлгэн шилжүүлэх замаар цуглуулсан бэ? Зураг 1 3) Усан оргилуур дотор нь "гэрэлтэж" эхлэхийн тулд хий дүүргэсэн колбо 3-тай юу хийх хэрэгтэй вэ (Зураг 2-ыг үз)? Хариултаа тайлбарлана уу. 4) Хэрэв та 4-р талстжуулагч руу асгавал юу ажиглагдах вэ (2-р зургийг үз): а) метил жүржийн усан уусмал; б) мөнгөний нитратын уусмал? 5) "Усан оргилуур"-ын хувьд яагаад хавтгай ёроолтой колбо хэрэглэхээс илүү дугуй ёроолтой колбыг ашиглах ёстой вэ? Зураг 2 1) Устөрөгчийн хлоридыг төхөөрөмжид авсан. M = 1.26 29 г/моль = 36.5 г/моль (2 оноо) Хүхрийн хүчилнатрийн хлорид руу хийнэ. Натрийн ионууд нь дөлийг шар өнгөтэй болгодог нь мэдэгдэж байгаа бөгөөд энэ нь давсны найрлагад натри байгааг нотолж байна. (1 оноо) Урвал Wurtz колбонд 1 явагдана: NaCl + H 2 SO 4 = NaHSO 4 + HCl. (1 оноо) (Тэгшитгэлийг зөвшөөрнө: 2NaCl + H 2 SO 4 = Na 2 SO 4 + 2HCl) 2) Устөрөгчийн хлорид нь усанд сайн уусдаг тул усыг нүүлгэн шилжүүлэх замаар цуглуулж чадахгүй. (1 оноо) 3) Колбонд "усан оргилуур өгөх" тулд хий гаргахгүйгээр хийн гаралтын хоолой бүхий таглаагаар хаах шаардлагатай. Дараа нь колбонд бага хэмжээний ус хийнэ, дотор нь устөрөгчийн хлорид уусна.
6 ба колбонд вакуум үүснэ. Хэрэв хийн гаралтын хоолойн төгсгөлийг ус руу буулгавал атмосферийн даралтын нөлөөн дор колбонд орж эхэлнэ. (2 оноо) 4) Устөрөгчийн хлоридыг колбонд уусгахад давсны хүчил үүснэ. a) Давсны хүчилд индикаторын улбар шар өнгө улаан болж өөрчлөгдөнө. (1 оноо) б) Харьцахдаа давсны хүчилмөнгөний нитратын уусмалаар цагаан тунадас үүсч, хольц нь үүлэрхэг болно: HCl + AgNO 3 = HNO 3 + AgCl. (1 оноо) 5) "Усан оргилуур" үзүүлэхдээ колбоны дотор вакуум үүсдэг тул түүний хананд гаднаас ихээхэн дарамт үүсдэг. Дугуй ёроолтой колбоны хувьд түүний хананд даралтыг жигд хуваарилдаг. Тиймээс дугуй ёроолтой колбыг ашиглах үед даралтын зөрүүгээс болж тэсрэх магадлал бага байдаг. Колбоны хана нь бүрэн гөлгөр, бүрэн бүтэн байх ёстойг анхаарах нь чухал бөгөөд тэдгээр дээр хагарал, зураас, чипс байх ёсгүй. (1 оноо) 6
2015 2016 оны хичээлийн жилд СУРГУУЛИЙН ХҮҮХДҮҮДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. СУРГУУЛИЙН ШАТ 9-р анги Шийдэл, үнэлгээний шалгуур Оролцогчийн оноо авсан таван шийдэл
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2016 2017 оны хичээлийн жил ХОТЫН ШАТ. 9-Р АНГИ Бие даалт, хариулт, үнэлгээний шалгуур Ерөнхий заавар: хэрэв асуудалд тооцоо шаардлагатай бол тэдгээр нь заавал байх ёстой.
Бүх Оросын олимпиадХимийн сургуулийн сурагчид, 2013/14 оны I шат 11-р ангийн даалгавар 1. Дараах химийн урвалын тэгшитгэлийн зүүн эсвэл баруун талыг сэргээнэ үү 1) t 2Fe 2 O 3 + 2FeCl 3 2) 2Cu 2 CO 3 (OH)
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2016 2017 оны хичээлийн жил ХОТЫН ШАТ. 10-р АНГИ Бие даалт, хариулт, үнэлгээний шалгуур Ерөнхий заавар: хэрэв асуудалд тооцоо шаардлагатай бол тэдгээр нь заавал байх ёстой.
Химийн сургуулийн сурагчдын бүх Оросын олимпиад Хотын шат 9-р анги Асуудлын шийдэл 2017 Даалгавар 1. Төмрийн (II) хлоридын 136 г ханасан усан уусмал дээр 34 г усгүй давс нэмсэн. Хүлээн авсан
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 014 015 СУРГУУЛИЙН ШАТ. 10 1-Р АНГИ Олимпиадын даалгаврыг үнэлэх шалгуур Оролцогчийн оноо авсан 5 шийдэл
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2017 2018 оны хичээлийн жил СУРГУУЛИЙН ШАТ. 9-Р АНГИ Даалгавар, хариулт, үнэлгээний шалгуур Даалгавар 1. Хоёр хий X ба Ү хоёр хий нь харилцан бие биедээ хувирах чадвартай.
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2016 2017 оны хичээлийн жил ХОТЫН ШАТ. 8-Р АНГИ Бие даалт, хариулт, үнэлгээний шалгуур Ерөнхий заавар: хэрэв асуудалд тооцоо шаардлагатай бол тэдгээр нь заавал байх ёстой.
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2018 2019 оны хичээлийн жил СУРГУУЛИЙН ШАТ. 9-Р АНГИ Даалгавар, хариулт, үнэлгээний шалгуур Даалгавар 1. Гурван хүчил Нэг сул, хоёр хүчтэй өөр өөр суурьтай гурван хүчил,
Хими - 8-9-р анги Хамгийн их оноо 100. 9-1. Үүнтэй ижил хэмжээний металл 0.8 г хүчилтөрөгч, 8.0 г галогентэй урвалд ордог. Асуудалд дурдсан галогенийг тодорхойлно уу. Хариултаа баталгаажуулна уу.
2013/2014 оны хичээлийн жилд химийн чиглэлээр сургуулийн сурагчдад зориулсан бүх Оросын 1 олимпиад. г.ШИЙДЭЛТЭЙ ДААЛГАВАР 9-р ангийн даалгавар 9-1. Стандарт нөхцөлд энгийн бодисоос OF 2 үүсэх дулаан нь
СУРГУУЛИЙН ХҮҮХДИЙН БҮХ ОРОСЫН ХИМИЙН ОЛИМПИАД 2015 2016 СУРГУУЛИЙН 11-Р АНГИ Шийдэл, үнэлгээний шалгуур Оролцогч хамгийн өндөр оноо авсан таван шийдлийг зургаан бодлогын эцсийн үнэлгээнд оруулсан болно.
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2017 2018 оны хичээлийн жил СУРГУУЛИЙН ШАТ. 8-Р АНГИ Даалгавар, хариулт, үнэлгээний шалгуур Даалгавар 1. Нэгдлийн урвал Хэд хэдэн бодисоос нэгдэл үүсэх урвалд а
2015 2016 оны хичээлийн жилд СУРГУУЛИЙН ХҮҮХДҮҮДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. СУРГУУЛИЙН ШАТ 10-р анги Шийдэл ба үнэлгээний шалгуур Оролцогчийн оноо авсан таван шийдэл
Олон салбарын олимп. 2017/2018 он хичээлийн жил. Москвагийн технологийн их сургууль. Эцсийн шат. Химийн даалгавар. 11-р анги Даалгавар 1. А, В, С гурван хийн хольц нь устөрөгчийн нягттай тэнцүү байна
ХИМИЙН СУРГУУЛИЙН ХҮҮХДИЙН ОЛИМПИАД 2014 ОНЫ ХОТЫН ШАТ 9 Олимпиадын даалгавар шийдвэрлэх, үнэлэх арга зүйн зөвлөмж 9-р ангийн даалгавар 1. Нийт 10 оноо 1 2 3 4 5 6 7 8 9 3 121
9-р анги 1. Аль бодисуудын 1 моль задрахад хамгийн их (молоор) ион үүсэх вэ? 1. Натрийн сульфат 2. Төмрийн (III) хлорид 3. Натрийн фосфат 4. Кобальт (II) нитрат 2. Нэгдлүүдийг зааж өгнө үү.
Янз бүрийн ангиудын хоорондын харилцааг баталгаажуулсан хариу үйлдэл органик бус бодисууд(даалгаврын дүн шинжилгээ 37). Химийн багш MBOU 25-р дунд сургууль Татьяна Павловна Корнилова. Химийн өөрчлөлтийг дагалддаг урвалын шинж тэмдэг
8-р ангийн химийн хичээлийн жилийн сорил. би сонголт. Заавар: Жил бүр дуусгана туршилтын ажилХимийн хичээлд 45 минут өгдөг. Уг ажил нь 2 хэсгээс бүрдэх ба 20 даалгавартай. 1-р хэсэг
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2016 2017 оны хичээлийн жил СУРГУУЛИЙН ШАТ. 9-Р АНГИ Бие даалт, хариулт, үнэлгээний шалгуур 6 бодлогоос эцсийн дүн нь оролцогчийн оноо авсан 5 шийдлийг багтаана.
2015 2016 оны хичээлийн жилд СУРГУУЛИЙН ХҮҮХДҮҮДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. ХОТЫН ШАТ 9-р анги Шийдэл, үнэлгээний шалгуур Оролцогч хамгийн өндөр оноо авсан 5 шийдлийг 6 бодлогоос эцсийн үнэлгээнд тооцно.
Сургуулийн сурагчдад зориулсан бүх Оросын олимпиад Хотын шат Химийн даалгавар 9-р ангийн ОНОЛЫН ТОЙР Даалгавар 9- (6 оноо) NO бөөмд хэдэн электрон, протон орсон бэ? Хариултаа зөвтгөөрэй. Аваач
1. Яагаад төлбөр тэнцүү байнанүүрстөрөгчийн атомын цөм? 1) 0 2) +6 3) +12 4) -1 2. 12 6С ба 11 6С атомуудад нийтлэг зүйл юу вэ? 1) Массын тоо 2) Протоны тоо 3) Нейтроны тоо 4) Цацраг идэвхит шинж чанар
2017 Асуудлын шийдэл Химийн сургуулийн сурагчдад зориулсан бүх Оросын олимпиад Хотын шат 10-р ангийн даалгавар 1. "Есөн элемент" Үелэх системд есөн элемент байдаг бөгөөд тэдгээрийн нэр нь орос хэл дээр байдаг.
ЧАНАРЫН ДААЛГАВАР Органик бус химиМАОУ "40-р дунд сургууль" Старый Оскол химийн багш Баштрыков П.М. 1. А металлыг урвалд оруулах замаар гаргаж авсан уусмалд натрийн карбонатын илүүдэл уусмал нэмнэ
Сонголт 3 2 1. XO 4 ион нь 50 электрон агуулдаг. Үл мэдэгдэх элементийг тодорхойлж, X-ийн харилцан үйлчлэлийн тэгшитгэлийг хэлбэрээр бич энгийн бодисхалуун төвлөрсөн азотын хүчилтэй. (6 оноо) Шийдэл.
IX анги төгсөгчдийн улсын (эцсийн) аттестатчилал боловсролын байгууллагууд 2009 (шинэ хэлбэр) ХИМИ Демо хувилбар шалгалтын хуудасХолбооны мужаас бэлтгэсэн
"ХИМИ" ХИЧЭЭЛИЙН ЧАДВАРТ ЧИГЛҮҮЛСЭН ДААЛГАВАР Даалгавар 1 X элемент нь байгальд өргөн тархсан өнгө, үнэргүй хий хэлбэртэй энгийн бодис үүсгэдэг. Хэд хэдэн нь мэдэгдэж байна
Химийн олимпиад 2015 оны 9-р ангийн хариулт >>> Химийн олимпиад 9-р анги 2015 оны хариулт Химийн олимпиад 9-р анги 2015 оны хариулт Химийн олимпиад 9-р анги 2015 оны хариулт Хлорофилийн молекул агуулагдаж байгааг харгалзан тэдгээрийн массыг олоорой.
C1 Хими. 11-р анги. Сонголт KHI1060 1 Нарийвчилсан хариулт бүхий даалгаврыг үнэлэх шалгуур Цахим балансын аргыг ашиглан урвалын тэгшитгэлийг үүсгэ: Cu 2 O + = SO 2 + + H 2 O Исэлдүүлэгч бодисыг тодорхойлно
Сургуулийн сурагчдад зориулсан бүх Оросын олимпиад II (хотын) шат Хими, 0-р анги Үнэлгээний шалгуур Даалгавар 0- (4 оноо). Манганы давхар исэлд А хүчлийн уусмал нэмэхэд хортой бодис ялгардаг
"Катав Ивановск хотын 1-р дунд сургууль" хотын боловсролын байгууллага Катав-Ивановский хотын дүүргийн Завсрын сургалт явуулах туршилт, хэмжих материал
Сургуулийн сурагчдад зориулсан бүх Оросын олимпиадын II (хотын) шат Хими, 9-р анги Үнэлгээний шалгуур Даалгавар 9- (3 оноо) Протаргол (8% орчим мөнгө агуулсан хуурай хэлбэрээр мөнгөний протеинатын %-ийн усан уусмал).
1-р хувилбар 1. XO 2 ион нь 24 электрон агуулдаг. Үл мэдэгдэх элементийг тодорхойлж, халуун лититэй энгийн бодис болох X-ийн харилцан үйлчлэлийн тэгшитгэлийг бич. (6 оноо) Шийдэл. Үл мэдэгдэх элемент
Ерөнхий боловсролын сургуулийн IX ангийн 2009 оны төгсөгчдийн улсын төгсөлтийн аттестатчиллын төслийн шалгалтын ажил (шинэ хэлбэрээр) ХИМИЙН шалгалтын ажил.
Химийн хичээлийн зуны даалгавар: 1. SO 3 бодист 160 г агуулагдах хүчилтөрөгчийн атомтай ижил тооны хүчилтөрөгчийн атом агуулагдах CO 2 бодисын химийн ямар хэмжээ вэ? 2. CH 4 бодис ямар химийн бодис агуулдаг вэ
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2017 2018 оны хичээлийн жил ХОТЫН ШАТ. 8-Р АНГИ Бие даалт, хариулт, үнэлгээний шалгуур Ерөнхий заавар: хэрэв асуудалд тооцоо шаардлагатай бол тэдгээр нь заавал байх ёстой.
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2017 2018 оны хичээлийн жил ХОТЫН ШАТ. 9-Р АНГИ Бие даалт, хариулт, үнэлгээний шалгуур Ерөнхий заавар: хэрэв асуудалд тооцоо шаардлагатай бол тэдгээр нь заавал байх ёстой.
9-р анги 1. Х нэгдэл дэх элементүүдийн массын хувь: натри 16.61%, устөрөгч 1.44%, хүчилтөрөгч 34.66%, Е элемент 47.29%. X нэгдлийн найрлагыг тодорхойл. Тодорхойлолтыг тодорхойлох урвалын тэгшитгэлийг өг
4.3.3 11-р ангийн даалгавар 1. Нэг чухал шинж чанарууд ковалент холбоонь түүний туйлшрал юм. Дараах нэгдлүүдийн аль нь туйлшралтай байна N-E холболтуудхамгийн бага уу? 1. H 2 O 2. H 2 S 3. H 2 Se 4.
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2018 2019 оны хичээлийн жил СУРГУУЛИЙН ШАТ. 10-Р АНГИ Бие даалт, хариулт, үнэлгээний шалгуур Даалгавар 1. Зүүн талууд Химийн урвалын тэгшитгэлийн зүүн талыг сэргээ.
Сургалтын сонголтхимийн чиглэлээр OGE-д бэлтгэх шалгалтын хуудас. Ажлыг гүйцэтгэх заавар нь ажлыг дуусгахад 2 цаг (120 минут) хуваарилсан. Энэхүү бүтээл нь 22 хэсгээс бүрдэх 2 хэсгээс бүрдэнэ
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2014 ОН 015 СУРГУУЛИЙН ШАТ. 11 1-Р АНГИ Олимпиадын даалгаврыг үнэлэх шалгуур 6 бодлогын эцсийн үнэлгээнд оролцогчийн оноо авсан 5 шийдлийг багтаасан болно.
4.1.3 11-р ангийн даалгавар 1. Ковалентын холбооны нэг чухал шинж чанар нь түүний урт юм. Дараах холболтуудын аль нь хамгийн бага холбооны урттай вэ? 1. HF 2. HCl 3. HBr 4. HI 2. Олон тооны
Хими. 9-р анги Сонголт 003-1 ХИМИЙН улсын үндсэн шалгалт Сонголт 003 Ажлыг гүйцэтгэх заавар Шалгалтын ажил нь 22 даалгавар бүхий хоёр хэсгээс бүрдэнэ. 1-р хэсэг нь агуулна
ХИМИЙН хичээлээр 9-р ангийн сурагчдын дунд шатны аттестатчилал (гэр бүлийн боловсрол, бие даан суралцах хэлбэрээр) шалгалтын материалын үлгэрчилсэн хувилбар 4 5 Үндсэн дэд бүлгийн V (А) бүлгийн 4-р үед
ХИМИ Сонголт 0000 Өргөдөл гаргагчдад зориулсан заавар шалгалтын ажлыг дуусгахад 3 цаг (180 минут) хуваарилсан. Уг ажил нь 40 даалгаврыг багтаасан 2 хэсгээс бүрдэнэ. Хэрэв даалгаврыг нэн даруй дуусгах боломжгүй бол,
4.3 Интернэт аяллын даалгавар (хоёр дахь давалгаа) Пермийн үндэсний судалгааны их сургуулийн http://ege.psu.ru цахим платформыг ашиглан интернетийн аялал онлайнаар явагдлаа.
Хими. Хариултын түлхүүр 10-р ангийн даалгавар 1. Археологийн экспедиц Крымд малтлага хийх үеэр үл мэдэгдэх хайлшаас үл мэдэгдэх эрин үеийн хоёр ер бусын зоос олжээ. Зоосны найрлагад дүн шинжилгээ хийхийн тулд тэдгээрийг илгээсэн
Ломоносовын нэрэмжит химийн олимпиад 10-11-р ангийн даалгаврын шийдэл 2-р хувилбар 1.6. Дараах бодисуудын химийн томъёог өгч, IUPAC дүрмийн дагуу нэрлэнэ үү: кварц, цусны улаан давс,
9-р анги Шийдэл (1 хувилбар) Асуудлын шийдэл 9.1: Б хүчил, хэвийн нөхцөлд анхны тусламжийн хайрцаг бүрт байдаг цагаан талст бодис нь борын хүчил юм. Тиймээс энгийн бодис А
Хими. 9-р анги 2 Үзүүлэх тестийн хувилбар хэмжих материал 2012 онд анхан шатны мэдлэг эзэмшсэн оюутнуудад ХИМИЙН улсын (эцсийн) аттестатчилал (шинэ хэлбэрээр) явуулах.
10-р зэрэглэл 1. 35 мл архины нитратын 15%-ийн усан уусмалд (нягшил 1.08 г/мл) 2.34 г хөнгөн цагааны гидроксидыг жижиг хэсгүүдэд нэмнэ. Үүссэн уусмал нь хүрээлэн буй орчны ямар хариу үйлдэл үзүүлэх вэ? Селитра
Химийн улсын нэгдсэн шалгалт 2019: тооцооны асуудал Молчанова Галина Николаевна Ph.D. химийн багш MOU Koterevskaya дунд сургууль 1 Химийн асуудал шийдвэрлэх чадвар нь тухайн сэдвийг бүтээлчээр эзэмших гол шалгуур юм. Шийдвэр гаргахдаа
1. Үндсэн шинж чанаруудыг элементийн гаднах исэл харуулж байна: 1) хүхэр 2) азот 3) бари 4) нүүрстөрөгч 2. Томъёоуудын аль нь электролитийн диссоциацийн зэрэглэлийн илэрхийлэлтэй тохирч байна: 1) α = n. \n 2) V m = V\n 3) n =
10-11-р ангийн сурагчдад зориулсан химийн чиглэлээр Ломоносовын нэрэмжит олимпиадын захидал харилцааны даалгаврын сонголтууд (11-р сар) Даалгавар 1 1.1. Цууны хүчил яагаад буцлах цэгээс өндөр (118ºC) байдгийг тайлбарла
1-р хэсэг 1 15 даалгаврын хариулт нь зөв хариултын тоотой тохирох нэг тоо юм. Ажлын текстийн хариултын талбарт энэ тоог бичнэ үү. 1 Эзлэгдсэн электрон давхаргын тоо 1) тоотой тэнцүү байна
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2016 2017 оны хичээлийн жил СУРГУУЛИЙН ШАТ. 10-Р АНГИ Даалгавар, хариулт, үнэлгээний шалгуур Төгсгөлийн ангид 6 бодлого, 5 шийдэлд оролцогч
8-9-р ангийн химийн чиглэлээр дунд шатны гэрчилгээ олгох асуултууд Сурах бичиг Г.Е., Рудзитис, Ф.Г.Фельдман "Хими 8-р анги", "Хими 9-р анги" Москва 2014 1. Тогтмол хуульТэгээд тогтмол хүснэгт химийн элементүүд
ДААЛГАВАР 3 Бодлого шийдвэрлэх жишээ Жишээ 1. Шошгогүй дөрвөн туршилтын хоолойд натрийн сульфат, натрийн карбонат, натрийн нитрат, натрийн иодид зэрэг бодисуудын уусмал агуулагдаж байна. Юугаар харуулах
FIPI OGE туршилт 2018 он Химийн чиглэлээр Сургалтын 1-р хувилбар Бэлтгэсэн Мустафина Екатерина Андреевна 1 Дээрх зурагт атомын загварыг харуулав 1) бор 2) хөнгөн цагаан 3) азот 4) бериллий 2 Атомын радиус
Бүрэн цагийн үе шат. 11-р анги. Шийдэл. Даалгавар 1. Гурвын холимог хий A, B, Cустөрөгчийн нягт нь 14. Энэ хольцын 168 г жинтэй хэсгийг идэвхгүй уусгагч дахь бромын илүүдэл уусмалаар дамжуулсан.
СУРГУУЛИЙН ХҮҮХДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. 2018 2019 оны хичээлийн жил ХОТЫН ШАТ. 8-Р АНГИ Бие даалт, үнэлгээний шалгуур Ерөнхий заавар: хэрэв даалгаварт тооцоо шаардлагатай бол заавал өгөх ёстой.
31-р даалгаврын зөв шийдэл нь 4-ийн тэгшитгэлийг агуулсан байх ёстой. Урвалын тэгшитгэл бүрийг зөв бичихийн тулд та 1 оноо авах боломжтой. Энэ даалгаврыг гүйцэтгэснээр та дээд тал нь 4 оноо авах боломжтой. Хүн бүр үнэн
2015 2016 оны хичээлийн жилд СУРГУУЛИЙН ХҮҮХДҮҮДИЙН ХИМИЙН БҮХ ОРОСЫН ОЛИМПИАД. ХОТЫН ШАТ 8-р анги Шийдэл, үнэлгээний шалгуур Оролцогч хамгийн өндөр оноо авсан 5 шийдлийг 6 бодлогоос эцсийн үнэлгээнд тооцно.
Олимпиад "ЛОМОНОСОВ" ХИМИЙН ХУВИЛБАР 1 1.1. Ихэнх сээр нуруутан амьтдын цусны улаан өнгө нь гемоглобинтой холбоотой байдаг. Гемоглобины устөрөгчийн массын хувийг тооцоолоорой C 2954 H 4516 N 780 O 806 S 12 Fe 4. (4 оноо)
ХИМИЙН ШАЛГАЛТЫН ШАЛГАЛТ (ЭЧНИЙ 9-Р АНГИ) 1. Химийн урвал, тунадас үүсэх замаар явна a) h 2 SO 4 + BaCl 2 b) HNO 3 + KOH c) HCl + CO 2 d) HCl + Ag 2. Аль бодисоор a) карбонат
Онолын дугуй 9-р анги 9-р анги Бодлого 1. 5.55 г кальцийн гидроксид агуулсан уусмал 3.96 г нүүрстөрөгчийн давхар ислийг шингээсэн. Энэ тохиолдолд тунадас ямар масс үүссэн бэ? Ca(OH) 2 + CO 2 = CaCO 3 + H 2 O (1)
Сургуулийн сурагчдын олимп "Бор шувууны толгодыг байлдан дагуулаарай!" химийн чиглэлээр Бүтэн цагийн аялал 01 жил 1. Фосфорын долоон атомын массыг тооцоол. M (P) 31 м 7 7 = 3.0 10 N 3 A.010 Хариулт: 3.0 10 РОСТОВ Хувилбар 11. Хийн хольц
Төмөр 1. 7. Төмөр ба хөнгөнцагааны ислийн шинж чанарын талаарх дараах дүгнэлтүүд үнэн үү? A. Хөнгөн цагаан ба төмөр хоёулаа +3 исэлдэлтийн төлөвт тогтвортой исэл үүсгэдэг. B. Төмрийн (III) исэл нь амфотер шинж чанартай. 2.
4.1.2 10-р ангийн даалгавар 1. Ковалентын холбооны нэг чухал шинж чанар нь түүний урт юм. Дараах холболтуудын аль нь хамгийн их харилцааны урттай вэ? 1. HF 3. HBr 2. HCl 4. HI 2. Хамгийн органик бус
Одоо олимпиад 4 үе шаттай явагдаж байна. Бүх Оросын олимпиадыг зохион байгуулах нь ОХУ-ын Боловсрол, шинжлэх ухааны яамнаас баталсан журмаар зохицуулагддаг.
Бүх Оросын болон Бүх Холбооны химийн олимпиадын газарзүй (1965-2015)
| Олимпиадын дугаар | Жил | Хот | Олимп |
|---|---|---|---|
| I | Бүх Оросын | ||
| 2. | 1966 | Казань | Бүх Оросын |
| 3. | 1967 | Днепропетровск | Бүх холбоот |
| 4. | 1968 | Вильнюс | Бүх холбоот |
| 5. | 1969 | Ростов-на-Дону | Бүх холбоот |
| 6. | 1970 | Воронеж | Бүх холбоот |
| 7. | 1971 | Минск | Бүх холбоот |
| 8. | 1972 | Уфа | Бүх холбоот |
| 9. | 1973 | Баку | Бүх холбоот |
| 10. | 1974 | Донецк | Бүх холбоот |
| 11. | 1975 | Вильнюс | Бүх холбоот |
| 12. | 1976 | Киев | Бүх холбоот |
| 13. | 1977 | Алматы | Бүх холбоот |
| 14. | 1978 | Казань | Бүх холбоот |
| 15. | 1979 | Кишинев | Бүх холбоот |
| 16. | 1980 | Ереван | Бүх холбоот |
| 17. | 1981 | Фрунзе | Бүх холбоот |
| 18. | 1982 | Таллин | Бүх холбоот |
| 19. | 1983 | Тбилиси | Бүх холбоот |
| 20. | 1984 | Душанбе | Бүх холбоот |
| 21. | 1985 | Рига | Бүх холбоот |
| 22. | 1986 | Донецк | Бүх холбоот |
| 23. | 1987 | Ташкент | Бүх холбоот |
| 24. | 1988 | Вильнюс | Бүх холбоот |
| 25. | 1989 | Пермийн | Бүх холбоот |
| 26. | 1990 | Минск | Бүх холбоот |
| 27. | 1991 | Иваново | Бүх холбоот |
| 28. | 1992 | Самара | Бүх холбоот |
| 29. | 1993 | Липецк | Бүх Оросын |
| 30. | 1994 | Казань | Бүх Оросын |
| 31. | 1995 | Н.-Новгород | Бүх Оросын |
| 32. | 1996 | Самара | Бүх Оросын |
| 33. | 1997 | Казань | Бүх Оросын |
| 34. | 1998 | Белгород | Бүх Оросын |
| 35. | 1999 | Рязань | Бүх Оросын |
| 36. | 2000 | Владимир | Бүх Оросын |
| 37. | 2001 | Ульяновск | Бүх Оросын |
| 38. | 2002 | Великий Новгород | Бүх Оросын |
| 39. | 2003 | Чебоксары | Бүх Оросын |
| 40. | 2004 | Челябинск | Бүх Оросын |
| 41. | 2005 | Белгород | Бүх Оросын |
| 42. | 2006 | Уфа | Бүх Оросын |
| 43. | 2007 | Уфа | Бүх Оросын |
| 44. | 2008 | Уфа | Бүх Оросын |
| 45. | 2009 | Архангельск | Бүх Оросын |
| 46. | 2010 | Казань | Бүх Оросын |
| 47. | 2011 | Архангельск | Бүх Оросын |
| 48. | 2012 | Магнитогорск | Бүх Оросын |
| 49. | 2013 | Курск | Бүх Оросын |
| 50. | 2014 | Казань | Бүх Оросын |
| 51. | 2015 | Новосибирск | Бүх Оросын |
| 52. | 2016 | Белгород | Бүх Оросын |
| 53 | Гуравдугаар сарын 30-аас дөрөвдүгээр сарын 5 | Бүх Оросын |
2006 онд Оросын сургуулийн сурагчдын олимпиадын зөвлөл (RSOSH) бий болсон үед авъяаслаг хүүхэд, залуучуудыг хайж олох, дэмжих, дагалдуулах зорилготой олимпиад болон бусад оюуны уралдааныг зохион байгуулах ажлыг зохицуулах зорилгоор байгуулагдсан. RSOS-ийн ажлыг сургуулийн сурагчдын олимпиад зохион байгуулах журмаар зохицуулдаг. Энэ журам нь сургуулийн сурагчдын бүх Оросын олимпиадад хамаарахгүй.
Олимпиадын үе шатууд
Сургуулийн сурагчдын бүх Оросын олимпиадыг зохион байгуулах журмын дагуу Химийн хичээлийн бүх Оросын сургуулийн сурагчдын олимпиадыг 4 үе шаттайгаар явуулдаг.
- Олимпиадын сургуулийн үе шат нь агуулгад үндэслэн хотын хичээлийн арга зүйн комиссоос боловсруулсан даалгаврын дагуу явагдана. боловсролын хөтөлбөрүүдүндсэн ерөнхий ба хоёрдогч Ерөнхий боловсрол 4-11-р ангийн хувьд гүнзгийрүүлсэн түвшин ба харгалзах фокус (профайл). Олимпиадын сургуулийн үе шатыг дуусгах эцсийн хугацаа нь 11-р сарын 1-ээс хэтрэхгүй;
- Олимпиадын хотын үе шат нь ерөнхий болон дунд ерөнхий боловсролын ахисан түвшний боловсролын хөтөлбөрийн агуулга, 7-р ангийн холбогдох чиглэл (профайл) дээр үндэслэн бүс нутгийн хичээл-арга зүйн комиссын боловсруулсан даалгаврын дагуу явагдана. 11. Олимпиадын хотын шатны шалгаруулалтын эцсийн хугацаа 12-р сарын 25-аас хэтрэхгүй;
- Олимпиадын бүсийн шатыг ерөнхий болон дунд ерөнхий боловсролын ахисан түвшний боловсролын хөтөлбөрийн агуулга, холбогдох чиглэл (профиль) дээр үндэслэн олимпиадын төв сэдэв-арга зүйн комиссоос боловсруулсан даалгаврын дагуу явуулдаг. 9-11-р ангийн хувьд. Эцсийн хугацаа бүс нутгийн үе шатОлимпиад - 2-р сарын 25-аас хэтрэхгүй;
- Олимпиадын эцсийн шат нь ерөнхий болон дунд ерөнхий боловсролын ахисан түвшний боловсролын хөтөлбөрийн агуулга, 9-р ангийн харгалзах чиглэл (профиль) дээр үндэслэн төв хичээл-арга зүйн комиссын боловсруулсан даалгаврын дагуу явагдана. -11. Олимпиадын эцсийн шатны шалгаруулалт 4-р сарын 30-наас хэтрэхгүй байна.
Ерөнхий боловсролын сургуулийн үе шатыг явуулах захидал харилцааны (зайны) хэлбэрүүд
Сургуулийн сурагчдад зориулсан Бүх Оросын олимпиадын сургууль, хотын болон бүс нутгийн үе шатууд заримдаа хэд хэдэн шатанд явагддаг бөгөөд тэдгээрийн нэг нь захидал харилцаа юм. Энэхүү аялал нь аль болох олон сургуулийн сурагчдыг олимпиадад оролцуулах, бүтэн цагийн аялалд оролцогчдыг үр дүнтэй сонгох боломжийг танд олгоно. Ихэнхдээ захидал харилцааны аялалыг интернетээр явуулдаг.
Зохион байгуулалт, шинжлэх ухаан-арга зүйн ажил
Олимпиадыг зохион байгуулах, явуулах ажлыг даргын удирдлага дор зохион байгуулах төв хороо зохицуулна. Олимпиадыг зохион байгуулах төв хорооны үйл ажиллагааны зохион байгуулалт, техник, мэдээллийн дэмжлэгийг ОХУ-ын Боловсрол, шинжлэх ухааны яам хариуцдаг. Олимпиадын шинжлэх ухаан, арга зүйн дэмжлэг үзүүлэх зорилгоор Олимпиадын төв сэдэв-арга зүйн комиссууд (ТСМХ) байгуулагдсан. Химийн чиглэлээр ЦПМК-ийн бүрэлдэхүүнийг олимпиадыг зохион байгуулах төв хорооны саналаар багш, шинжлэх ухаан, шинжлэх ухаан, сурган хүмүүжүүлэх ажилчдын дундаас бүрдүүлж, ОХУ-ын Боловсрол, шинжлэх ухааны яам батална. Олимпиадыг зохион байгуулах төв хороо, Олимпиадын төв сэдэв-арга зүйн комисс, олимпиадын бүх шатны шүүгчдийн бүрэлдэхүүний үйл ажиллагааны үндсэн зарчим нь ур чадвар, бодитой, ил тод байдал, түүнчлэн мэргэжлийн ёс зүйг сахин биелүүлэх явдал юм.
Сургуулийн сурагчдад зориулсан бүх Оросын химийн олимпиад дөрвөн үе шаттайгаар явагддаг. Сургууль, хотын захиргааг ихэвчлэн 7-11-р ангийн сурагчдад онолын нэг удаагийн...
Бүс нутгийн шатанд зөвхөн 9-11-р ангийнхан оролцох боломжтой бөгөөд өөр нэг шат нэмэгдэнэ - практик. Эцсийн шат нь 9-11-р ангийн хувьд онол, практик гэсэн хоёр үе шаттайгаар явагдана.
Химийн олимпиадын даалгавар нь оролцогчдоос бусад чиглэлээр, жишээлбэл, физик, биологи, геологи, газарзүйн нэмэлт мэдлэгтэй байхыг шаарддаг. Бүх Оросын олимпиадын эцсийн шатны ялагч, шагналтнууд төрөлжсөн чиглэлээр их дээд сургуульд элсэн орохдоо тэтгэмж авдаг.
Сургуулийн сурагчдын химийн олимпиад 1938 онд Москва, Ленинград хотод болсон. Анхны Бүх Холбооны олимпиад 1967 онд болсон.
Шинэ юу байна
Хэрхэн оролцох вэ
- Олимпиадад оролцох хүсэлтэй байгаагаа хичээлийн багшдаа мэдэгдэх, ангийн багш руу, сургуулийн ахлах багш эсвэл тэмцээн хариуцсан хүн.
- Хичээлийн үе шат хэдэн өдөр, хаана явагдахыг сургуулиасаа олж мэдээрэй.
- Олимпод ирж оролцоорой.
- Сургуулийнхаа дараагийн шатанд орох үр дүн болон тэнцсэн оноогоо олж мэдээрэй.
- Хотын шатанд оролцох. Олимпиад хаана явагдахыг багшаасаа мэдэж аваарай.
- Үр дүнг олж, ажлаа сайтар хянаж, шалгууртай харьцуулж, тангарагтны бүрэлдэхүүнд асуулт асуугаарай.
- Бүсийн шатанд тэнцэх оноог хүлээнэ үү.
- Тэмцээн хаана, хэзээ болох талаар олимпиад зохион байгуулагчийн цахим хуудаснаас эсвэл тухайн бүс нутагтаа тэмцээн зохион байгуулах эрх бүхий хүнээс олж мэдээрэй.
- Бүсийн шатыг явуулахад тавигдах шаардлагыг судал. Туршилтын үеэр лабораторийн цув, резинэн бээлий эсвэл нүдний шил авчрах шаардлагатай эсэхийг шалгаарай.
- Бүсийн шатанд оролцох.
- Үр дүнгээ хүлээнэ үү. Бүтээлийг харж, үнэлгээний шалгууртай харьцуулна уу. Баталгаажуулах тангарагтны шүүгчид асуулт асууж, тэдний хариулттай санал нийлэхгүй байгаа бол давж заалдана уу.
- Эцсийн шатанд тэнцсэн оноог зарлахыг хүлээнэ үү.
- Бүс нутгийн олимпиадыг зохион байгуулагч тантай холбоо барьж, финалын тэмцээний талаар шаардлагатай мэдээллийг өгөх ёстой.
- Д оролцох эцсийн шатболон лабораторид аюулгүй байдлын арга хэмжээг дагаж мөрдөнө!
 Их Тартар - Оросын эзэнт гүрэн Хүн төрөлхтний эртний түүхийн тухай
Их Тартар - Оросын эзэнт гүрэн Хүн төрөлхтний эртний түүхийн тухай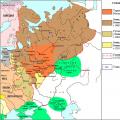 Ханхүү Иван Васильевич 1472 он
Ханхүү Иван Васильевич 1472 он "А.П. Платоновын "Үл мэдэгдэх цэцэг" түүх (бяцхан тойм). Андрей Платоновын "Үл мэдэгдэх цэцэг" өгүүллэгийн тухай "Үл мэдэгдэх цэцэг" жинхэнэ үлгэр надад юу зааж өгсөн бэ?
"А.П. Платоновын "Үл мэдэгдэх цэцэг" түүх (бяцхан тойм). Андрей Платоновын "Үл мэдэгдэх цэцэг" өгүүллэгийн тухай "Үл мэдэгдэх цэцэг" жинхэнэ үлгэр надад юу зааж өгсөн бэ?