Аминдердің жануы. Аминдер
Көмірсутекті алмастырғыштардың табиғаты бойынша аминдер бөлінеді
Аминдердің жалпы құрылымдық ерекшеліктері
Аммиак молекуласындағы сияқты, кез келген амин молекуласында азот атомының бұрмаланған тетраэдр шыңдарының біріне бағытталған жалғыз электрон жұбы болады:
Осы себепті аминдер аммиак сияқты негізгі қасиеттерді айтарлықтай көрсетті.
Осылайша, аммиакқа ұқсас аминдер сумен қайтымды әрекеттесіп, әлсіз негіздер түзеді:
Амин молекуласындағы сутегі катионы мен азот атомы арасындағы байланыс азот атомының жалғыз электрон жұбының арқасында донор-акцепторлық механизм арқылы жүзеге асады. Қаныққан аминдер аммиакпен салыстырғанда күшті негіздер, өйткені мұндай аминдерде көмірсутекті алмастырғыштар оң индуктивті (+I) әсер етеді. Осыған байланысты азот атомындағы электрон тығыздығы артады, бұл оның Н+ катионымен әрекеттесуін жеңілдетеді.
Хош иісті аминдер, егер амин тобы ароматты сақинамен тікелей байланысқан болса, аммиакпен салыстырғанда әлсіз негіздік қасиеттерді көрсетеді. Бұл азот атомының жалғыз электрон жұбы бензол сақинасының ароматты π-жүйесіне қарай ығысады, соның нәтижесінде азот атомындағы электрон тығыздығы төмендейді. Бұл өз кезегінде негізгі қасиеттердің, атап айтқанда сумен әрекеттесу қабілетінің төмендеуіне әкеледі. Мысалы, анилин тек күшті қышқылдармен әрекеттеседі, бірақ іс жүзінде сумен әрекеттеспейді.
Қаныққан аминдердің химиялық қасиеттері
Жоғарыда айтылғандай, аминдер сумен қайтымды әрекеттеседі:
Аминдердің сулы ерітінділері пайда болған негіздердің диссоциациялануына байланысты сілтілі реакцияға ие:
Қаныққан аминдер аммиакқа қарағанда сумен жақсырақ әрекеттеседі, өйткені олардың негізгі қасиеттері күштірек.
Қаныққан аминдердің негізгі қасиеттері қатарда артады.
Екінші қаныққан аминдер бірінші реттік қаныққан аминдерге қарағанда күшті негіздер, олар өз кезегінде аммиакқа қарағанда күшті негіздер. Үшінші реттік аминдердің негізгі қасиеттеріне келетін болсақ, егер біз сулы ерітінділердегі реакциялар туралы айтатын болсақ, онда үшінші реттік аминдердің негізгі қасиеттері екінші реттік аминдерге қарағанда әлдеқайда нашар, тіпті біріншілік аминдерге қарағанда біршама нашар көрінеді. Бұл амин протонациясының жылдамдығына айтарлықтай әсер ететін стерикалық кедергілерге байланысты. Басқаша айтқанда, үш орынбасар азот атомын «блоктайды» және оның H + катиондарымен әрекеттесуіне кедергі жасайды.
Қышқылдармен әрекеттесу
Бос қаныққан аминдер де, олардың судағы ерітінділері де қышқылдармен әрекеттеседі. Бұл жағдайда тұздар түзіледі:
Қаныққан аминдердің негізгі қасиеттері аммиакқа қарағанда айқынырақ болғандықтан, мұндай аминдер көмір қышқылы сияқты әлсіз қышқылдармен де әрекеттеседі:
Амин тұздары қатты заттар, суда жақсы ериді және полярлы емес органикалық еріткіштерде нашар ериді. Амин тұздарының сілтілермен әрекеттесуі сілтілер аммоний тұздарына әсер еткенде аммиактың ығысуына ұқсас бос аминдердің бөлінуіне әкеледі:
2. Алғашқы қаныққан аминдер азот қышқылымен әрекеттесіп, сәйкес спирттер, азот N2 және су түзеді. Мысалы:
Тән ерекшелігіБұл реакция азот газының түзілуі болып табылады, сондықтан ол біріншілік аминдер үшін сапалы болып табылады және оларды екінші және үшінші реттік аминдерден айыру үшін қолданылады. Айта кету керек, көбінесе бұл реакция аминді азот қышқылының ерітіндісімен емес, азот қышқылының (нитрит) тұзының ерітіндісімен араластырып, содан кейін осы қоспаға күшті минералды қышқылды қосу арқылы жүзеге асырылады. Нитриттер күшті минералды қышқылдармен әрекеттескенде, азот қышқылы түзіледі, содан кейін ол аминмен әрекеттеседі:
Екіншілік аминдер береді ұқсас жағдайлармайлы сұйықтықтар, N-нитрозаминдер деп аталады, бірақ бұл реакция нақты тапсырмаларХимиядан Бірыңғай мемлекеттік емтихан жоқ. Үшінші реттік аминдер азот қышқылымен әрекеттеспейді.
Кез келген аминдердің толық жануы көмірқышқыл газының, судың және азоттың түзілуіне әкеледі:
Галоалкандармен әрекеттесу
Бір қызығы, дәл сол тұзды хлорсутектің неғұрлым алмастырылған аминге әсер етуінен алады. Біздің жағдайда хлорсутек диметиламинмен әрекеттескенде:
Аминдерді дайындау:
1) Аммиактың галогеналкандармен алкилденуі:
Аммиак тапшылығы кезінде оның тұзы амин орнына алынады:
2) Қышқыл ортада металдармен тотықсыздану (белсенділік қатарындағы сутегі):
бос аминді босату үшін ерітіндіні сілтімен өңдеуден кейін:
3) Аммиактың спирттермен олардың қоспасын қыздырылған алюминий оксидінен өткізгенде реакциясы. Алкоголь/амин пропорцияларына байланысты біріншілік, екіншілік немесе үшінші реттік аминдер түзіледі:
Анилиннің химиялық қасиеттері
Анилин – тривиальды атауФормуласы бар аминобензол:
Суреттен көрініп тұрғандай, анилин молекуласында амин тобы ароматты сақинамен тікелей байланысқан. Мұндай аминдер, жоғарыда айтылғандай, аммиакқа қарағанда әлдеқайда аз негізгі қасиеттерге ие. Осылайша, атап айтқанда, анилин іс жүзінде сумен және көмір қышқылы сияқты әлсіз қышқылдармен әрекеттеспейді.
Анилиннің қышқылдармен әрекеттесуі
Анилин күшті және орташа күшті бейорганикалық қышқылдармен әрекеттеседі. Бұл жағдайда фениламмоний тұздары түзіледі:
Анилиннің галогендермен әрекеттесуі
Осы тараудың ең басында айтылғандай, ароматты аминдердегі амин тобы ароматты сақинаға тартылады, бұл өз кезегінде азот атомындағы электрон тығыздығын төмендетеді, нәтижесінде оны ароматты сақинада арттырады. Ароматты сақинадағы электрон тығыздығының артуы электрофильді орын басу реакцияларының, атап айтқанда галогендермен реакциялардың, әсіресе амин тобына қатысты орто және пара позицияларында әлдеқайда жеңіл жүруіне әкеледі. Осылайша, анилин бром суымен оңай әрекеттесіп, 2,4,6-трибромоанилиннің ақ тұнбасын түзеді:
Бұл реакция анилин үшін сапалы болып табылады және көбінесе оны басқалармен бірге анықтауға мүмкіндік береді органикалық қосылыстар.
Анилиннің азот қышқылымен әрекеттесуі
Анилин азот қышқылымен әрекеттеседі, бірақ бұл реакцияның ерекшелігі мен күрделілігіне байланысты ол химиядан нақты Бірыңғай мемлекеттік емтиханда көрінбейді.
Анилинді алкилдеу реакциялары
Азот атомындағы анилинді галогенді көмірсутектермен дәйекті алкилдеу арқылы екіншілік және үшінші реттік аминдерді алуға болады:
Анилинді алу
1. Күшті тотықтырмайтын қышқылдар қатысында нитробензолды металдармен тотықсыздандыру:
C 6 H 5 -NO 2 + 3Fe + 7HCl = +Cl- + 3FeCl 2 + 2H 2 O
Cl - + NaOH = C 6 H 5 -NH 2 + NaCl + H 2 O
Белсенділік қатарында сутектен бұрын орналасқан кез келген металдарды металдар ретінде пайдалануға болады.
Хлорбензолдың аммиакпен әрекеттесуі:
C 6 H 5 −Cl + 2NH 3 → C 6 H 5 NH 2 + NH 4 Cl
Аминқышқылдарының химиялық қасиеттері
Амин қышқылдары молекулаларында функционалдық топтардың екі түрі - амин (-NH 2) және карбокси- (-COOH) топтары бар қосылыстар.
Басқаша айтқанда, аминқышқылдарын карбон қышқылдарының туындылары ретінде қарастыруға болады, олардың молекулаларында бір немесе бірнеше сутегі атомдары амин топтарымен ауыстырылады.
Осылайша, жалпы формулаамин қышқылдарын (NH 2) x R(COOH) y түрінде жазуға болады, мұнда x пен у көбінесе бір немесе екіге тең.
Амин қышқылдарының молекулаларында амин тобы да, карбоксил тобы да бар болғандықтан, олар көрсетеді Химиялық қасиеттеріаминдер мен карбон қышқылдарына ұқсас.
Амин қышқылдарының қышқылдық қасиеттері
Сілтілермен және сілтілік металдар карбонаттарымен тұздардың түзілуі
Амин қышқылдарының эфирленуі
Аминқышқылдары спирттермен этерификациямен әрекеттесе алады:
NH 2 CH 2 COOH + CH 3 OH → NH 2 CH 2 COOCH 3 + H 2 O
Амин қышқылдарының негізгі қасиеттері
1. Қышқылдармен әрекеттескенде тұздардың түзілуі
NH 2 CH 2 COOH + HCl → + Cl —
2. Азот қышқылымен әрекеттесу
NH 2 -CH 2 -COOH + HNO 2 → HO-CH 2 -COOH + N 2 + H 2 O
Ескерту: азот қышқылымен әрекеттесу бастапқы аминдермен бірдей жүреді
3. Алкилдену
NH 2 CH 2 COOH + CH 3 I → + I —
4. Амин қышқылдарының бір-бірімен әрекеттесуі
Амин қышқылдары бір-бірімен әрекеттесіп, пептидтер түзе алады - олардың молекулаларында C(O)-NH- пептидтік байланысы бар қосылыстар.
Бұл ретте екі түрлі аминқышқылдары арасында реакция болған жағдайда синтездің кейбір ерекше жағдайларын сақтамай, әртүрлі дипептидтердің түзілуі қатар жүретінін атап өткен жөн. Мысалы, глициннің аланинмен жоғарыдағы реакциясының орнына глицилананинге әкелетін реакция аланилглицинге әкелуі мүмкін:
Сонымен қатар, глицин молекуласы аланин молекуласымен міндетті түрде әрекеттеспейді. Пептизация реакциялары глицин молекулалары арасында да жүреді:
Ал аланин:
Сонымен қатар, пайда болған пептидтердің молекулаларында бастапқы аминқышқылдарының молекулалары сияқты амин топтары мен карбоксил топтары болғандықтан, пептидтердің өзі жаңа пептидтік байланыстардың түзілуіне байланысты аминқышқылдарымен және басқа пептидтермен әрекеттесе алады.
Жеке аминқышқылдары синтетикалық полипептидтерді немесе полиамидті талшықтар деп аталатындарды алу үшін қолданылады. Осылайша, атап айтқанда, 6-аминогексан (ε-аминокапрон) қышқылының поликонденсациясын қолдана отырып, нейлон өнеркәсіпте синтезделеді:
Алынған нейлон шайыры тоқыма талшықтары мен пластмассаларды өндіру үшін қолданылады.
Су ерітіндісінде аминқышқылдарының ішкі тұздарының түзілуі
Су ерітінділерінде аминқышқылдары негізінен ішкі тұздар – биполярлы иондар (цвиттериондар) түрінде болады:
Амин қышқылдарын алу
1) Хлорлы карбон қышқылдарының аммиакпен әрекеттесуі:
Cl-CH 2 -COOH + 2NH 3 = NH 2 -CH 2 -COOH + NH 4 Cl
2) Күшті минералды қышқылдар мен сілтілер ерітінділерінің әсерінен белоктардың ыдырауы (гидролизі).
Аминдер- молекуласында бір, екі немесе барлық үш сутегі атомдары көміртегі қалдығымен ауыстырылатын аммиактың органикалық туындылары.
Әдетте аминдердің үш түрі бар:
Амин тобы ароматты сақинамен тікелей байланысқан аминдер ароматты аминдер деп аталады.
Бұл қосылыстардың ең қарапайым өкілі - аминобензол немесе анилин:

Негізгі айрықша ерекшелігі электрондық құрылымаминдер – функционалдық топқа кіретін азот атомында жалғыз электрон жұбының болуы. Бұл аминдердің негіздердің қасиеттерін көрсетуіне әкеледі.
Аммоний ионындағы барлық сутегі атомдарының көмірсутек радикалымен формальды алмасуының туындысы болып табылатын иондар бар:

Бұл иондар аммоний тұздарына ұқсас тұздарда кездеседі. Оларды төрттік аммоний тұздары деп атайды.
Аминдердің изомериясы және номенклатурасы
1. Аминдерге құрылымдық изомерия тән:
A) Көміртек қаңқасының изомериясы:

б) функционалдық топ позициясының изомериясы:
2. Біріншілік, екіншілік және үшінші реттік аминдер бір-біріне изомерлі (классаралық изомерия):

Келтірілген мысалдардан көрініп тұрғандай, аминді атау үшін азот атомымен байланысты орынбасарлар тізімделеді (басымдық ретімен) және жұрнақ қосылады - амин.
Аминдердің физикалық қасиеттері
Ең қарапайым аминдер (метиламин, диметиламин, триметиламин) - газ тәрізді заттар. Қалған төменгі аминдер суда жақсы еритін сұйықтықтар. Олардың аммиакты еске түсіретін тән иісі бар.
Біріншілік және екіншілік аминдер сутектік байланыс түзуге қабілетті. Бұл молекулалық массасы бірдей, бірақ сутегі байланысын құра алмайтын қосылыстармен салыстырғанда олардың қайнау температураларының айтарлықтай жоғарылауына әкеледі.
Анилин - суда аз еритін, 184 °С температурада қайнайтын майлы сұйықтық.
Аминдердің химиялық қасиеттері
Аминдердің химиялық қасиеттері негізінен азот атомында жалғыз электрон жұбының болуымен анықталады.
Негіз ретінде аминдер.Аммиак молекуласындағы азот атомы сияқты амин тобының азот атомы электрондардың жалғыз жұбына байланысты түзілуі мүмкін. коваленттік байланысдонор ретінде әрекет ететін донор-акцепторлық механизм бойынша. Осыған байланысты аминдер аммиак сияқты сутегі катионын қосуға қабілетті, яғни негіз ретінде әрекет етеді:

1. Амиондардың сумен әрекеттесуігидроксид иондарының түзілуіне әкеледі:
2. Қышқылдармен әрекеттесу. Аммиак қышқылдармен әрекеттесіп аммоний тұздарын түзеді. Аминдер қышқылдармен де әрекеттеседі:

Алифаттық аминдердің негізгі қасиеттері аммиакқа қарағанда айқынырақ. Бұл оң индуктивті әсері азот атомындағы электрон тығыздығын арттыратын бір немесе бірнеше донор алкил алмастырғыштарының болуына байланысты. Электрондық тығыздықтың жоғарылауы азотты күшті электронды жұп донорына айналдырады, бұл оның негізгі қасиеттерін жақсартады:

Амионның жануы. Аминдер ауада жанып, көмірқышқыл газы, су және азот түзеді:
Аминдердің қолданылуы
Аминдер препараттар мен полимерлі материалдарды алу үшін кеңінен қолданылады. Анилин - бұл анилинді бояғыштарды, препараттарды (сульфаниламидті препараттар) және полимерлі материалдарды (анилин формальдегидті шайырлар) өндіру үшін қолданылатын осы кластың ең маңызды қосылысы.



АМИНДЕР- бір, екі немесе үш сутегі атомы органикалық топтармен ауыстырылатын аммиактың органикалық туындылары болып табылатын қосылыстар класы. Айырықша ерекшелігі - R–N фрагментінің болуы<, где R – органическая группа.
Аминдердің жіктелуі алуан түрлі және қандай құрылымдық белгі негізге алынғанымен анықталады.
Азот атомымен байланысқан органикалық топтардың санына байланысты:
біріншілік аминдер – RNH2 азотындағы бір органикалық топ
екінші реттік аминдер – R2NH азотындағы екі органикалық топ, органикалық топтар әртүрлі R"R"NH болуы мүмкін.
үшінші реттік аминдер - R3N немесе R"R"R""N азотындағы үш органикалық топ
Азотпен байланысты органикалық топтың түріне қарай алифатты СH3 – N бөлінеді.< и ароматические С 6 H5 – N< амины, возможны и смешанные варианты.
Молекуладағы амин топтарының санына қарай аминдер моноаминдер СН3 - NH2, диаминдер H2N(CH2) 2 NH2, триаминдер және т.б.
Аминдердің химиялық қасиеттері.Аминдердің айырықша қабілеті бейтарап молекулаларды (мысалы, бейорганикалық химиядағы аммоний тұздарына ұқсас аммоорганикалық тұздардың түзілуімен, HHal галогенсутектері. Жаңа байланыс түзу үшін азот донор рөлін атқаратын жалғыз электрон жұбын қамтамасыз етеді. Байланыстың түзілуіне қатысатын Н + протоны (галогенсутектен) акцептор (қабылдағыш) рөлін атқарады, мұндай байланыс донор-акцептор деп аталады (1-сурет).Алынған коваленттік N–H байланысы. аминде бар байланыстарға толығымен эквивалентті
Үшінші реттік аминдер де HCl қосады, бірақ алынған тұзды қышқыл ерітіндісінде қыздырғанда ол ыдырайды, ал R N атомынан бөлінеді:
(C 2 H 5) 3 Н+ HCl [(C 2 H 5) 3 Н H]Cl
[(C 2 H 5) 3 Н H]Cl (C 2 H 5) 2 Н H + C 2 H 5 Cl
Осы екі реакцияны салыстырған кезде C2H5 тобы мен Н орнын ауыстыратын сияқты екені анық, нәтижесінде үшінші реттік аминден екінші реттік амин түзіледі.
Суда еріген аминдер протонды дәл осылай ұстайды, нәтижесінде ерітіндіде OH – иондары пайда болады, бұл сілтілі ортаның түзілуіне сәйкес келеді, оны әдеттегі индикаторлар арқылы анықтауға болады.
C2H5 Н H2 + H2O + + OH–
Донор-акцепторлық байланыстың түзілуімен аминдер тек HCl емес, сонымен қатар галоалкил RCl қоса алады, осылайша жаңа N–R байланысын түзеді, ол да барларға тең. Егер бастапқы зат ретінде үшінші реттік аминді алсақ, тетраалкиламмоний тұзын аламыз (бір N атомында төрт R тобы):
(C 2 H 5) 3 Н+ C 2 H 5 I [(C 2 H 5) 4 Н]Мен
Бұл тұздар суда және кейбір органикалық еріткіштерде ери отырып, диссоциацияланады (ыдырайды), иондар түзеді:
[(C2H5) 4 Н]I [(C2H5) 4 Н] + + I–
Мұндай ерітінділер, құрамында иондары бар барлық ерітінділер сияқты, электр тогын өткізеді. Тетраалкиламмоний тұздарында галогенді HO тобымен ауыстыруға болады:
[(CH 3) 4 Н]Cl + AgOH [(CH 3) 4 Н]OH + AgCl
Алынған тетраметиламмоний гидроксиді сілтілерге ұқсас қасиеттері бар күшті негіз болып табылады.
Біріншілік және екіншілік аминдер азот қышқылымен HON=O әрекеттеседі, бірақ олар әртүрлі жолмен әрекеттеседі. Біріншілік спирттер біріншілік аминдерден түзіледі:
C2H5 Н H2+H Н O2 C2H5OH + Н 2 +H2O
Біріншілік аминдерден айырмашылығы, қайталама аминдер азот қышқылымен сары түсті нашар еритін нитрозаминдер түзеді - құрамында >N–N = O фрагменті бар қосылыстар:
(C 2 H 5) 2 Н H+H Н O 2 (C 2 H 5) 2 Н–Н=O + H2O
Үшінші реттік аминдер қарапайым температурада азот қышқылымен әрекеттеспейді, сондықтан азот қышқылы біріншілік, екіншілік және үшінші реттік аминдерді ажыратуға мүмкіндік беретін реагент болып табылады.
Аминдер конденсацияланған кезде карбон қышқылдарықышқыл амидтер түзіледі - C(O)N фрагменті бар қосылыстар< (рис. 2А). Если в качестве исходных соединений взять диамин и дикарбоновую кислоту (соединения, содержащие соответственно две амино- и две карбоксильные группы, соответственно), то они взаимодействуют по такой же схеме, но поскольку каждое соединение содержит две реагирующие группы, то образуется полимерная цепь, содержащая амидные группы (рис. 2Б). Такие полимеры называют полиамидами.
Аминдердің альдегидтермен және кетондармен конденсациясы Шифф негіздері деп аталатындардың түзілуіне әкеледі – құрамында –N=C фрагменті бар қосылыстар.< (рис. 2В). На схеме В видно, что для образования двойной связи между N и С азот должен предоставить два атома Н (для образования конденсационной воды), следовательно, в такой реакции могут участвовать только первичные амины RNH2.
Біріншілік аминдер Cl2C=O фосгенімен әрекеттескенде изоцианаттар деп аталатын –N=C=O тобы бар қосылыстар түзіледі (2Д-сурет, екі изоцианат тобы бар қосылыс алу).

Ароматты аминдердің ішінде ең танымалы анилин (фениламин) C 6 H 5 NH 2. Оның қасиеттері алифатты аминдерге ұқсас, бірақ оның негізділігі азырақ - сулы ерітінділерде сілтілі орта түзбейді. Алифатты аминдер сияқты күшті минералды қышқылдармен аммоний тұздарын [C 6 H 5 NH 3 ] + Cl– түзе алады. Анилин азот қышқылымен (HCl қатысында) әрекеттескенде R–N=N фрагменті бар диазоқосылыс түзіледі, ол диазоний тұзы деп аталатын иондық тұз түрінде алынады (3А-сурет). Сонымен, азот қышқылымен әрекеттесу алифатты аминдердегідей жүрмейді. Анилиндегі бензол сақинасы хош иісті қосылыстарға тән реактивтілікке ие (АРОМАТТЫЛЫҚ бөлімін қараңыз), галогендеу кезінде амин тобына орто және пара позициялардағы сутегі атомдары ауыстырылады, нәтижесінде әртүрлі дәрежедегі алмастырулары бар хлоранилиндер пайда болады (3В-сурет). Күкірт қышқылының әрекеті пара позицияда амин тобына сульфалануға әкеледі, сульфанил қышқылы деп аталатын зат түзіледі (3В-сурет).

Аммиак туындылары болғандықтан, аминдер оған ұқсас құрылымға ие болғандықтан (яғни, олардың азот атомында жалғыз жұп электрондары бар), олар оған ұқсас қасиеттер көрсетеді. Анау. аминдер, аммиак сияқты, негіз болып табылады, өйткені азот атомы донор-акцепторлық механизм арқылы электрон тапшылығы бар түрлермен байланыстар құру үшін электрон жұбын қамтамасыз ете алады (Льюистің негіздік анықтамасына сәйкес).
I. Аминдердің негіз ретіндегі қасиеттері (протон акцепторлары)
1. Алифаттық аминдердің сулы ерітінділері сілтілі реакция көрсетеді, өйткені олар сумен әрекеттескенде аммоний гидроксидіне ұқсас алкил аммоний гидроксидтері түзіледі:
CH 3 NH 2 + H 2 O CH 3 NH 3 + + OH −


Анилин іс жүзінде сумен әрекеттеспейді.
Сулы ерітінділер сілтілі болып табылады:
Аммиак сияқты аминмен протондық байланыс азот атомының жалғыз электрон жұбының арқасында донор-акцепторлық механизм арқылы түзіледі.
Алифаттық аминдер аммиакқа қарағанда күшті негіздер, өйткені алкил радикалдары + есебінен азот атомындағы электрон тығыздығын арттырады I-әсер. Осы себепті азот атомының электронды жұбы азырақ тығыз ұсталады және протонмен оңай әрекеттеседі.
2. Аминдер қышқылдармен әрекеттесе отырып, тұздар түзеді:
C 6 H 5 NH 2 + HCl → (C 6 H 5 NH 3) Cl
фениламмоний хлориді

2CH 3 NH 2 + H 2 SO 4 → (CH 3 NH 3) 2 SO 4
метил аммоний сульфаты
Амин тұздары суда жақсы еритін және полярлы емес сұйықтықтарда нашар еритін қатты заттар. Сілтілермен әрекеттескенде бос аминдер бөлінеді:
Хош иісті аминдер аммиакқа қарағанда әлсіз негіздер болып табылады, өйткені азот атомының жалғыз электронды жұбы бензол сақинасына қарай ығысады, ароматты сақинаның π электрондарымен конъюгацияланады, бұл азот атомындағы электрон тығыздығын төмендетеді (-M эффектісі). Керісінше, алкил тобы электронды тығыздықтың жақсы доноры болып табылады (+I-эффект).
 немесе
немесе 

Азот атомындағы электрон тығыздығының төмендеуі әлсіз қышқылдардан протондарды алу қабілетінің төмендеуіне әкеледі. Сондықтан анилин тек күшті қышқылдармен (HCl, H 2 SO 4) әрекеттеседі, ал оның судағы ерітіндісі лакмусты боямайды. Көк түс.
Амин молекулаларындағы азот атомында донор-акцепторлық механизм бойынша байланыс түзуге қатыса алатын жалғыз жұп электрондар болады.
анилин аммиак біріншілік амин екінші амин үшінші реттік амин
азот атомындағы электрон тығыздығы артады.
Молекулаларда жалғыз электрон жұбының болуына байланысты аминдер аммиак сияқты негізгі қасиеттерді көрсетеді.
анилин аммиак біріншілік амин екіншілік амин
негізгі қасиеттері радикалдардың түрі мен санының әсерінен күшейеді.
C6H5NH2< NH 3 < RNH 2 < R 2 NH < R 3 N (в газовой фазе)
II. Амин тотығуы
Аминдер, әсіресе хош иісті заттар ауада оңай тотығады. Аммиактан айырмашылығы олар ашық жалыннан тұтануы мүмкін. Ароматты аминдер ауада өздігінен тотығады. Осылайша, анилин тотығу әсерінен ауада тез қоңыр түске айналады.
4СH 3 NH 2 + 9O 2 → 4CO 2 + 10H 2 O + 2N 2
4C 6 H 5 NH 2 + 31O 2 → 24CO 2 + 14H 2 O + 2N 2
III. Азот қышқылымен әрекеттесу
Азот қышқылы HNO 2 – тұрақсыз қосылыс. Сондықтан ол таңдау кезінде ғана қолданылады. HNO 2 барлық әлсіз қышқылдар сияқты оның тұзының (нитрит) әсерінен түзіледі. күшті қышқыл:
KNO 2 + HCl → HNO 2 + KCl
немесе NO 2 − + H + → HNO 2
Азот қышқылымен реакция өнімдерінің құрылымы амин табиғатына байланысты. Сондықтан бұл реакция біріншілік, екіншілік және үшінші реттік аминдерді ажырату үшін қолданылады.
· Біріншілік алифатты аминдер HNO 2 бар спирттер түзеді:
R-NH 2 + HNO 2 → R-OH + N 2 + H 2 O
- Натрий нитритінің азот қышқылының әсерінен бастапқы ароматты аминдерді диазотизациялау реакциясы үлкен маңызға ие. тұз қышқылы. Ал кейіннен фенол түзіледі:


· HNO 2 әсерінен екінші ретті аминдер (алифатты және ароматты) N-нитрозотуындыларына (өзіне тән иісі бар заттар) айналады:
R 2 NH + H-O-N=O → R 2 N-N=O + H 2 O
алкилнитрозамин
· Үшінші реттік аминдермен әрекеттесу тұрақсыз тұздардың түзілуіне әкеледі және практикалық маңызы жоқ.
IV. Арнайы қасиеттері:
1. Өтпелі металдармен комплексті қосылыстардың түзілуі:
2. Алкилгалогенидтердің қосылуы Аминдер галогеналкандарды қосып, тұз түзеді:

Алынған тұзды сілтімен өңдеу арқылы бос аминді алуға болады:

V. Ароматты аминдердегі ароматты электрофильді орынбасу (анилиннің бром суымен реакциясы немесе азот қышқылы):
Ароматты аминдерде амин тобы бензол сақинасының орто және пара позицияларында орын басуды жеңілдетеді. Сондықтан анилиннің галогенденуі катализаторларсыз тез жүреді де, бензол сақинасының үш сутегі атомы бірден ауыстырылады да, 2,4,6-трибромоанилиннің ақ тұнбасы түзіледі:

Бром суымен бұл реакция анилин үшін сапалық реакция ретінде қолданылады.
Бұл реакциялар (бромдау және нитрлеу) негізінен түзеді орто- Және жұп- туындылар.
4. Аминдерді алу әдістері.
1. Гоффман реакциясы. Біріншілік аминдерді алудың алғашқы әдістерінің бірі аммиакты алкилгалогенидтермен алкилдеу болды:
Бұл ең жақсы әдіс емес, өйткені нәтиже барлық алмастыру дәрежесіндегі аминдердің қоспасы болып табылады:
және т.б. Алкилирлеуші ретінде тек алкилгалогенидтер ғана емес, сонымен қатар спирттер де әрекет ете алады. Ол үшін аммиак пен спирт қоспасын жоғары температурада алюминий оксидінің үстінен өткізеді.
2. Зинин реакциясы- ароматты нитроқосылыстарды қалпына келтіру арқылы ароматты аминдерді алудың ыңғайлы тәсілі. Тотықсыздандырғыш ретінде мыналар қолданылады: H 2 (катализаторда). Кейде сутегі реакция кезінде тікелей түзіледі, ол үшін металдар (мырыш, темір) сұйылтылған қышқылмен өңделеді.

2HCl + Fe (чиптер) → FeCl 2 + 2H
C 6 H 5 NO 2 + 6[H] C 6 H 5 NH 2 + 2H 2 O.
Өнеркәсіпте бұл реакция нитробензолды темірдің қатысуымен бумен қыздырғанда жүреді. Зертханада сутегі «шығару сәтінде» мырыштың сілтімен немесе темірдің тұз қышқылымен әрекеттесуі нәтижесінде түзіледі. Соңғы жағдайда анилиний хлориді түзіледі.
3. Нитрилдердің азаюы. LiAlH 4 пайдаланыңыз:
4. Амин қышқылдарының ферментативті декарбоксилденуі:

5. Аминдердің қолданылуы.
Аминдер фармацевтика өнеркәсібінде және органикалық синтезде қолданылады (CH 3 NH 2, (CH 3) 2 NH, (C 2 H 5) 2 NH, т.б.); нейлон өндірісінде (NH 2 -(CH 2) 6 -NH 2 - гексаметилендиамин); бояғыштар мен пластмассаларды (анилин), сонымен қатар пестицидтерді өндіру үшін шикізат ретінде.
Пайдаланылған көздер тізімі:
- О.С. Габриелян және басқалар Химия. 10-сынып. Профиль деңгейі: жалпы білім беретін оқу орындарына арналған оқулық; Бустард, Мәскеу, 2005;
- А.С.Егоровтың редакциясымен «Химия пәнінің мұғалімі»; «Феникс», Ростов-на-Дону, 2006 ж.;
- Г.Е.Рудзитис, Ф.Г.Фельдман. Химия 10 сынып. М., Білім, 2001;
- https://www.calc.ru/Aminy-Svoystva-Aminov.html
- http://www.yaklass.ru/materiali?mode=lsntheme&themeid=144
- http://www.chemel.ru/2008-05-24-19-21-00/2008-06-01-16-50-05/193-2008-06-30-20-47-29.html
- http://cnit.ssau.ru/organics/chem5/n232.htm
Аминдер біздің өмірімізге күтпеген жерден келді. Соңғы уақытқа дейін бұл улы заттар болды, соқтығысуы өлімге әкелуі мүмкін. Ал енді, бір жарым ғасырдан кейін біз синтетикалық талшықтарды, маталарды, құрылыс материалдарын, амин негізіндегі бояуларды белсенді қолданамыз. Жоқ, олар қауіпсіз бола алмады, адамдар өздері үшін белгілі бір артықшылықтарды ала отырып, оларды «үйретіп», бағындыра алды. Қайсысы туралы әрі қарай сөйлесеміз.
Анықтама
Ерітінділердегі немесе қосылыстардағы анилинді сапалық және сандық анықтау үшін реакция қолданылады, оның соңында пробирка түбіне 2,4,6-трибромоанилин түріндегі ақ тұнба түседі.
Табиғаттағы аминдер
Аминдер табиғаттың барлық жерінде витаминдер, гормондар және аралық зат алмасу өнімдері түрінде кездеседі, олар жануарлардың денесінде де, өсімдіктерде де кездеседі. Сонымен қатар, тірі ағзалардың ыдырауы сұйық күйде майшабақ тұзды ерітіндісінің жағымсыз иісін шығаратын орташа аминдерді де шығарады. Әдебиетте кеңінен сипатталған «жансыз улану» дәл аминдердің нақты кәріптастарының арқасында пайда болды.
Ұзақ уақыт бойы біз қарастырып жатқан заттар ұқсас иіске байланысты аммиакпен шатастырылды. Бірақ он тоғызыншы ғасырдың ортасында француз химигі Вурц метиламин мен этиламинді синтездеп, жанған кезде көмірсутектерді бөлетінін дәлелдей алды. Бұл аталған қосылыстар мен аммиак арасындағы негізгі айырмашылық болды.
Өндірістік жағдайларда аминдерді өндіру
Аминдердегі азот атомы ең төменгі тотығу күйінде болғандықтан, құрамында азот бар қосылыстарды қалпына келтіру оларды алудың ең қарапайым және қол жетімді әдісі болып табылады. Бұл кең тараған өндірістік тәжірибеарзандығынан.
Бірінші әдіс - нитроқосылыстарды қалпына келтіру. Анилин түзілетін реакцияны ғалым Зинин атаған және алғаш рет ХІХ ғасырдың ортасында жүргізген. Екінші әдіс - литий алюминий гидридінің көмегімен амидтерді азайту. Бастапқы аминдерді нитрилдерден де алуға болады. Үшінші нұсқа – алкилдену реакциялары, яғни аммиак молекулаларына алкил топтарын енгізу.
Аминдердің қолданылуы

Өздігінен, таза заттар түрінде аминдер сирек қолданылады. Сирек мысалдардың бірі - тұрмыстық жағдайда эпоксидті шайырдың қатаюын жеңілдететін полиэтиленді полиамин (PEPA). Негізінде біріншілік, үшіншілік немесе екіншілік амин әртүрлі өндірістегі аралық өнім болып табылады органикалық заттар. Ең танымал - анилин. Ол анилиндік бояғыштардың үлкен палитрасының негізі болып табылады. Соңында алынған түс тікелей таңдалған шикізатқа байланысты. Таза анилин көк түс береді, бірақ анилин, орто- және пара-толуидин қоспасы қызыл болады.
Алифатты аминдер нейлон және басқалар сияқты полиамидтерді алу үшін қажет.Олар машина жасауда, сонымен қатар арқан, маталар және пленка өндірісінде қолданылады. Сонымен қатар, алифатты диизоцианаттар полиуретандар өндірісінде қолданылады. Ерекше қасиеттеріне байланысты (жеңілдік, беріктік, икемділік және кез келген бетке жабысу мүмкіндігі) олар құрылыста (көбік, желім) және аяқ киім өнеркәсібінде (тайғаққа қарсы табан) сұранысқа ие.
Медицина - аминдер қолданылатын тағы бір сала. Химия олардан сульфаниламидтер тобынан антибиотиктерді синтездеуге көмектеседі, олар екінші қатардағы препараттар ретінде сәтті қолданылады, яғни резервтік. Бактериялар маңызды препараттарға төзімділік танытқан жағдайда.
Адам ағзасына зиянды әсерлері
Аминдер өте улы заттар екені белгілі. Олармен кез келген өзара әрекеттесу денсаулыққа зиян келтіруі мүмкін: буларды ингаляциялау, ашық теріге тию немесе денеге қосылыстарды жұту. Өлім оттегінің жетіспеушілігінен болады, өйткені аминдер (атап айтқанда, анилин) қандағы гемоглобинмен байланысып, оның оттегі молекулаларын ұстауына жол бермейді. Дабыл белгілері - ентігу, мұрын-ерін үшбұрышының және саусақ ұштарының көк түске боялуы, тахипноэ (тез тыныс алу), тахикардия, сананың жоғалуы.
Егер бұл заттар дененің жалаңаш жерлеріне түссе, оларды бұрын спиртке малынған мақтамен тез жою керек. Бұл ластану аймағын арттырмау үшін мүмкіндігінше мұқият жасалуы керек. Егер улану белгілері пайда болса, сіз міндетті түрде дәрігермен кеңесуіңіз керек.
Алифаттық аминдер жүйке және жүрек-тамыр жүйесі үшін улану болып табылады. Олар бауыр функциясының төмендеуіне, бауыр дистрофиясына және тіпті қуықтың қатерлі ісігіне әкелуі мүмкін.
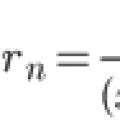 Тейлор қатарын кеңейту. Кәдімгі үшін Коши есебінің шамамен шешімі
Тейлор қатарын кеңейту. Кәдімгі үшін Коши есебінің шамамен шешімі Мектепте не ОҚЫТЫЛМАЙДЫ Мектепте нені оқытпайды деп сұраңыз
Мектепте не ОҚЫТЫЛМАЙДЫ Мектепте нені оқытпайды деп сұраңыз Ақшаны ойлау формуласы (А
Ақшаны ойлау формуласы (А