آیا چربی ها در آب محلول هستند؟ چربی های نامحلول در آب عملکرد انرژی آنها جزء ساختاری اصلی غشاهای بیولوژیکی هستند
بدن ما یاد گرفته است که تمام اجزای اصلی تغذیه را در ذخیره ذخیره کند.- بله، برای هر موردی. قند را در کبد، پروتئین ها را در معده ذخیره می کند، اما محلی که برای چربی ها انتخاب می شود، زیر پوست است. آیا می خواهید لاغر شوید؟ ما باید با بدن خود به جنگ برویم! برای پیروزی باید ماهرانه بجنگید. این مقاله چیزهای زیادی به شما یاد خواهد داد!
چربی ها... چیست؟ آنها از کجا می آیند؟ چرا زیر پوست رسوب می کنند؟ و به طور کلی، چرا آنها مورد نیاز هستند؟ یا شاید نباید آنها را خورد؟ منطقی به نظر می رسد، زیرا چربی باعث ایجاد مشکلات زیادی در بدن ما می شود!
مرحله اول تبدیل چربی: خوردنهمه چیز روشن است: ما سر میز نشستیم و غذا را بار کردیم. بنابراین، "فرآوری" چربی ها توسط بدن در دهان شما آغاز می شود، زمانی که غدد بزاقی بزاق اشباع شده با آنزیم های گوارشی خاص را ترشح می کنند. بعد، به نظر می رسد، معده باید در این کار بپیوندد. به اندازه کافی عجیب، چربی ها مشخصات او نیستند. بنابراین او به سادگی آنها را از خود عبور می دهد و آنها را بیشتر به روده می فرستد. و در اینجا چربی ها هضم و جذب خون می شوند. به هر حال، چرا ما به همین چربی ها نیاز داریم؟ و آیا بهتر نیست آنها را اصلا نخورید؟
بیایید زمین را به علم بدهیم- چربی ها سوخت انرژی بدن هستند
- چربی ها به عنوان یکی از اجزای سازنده پوست، مو، ناخن ها و...
- چربی ها "مواد اولیه" برای تولید هورمون ها هستند.
چربی ها بر خلاف کربوهیدرات ها و پروتئین ها هستند زیرا در آب حل نمی شوند. معلوم می شود که آب باید با چیزی جایگزین شود، درست است؟ بدن ما صفرا را مخصوصاً به خاطر چربی ها ترشح می کند. انحلال کامل چربی ها برای او خیلی سخت است. اما او می داند که چگونه چربی ها را به قطره های میکروسکوپی - تری گلیسیرید - تقسیم کند. و روده ها می توانند با آنها کنار بیایند.
کلمه به علمتری گلیسیرید سه مولکول اسید چرب است که به یک مولکول گلیسرول "چسبانده شده" است. در روده ها، برخی از تری گلیسیریدها با پروتئین ها ترکیب می شوند و همراه با آنها، سفر خود را در بدن آغاز می کنند.
مرحله سوم تبدیل چربی: سفر
بله، تری گلیسیریدها به تنهایی نمی توانند حرکت کنند. آنها قطعاً به وسیله ای به نام "لیپوپروتئین" نیاز دارند. لیپوپروتئین ها متفاوت هستند و هر کدام وظایف خاص خود را دارند.
- شیلومیکرون ها در روده ها از چربی ها و پروتئین های حامل تشکیل می شوند. وظیفه آنها انتقال چربی به دست آمده از غذا از روده ها به بافت ها و سلول ها است.
- لیپوپروتئینهای با چگالی بسیار بالا نیز چربی را به بافتها و سلولهای مختلف منتقل میکنند، اما آن را منحصراً در کبد مصرف میکنند.
- لیپوپروتئین های کم چگالی نیز چربی ها را از کبد به بافت های بدن می رساند. تفاوت در چیست؟ و واقعیت این است که در طول مسیر، این لیپوپروتئینها کلسترول را از روده گرفته و آن را در سراسر بدن توزیع میکنند. بنابراین اگر لخته های خونی کلسترول در جایی در رگ های شما تشکیل شده است که بیماری قلبی عروقی را تهدید می کند، مقصر لیپوپروتئین های با چگالی کم هستند.
- لیپوپروتئین های با چگالی بالا یک عملکرد دارند - دقیقا برعکس. این لیپوپروتئین ها، برعکس، کلسترول را در سراسر بدن جمع آوری می کنند و آن را برای تخریب به کبد می برند. اتصالات بسیار مفید
 این جزئیات به درک این نکته کمک می کند که مصرف غذاهای چرب به طور خودکار سطح کلسترول را در بدن افزایش نمی دهد. یک وضعیت خطرناک زمانی رخ می دهد که بدن مقدار زیادی لیپوپروتئین با چگالی کم (آنهایی که به ذخیره کلسترول کمک می کنند) و لیپوپروتئین های با چگالی بالا (آنهایی که مسئول حذف کلسترول هستند) کافی نباشد. و این یک عامل کاملا ژنتیکی است. یک عامل حسابی نیز وجود دارد. این زمانی است که شما آنقدر از این کلسترول می خورید که هیچ لیپوپروتئینی برای حذف آن کافی نیست. این یک کشف علمی دیگر است. مشخص شده است که کلسترول به ویژه در چربی های حیوانی بالا است. اما چربی های گیاهی از این نظر بسیار سالم تر هستند. به نظر می رسد که ما نیاز به مصرف کمتر چربی حیوانی و بیشتر چربی های گیاهی داریم. مهم نیست که چگونه است! تأثیر مفید چربی های گیاهی فقط در یک مورد احساس می شود: اگر حیوانات را به طور کامل با آنها جایگزین کنید.
این جزئیات به درک این نکته کمک می کند که مصرف غذاهای چرب به طور خودکار سطح کلسترول را در بدن افزایش نمی دهد. یک وضعیت خطرناک زمانی رخ می دهد که بدن مقدار زیادی لیپوپروتئین با چگالی کم (آنهایی که به ذخیره کلسترول کمک می کنند) و لیپوپروتئین های با چگالی بالا (آنهایی که مسئول حذف کلسترول هستند) کافی نباشد. و این یک عامل کاملا ژنتیکی است. یک عامل حسابی نیز وجود دارد. این زمانی است که شما آنقدر از این کلسترول می خورید که هیچ لیپوپروتئینی برای حذف آن کافی نیست. این یک کشف علمی دیگر است. مشخص شده است که کلسترول به ویژه در چربی های حیوانی بالا است. اما چربی های گیاهی از این نظر بسیار سالم تر هستند. به نظر می رسد که ما نیاز به مصرف کمتر چربی حیوانی و بیشتر چربی های گیاهی داریم. مهم نیست که چگونه است! تأثیر مفید چربی های گیاهی فقط در یک مورد احساس می شود: اگر حیوانات را به طور کامل با آنها جایگزین کنید.
اگر بدن بیش از نیاز خود دریافت کند، آنزیمی به نام لیپاز وارد عمل می شود. وظیفه آن پنهان کردن هر چیزی غیر ضروری در داخل سلول های چربی است.
کلمه به علملیپاز نوعی کلید است که درهای سلول های چربی را به سمت چربی ها باز می کند. سلول های چربی می توانند مقدار زیادی چربی جذب کرده و مانند یک بادکنک متورم شوند. این دقیقاً پاسخی است که شما چاق می شوید. اگر یک سلول چربی یا حتی صد عدد افزایش یابد، هیچ کس متوجه آن نخواهد شد. با این حال، اگر بیش از حد چربی بخورید، سلول های چربی بی شماری که زیر پوست قرار دارند، به یکباره متورم می شوند. و شما نمی توانید این را از نظر پنهان کنید. علاوه بر این، لیپاز می تواند دستور تکثیر سلول های چربی را بدهد. و همچنین آنها را با چربی پر خواهد کرد. بدترین قسمت این است که سلول های چربی نمی توانند از بین بروند. هنگامی که شروع به کاهش وزن می کنید، لیپاز سلول های چربی را "باز" می کند و چربی را آزاد می کند و سپس در حین ورزش "می سوزد". شما در آینه نگاه می کنید: نه یک قطره چربی! در همین حال، تمام سلول های چربی وجود دارد، اما آنها فقط شبیه بادکنک های سوراخ شده هستند. به محض اینکه ورزش را کنار بگذارید، لیپاز دوباره شروع به پر کردن آنها با چربی می کند.
چرا اینقدر چربی وجود دارد؟بدن نه تنها چربی ها، بلکه کربوهیدرات ها را نیز ذخیره می کند. فرض کنید شما 100 کالری کربوهیدرات مصرف کرده اید. بنابراین، بدن باید تقریباً 23 کالری مصرف کند تا 77 کالری باقیمانده را ذخیره کند. اما برای صرفه جویی 100 کالری اضافی «چربی»، تنها به 3 کالری نیاز دارید. 97 کالری باقیمانده همه مال شماست! بنابراین معلوم می شود که ذخایر چربی همیشه بزرگترین هستند.
عوامل موثر در رسوب چربی در بدن:
- سن (هر چه سن شما بالاتر باشد، چربی به راحتی رسوب می کند)
- جنسیت (زنان سریعتر چربی جمع می کنند)
- پرخوری (زیاد غذا می خورید)
- سبک زندگی کم تحرک (شما به انرژی چربی نیاز ندارید)
- لیپاز اضافی (عامل وراثت)
- استرس عصبی (برخلاف تصور عمومی، استرس شما را چاق می کند)
- عادت به خوردن غذاهای چرب (ما در مورد ویژگی های غذاهای ملی صحبت می کنیم)
- عوامل ژنتیکی (وزن ارثی است).
ورزش چگونه به خلاص شدن از شر پوندهای اضافی کمک می کند؟ و مثل این. ابتدا، بدن با مصرف گلیکوژن، یک قند از پیش ذخیره شده، به ورزش واکنش نشان می دهد. و تنها پس از آن، هنگامی که او ذخایر "قند" خود را خرج می کند، رسوبات چربی وارد بازی می شوند. این تقریباً نیم ساعت پس از شروع تمرین هوازی اتفاق می افتد، یعنی. دقیقا زمانی که خیلی ها معمولا آن را تا می کنند.
تغییر شکل در مورد ژنتیک خیلی صحبت شده است! مثلاً اگر مادرت چاق بود، نمیتوانی از همان سرنوشت فرار کنی. در واقع، همه چیز چندان ترسناک نیست. ژن ها 25 درصد از ترکیب بدن شما را تعیین می کنند. فقط یک ربع! این به تعداد سلول های چربی و محل تجمع آنها (در ناحیه کمر یا باسن و باسن) مربوط می شود. بنابراین، اگر واقعاً مانند مامان هستید، به احتمال زیاد به این دلیل است که عادات غذایی مشابهی با او دارید: شما نیز مانند او پرخوری میکنید. اگر شروع به ورزش کنید و رژیم بگیرید، ظاهری کاملاً متفاوت خواهید داشت. به هر حال، نیازی به دوری از تمرینات قدرتی وجود ندارد. ماهیچه ها حالتی در یک حالت هستند. درست مانند مغز، آنها حتی در هنگام خواب نیز بیدار هستند و انرژی مصرف می کنند. هرچه عضلات شما بیشتر باشد، کالری مصرفی روزانه شما نیز بیشتر می شود. آیا از تبدیل شدن به یک بدنساز مردانه می ترسید؟ افزایش عضلانی 12-25 کیلوگرم از نظر بصری قابل توجه است. با این حال، بدنسازان چندین دهه است که این کار را انجام می دهند. انشالله که حداقل 5-8 کیلو وزن اضافه کنید!
در مورد ژنتیک خیلی صحبت شده است! مثلاً اگر مادرت چاق بود، نمیتوانی از همان سرنوشت فرار کنی. در واقع، همه چیز چندان ترسناک نیست. ژن ها 25 درصد از ترکیب بدن شما را تعیین می کنند. فقط یک ربع! این به تعداد سلول های چربی و محل تجمع آنها (در ناحیه کمر یا باسن و باسن) مربوط می شود. بنابراین، اگر واقعاً مانند مامان هستید، به احتمال زیاد به این دلیل است که عادات غذایی مشابهی با او دارید: شما نیز مانند او پرخوری میکنید. اگر شروع به ورزش کنید و رژیم بگیرید، ظاهری کاملاً متفاوت خواهید داشت. به هر حال، نیازی به دوری از تمرینات قدرتی وجود ندارد. ماهیچه ها حالتی در یک حالت هستند. درست مانند مغز، آنها حتی در هنگام خواب نیز بیدار هستند و انرژی مصرف می کنند. هرچه عضلات شما بیشتر باشد، کالری مصرفی روزانه شما نیز بیشتر می شود. آیا از تبدیل شدن به یک بدنساز مردانه می ترسید؟ افزایش عضلانی 12-25 کیلوگرم از نظر بصری قابل توجه است. با این حال، بدنسازان چندین دهه است که این کار را انجام می دهند. انشالله که حداقل 5-8 کیلو وزن اضافه کنید!
زنانی که «سیب» هستند، نسبت به زنانی که «گلابی» هستند، راحتتر چربی اضافی خود را از دست میدهند.چربی دور کمر 5 برابر بیشتر از چربی دور باسن و باسن قابل انعطاف است. اما زنان با شکل "گلابی" نیز روش های خاص خود را دارند. ابتدا باید بدانید که «سوزاندن» چربی بخشی از متابولیسم کلی شماست. این اتفاق نمی افتد که متابولیسم کند باشد و چربی به سرعت "سوزانده شود". بنابراین در اینجا اولین ترفند شما است. اغلب غذا بخورید - هر 2-2.5 ساعت، اما در بخش های کوچک. این تکنیک واقعاً سرعت متابولیسم و در نتیجه «چربی سوزی» را افزایش می دهد. دومین. ایروبیک بیشتر! همه این فعالیت های هوازی 40-45 دقیقه ای برای شما مناسب نیستند. حداقل 4-5 روز در هفته یک و نیم تا دو ساعت ایروبیک انجام دهید! و بیشتر. چربی، اکسیژن را "سوزانده". شما به ایروبیک در فضای باز نیاز دارید. فقط در هوای تازه! سوم. حتی سعی نکنید یک رژیم غذایی "سخت" کمتر از 1200 کالری داشته باشید! ثابت شده است که چنین رژیم هایی، برعکس، سرعت متابولیسم را کاهش می دهند، که به طور خودکار سرعت "چربی سوزی" را کاهش می دهد!
بدن از کجا انرژی می گیرد؟انرژی مورد نیاز برای بلند کردن هالتر یا دویدن در یک دوره متقابل می تواند از دو منبع تامین شود. اینها گلیکوژن (کربوهیدرات) و چربی هستند. بنابراین چگونه می توانید خود را مجبور به کاهش چربی بیشتر کنید؟ در اینجا دلایلی وجود دارد که بر "انتخاب" ارگانیسم تأثیر می گذارد:
- غذایی که قبل از تمرین خورده اید (اگر چیزی با کربوهیدرات بالا بخورید، مانند سالاد سبزیجات، فرنی، میوه یا شکلات، بدن نه چربی را به عنوان منبع اصلی انرژی، بلکه قند از پیش ذخیره شده - گلیکوژن را انتخاب می کند.)
- مدت زمان تمرین (هرچه بیشتر تمرین کنید، چربی بیشتری می سوزانید)
- شدت ورزش (هرچه بار بیشتر باشد، گلیکوژن بیشتری مصرف می شود)
- نوع ورزش (ایروبیک چربی بیشتری می سوزاند و وسایل ورزشی گلیکوژن بیشتری می سوزانند)
- سطح تناسب اندام (هرچه تجربه ورزشی بیشتری داشته باشید، چربی بیشتری می سوزانید)
- کربوهیدرات های مصرف شده در طول تمرین (اگر تصمیم به نوشیدن یا خوردن چیزی شیرین داشته باشید، گلیکوژن بیشتری مصرف خواهید کرد).
 02.02.2020 21:05:00 02.02.2020 21:05:00 |
"استفاده از چربی ها" - عطرسازی. غذای حیوانات. چربی ها چرا شیرینی بهتر از چرب است؟ صابون. یک فرد به چه مقدار و چه نوع چربی نیاز دارد؟ شکلات. استفاده از چربی ها شمع ها. گلیسرول. بره موم. رنگ.
"خواص و کاربرد چربی ها" - مارگارین. 600 نوع مختلف چربی شناسایی شده است. استفاده عملیدر زندگی. مخلوطی از استرها چارلز ورتز. تعیین میزان غیر اشباع چربی سنتز چربی. چربی ها تغییر رنگ آب برم مواد قلیایی. دانه های کاکائو. مخلوط. تهیه رنگ روغن. معادله واکنش هیدرولیز چربی. چربی غیر قابل خوردن
"روغن های ضروری" - فنل ها. جنگجویان یونانی زخم ها را با مرهم های ساخته شده از مرم درمان می کردند. پینن. اترها. اکسیژن عنصر اصلی اسانس است. حمام استرس. کتون ها احتقان را از بین می برند و گردش خون را تسریع می کنند. عطر سرد، تازه، تلخ است. رایحه درمانی چیست؟ از خواص درمانی نعناع 3000 سال پیش در مصر باستان استفاده می شد.
"چربی های خوراکی" - چربی های خوراکی. یک نمونه روغن گیاهی را مشخص کنید. گرایش. سوالات از قبل آماده شده است. جدول کلمات متقاطع را حل کنید. روغن خردل. انتقال بزرگترین عددنام چربی های خوراکی در مورد قوانین خرید و نگهداری روغن. اصالت کالا. محتوای کار. شطرنج. مراحل رقابت همه جانبه کالا.
"چربی های شیمی درجه 10" - چربی ها. نتیجهگیری: اسیدهای قوی، اسیدهای ضعیف را از محلولهای نمکی جابجا میکنند. استئارات سدیم. خواص کربوهیدرات to-t، شبیه به مواد معدنی، با استفاده از اسید استیک به عنوان مثال. استرها آزمایش آزمایشگاهی شماره 1 «اقدام اسیدهای قویبرای صابون" L. هیدرولیز قلیایی چربی ها. آزمایش آزمایشگاهی شماره 2 "اثر صابون در آب سخت."
"استرها و چربی ها" - اسید استیک. برای جابجایی تعادل به سمت راست، لازم است آب یا اتر حذف شود. چربی ها به طور گسترده در طبیعت پراکنده هستند و بر اساس منشاء آنها به دو دسته حیوانی و گیاهی تقسیم می شوند. استرها در طبیعت بسیار رایج هستند. استرهای با بوی مطبوع در عطرسازی و صنایع غذایی کاربرد دارند.
در مجموع 13 ارائه در این موضوع وجود دارد
1-2 قطره روغن نباتی (یا سایر چربی ها) را در پنج لوله آزمایش بریزید. 1 میلی لیتر اتیل الکل در لوله آزمایش اول، اتیل اتر در لوله دوم، بنزین در سوم، بنزن در لوله آزمایش و آب در لوله آزمایش بریزید. محتویات لوله های آزمایش را تکان دهید و بگذارید بماند.
آیا چربی در همه مواد حل می شود؟ کدام مواد حلال چربی خوب و کدام مواد مضر هستند؟ بر اساس آزمایش چه نتیجه ای می توان در مورد حلالیت چربی ها گرفت.
خروجی نمونه
1. روغن آفتابگردان + آب = تشکیل امولسیون ناپایدار به دنبال جداسازی سریع مخلوط به دو لایه.
2. روغن آفتابگردان + اتیل الکل = تشکیل محلول کدر در نتیجه حل نشدن کافی روغن.
3. روغن آفتابگردان + بنزن = محلول تقریبا شفاف.
4. روغن آفتابگردان + بنزین = محلول شفاف روغن کاملا در بنزین محلول است
به طور کامل در اتیل اتر محلول است
روغن نباتی که غیرقطبی است در حلال های غیر قطبی مانند بنزین، اتیل اتر حل می شود.
آب و الکل حلال های قطبی هستند، چربی در آنها به مقدار ضعیف یا عملا نامحلول است.
آزمایش شماره 2. امولسیون کردن چربی ها. (اگر نکته ای دارید پاسخ خود را بنویسید)
3-4 قطره روغن نباتی را در پنج لوله آزمایش بریزید. 5 میلی لیتر آب به اولین لوله آزمایش، محلول 5 درصد NaOH به دوم، محلول سودا به سوم، محلول صابون به چهارم، محلول پروتئین به پنجم اضافه کنید. محتویات هر لوله را به شدت تکان دهید و تشکیل امولسیون را مشاهده کنید. لوله های آزمایش را با امولسیون های به دست آمده به مدت چند دقیقه در یک قفسه قرار دهید.
جداسازی در کدام لوله آزمایش اتفاق افتاد؟ چه موادی امولسیون های پایدار تولید می کنند؟
امولسیونیک سیستم پراکندگی متشکل از دو یا چند فاز مایع است که یکی از آنها (به نام محیط پراکندگی) پیوسته است.
اگر تقریباً به همان مقدار روغن و آب مصرف کنید و امولسیون را بطور مکانیکی مثلاً با هم زدن تهیه کنید، جداسازی سریع اتفاق می افتد.
تشکیل امولسیون های پایدار با افزودن سورفکتانت ها اتفاق می افتد.
آزمایش شماره 3. صابون سازی چربی ها در محلول قلیایی آبی-الکلی. (تظاهرات تصویری) توضیح کوتاهتجربه.
2 گرم چربی را در یک لوله آزمایش قرار دهید و 6 میلی لیتر محلول الکلی 15٪ قلیایی را اضافه کنید. مخلوط را با یک میله شیشه ای هم بزنید، لوله آزمایش را در پایه محکم کنید و با درب رفلاکس ببندید. لوله آزمایش را با مخلوط در یک حمام آب قرار دهید و به مدت 12-15 دقیقه حرارت دهید تا به جوش آید. صابون سازی را تا زمانی که مایع یکدست شود ادامه دهید. برای تعیین پایان صابونی شدن، چند قطره از مخلوط حاصل را در لوله آزمایش بریزید و 6 میلی لیتر آب اضافه کنید و محلول را حرارت دهید. اگر مخلوط گرفته شده بدون ترشح قطرات چربی در آب حل شود، می توان صابون سازی را کامل در نظر گرفت. اگر قطرات چربی در محلول وجود داشت، چند دقیقه دیگر به حرارت دادن مخلوط در حمام آب ادامه دهید.
محلول NaOH اشباع شده را به مایع غلیظ حاصل اضافه کنید. مایع کدر می شود و لایه ای از صابون آزاد می شود که روی سطح شناور می شود. اجازه دهید مخلوط ته نشین شود و لوله آزمایش را با آب سرد خنک کنید، صابون حاصل را خارج کرده و برای آزمایش های بعدی بگذارید.
سوالات خودآزمایی: (پاسخ به سوالات برجسته شده در دفترچه یادداشت شما)
1. چه موادی به عنوان چربی طبقه بندی می شوند؟
2. نقش چربی ها در بدن چیست؟
3- چه فرآیندی به نام rancidity نامیده می شود؟
4. روغن های گیاهی و چربی های حیوانی را از نظر ترکیب، خواص و
کاربرد.
5. روش های بدست آوردن چربی های حیوانی و روغن های گیاهی را شرح دهید.
6. سورفکتانت چیست؟
بر اساس ماهیت گروه های آب دوست و آبگریز به چه انواع سورفکتانت ها تقسیم می شوند؟
صابون معمولی چه نوع سورفکتانتی است؟
9. صابون مایع (مواد شوینده)، صابون جامد چیست؟ (صابون های آرایشی و بهداشتی و لباسشویی)
10. معادلات واکنش سنتز چربی ها را بنویسید: الف) اسید پالمیتیک و
گلیسرین؛ ب) اسید لینولئیک و گلیسرول. چربی های بدست آمده را نام ببرید.
11. معادلات واکنش برای تولید: الف) اولئولینولئوپالمیتین را بنویسید. ب) تری گلیسیرید اسید بوتیریک. ج) دیلوستئارین.
12. تمام تغییراتی را که با چربی ها در طی پردازش تکنولوژیکی غذا رخ می دهد، شرح دهید.
"هیدرولیز کربوهیدرات، دناتوره شدن پروتئین."
الف) کربوهیدرات (متن برای خواندن و تکرار)
کربوهیدرات ها (قندها) در طبیعت رایج هستند و نقش مهمی در زندگی انسان دارند. آنها تا 80 درصد از جرم ماده خشک گیاهان و حدود 2 درصد از ماده خشک موجودات جانوری را تشکیل می دهند.
نام کربوهیدرات ها به این دلیل به وجود آمد که در ابتدا موادی شناخته شدند که ترکیب آنها را می توان با فرمول Cn(H2O)m بیان کرد.
مونوساکاریدها آلدهیدهای پلی هیدریک یا کتو الکل هستند.
پلی ساکاریدها به دو دسته قند مانند (الیگوساکارید) و غیر قندی تقسیم می شوند. پلی ساکاریدهای با وزن مولکولی کم (شبه مانند) حاوی تعداد کمی (10-2) باقی مانده مونوساکارید در مولکول هستند. آنها به خوبی در آب حل می شوند، طعم شیرین و مشخصی دارند ساختار کریستالی. برخی از آنها (مالتوز، لاکتوز) باعث کاهش یون های مس (P) (مایع Fehling) می شوند، آنها احیا کننده نامیده می شوند، برخی دیگر (ساکارز، ترهالوز) کاهش نمی دهند و بنابراین به عنوان الیگوساکاریدهای غیر احیا کننده طبقه بندی می شوند.
پلی ساکاریدهای با وزن مولکولی بالا (غیر قند مانند) حاوی ده ها تا چند ده هزار باقیمانده مونوساکارید هستند. آنها در آب نامحلول، بی مزه هستند و ساختار کریستالی مشخصی ندارند.
بالاترین ارزشمونوساکاریدها شامل گلوکز و فروکتوز هستند.
گلوکز (C 6 H 12 O 6 ) یک ماده کریستالی بی رنگ و محلول در آب است.
مطالعه ساختار و خواص نشان داد که گلوکز می تواند به اشکال مختلف وجود داشته باشد: آلدهید و دو شکل حلقوی.
گلوکز در بسیاری از میوه ها و انواع توت ها (انگور) یافت می شود و در طی تجزیه دی ساکاریدها و نشاسته در غذا در بدن تشکیل می شود. به سرعت و به راحتی از روده ها به خون جذب می شود و بدن به عنوان منبع انرژی برای تشکیل گلیکوژن در کبد، تغذیه بافت مغز، ماهیچه ها و حفظ سطح قند خون مورد نیاز استفاده می کند.
گلوکز تحت تأثیر آنزیم ها تخمیر می شود.
1-2 قطره روغن نباتی (یا سایر چربی ها) را در چهار لوله آزمایش بریزید. در لوله آزمایش اول 1 میلی لیتر اتیل اتر، در لوله آزمایشی 1 میلی لیتر اتیل الکل، در لوله سوم 1 میلی لیتر بنزین و در لوله چهارم 1 میلی لیتر آب بریزید. محتویات لوله های آزمایش را تکان دهید و بگذارید بماند. آیا چربی در هر لوله آزمایش حل شد؟ کدام مواد حلال چربی خوب و کدام مواد مضر هستند؟ چرا؟ بر اساس آزمایش چه نتیجه ای می توان در مورد حلالیت چربی ها گرفت؟
نتیجه:
آزمایش شماره 6 افزودن برم به اسید اولئیک
3-4 قطره آب برم و 1 قطره اسید اولئیک به لوله آزمایش اضافه کنید و به شدت تکان دهید. آب برم تغییر رنگ می دهد.
(CH 3)-(CH2) 7 -CH=CH-(CH2) 7 – COOH + Br 2 → (CH 3)-(CH 2) 7 -CHBr -CHBr -(CH 2) 7 – COOH
(دیبروموستئاریک اسید)
آزمایش شماره 7 اکسیداسیون اسید اولئیک با پرمنگنات پتاسیم
2 قطره اسید اولئیک، محلول کربنات سدیم و محلول پرمنگنات پتاسیم را در یک لوله آزمایش بریزید. وقتی مخلوط تکان می خورد، رنگ صورتی از بین می رود. تغییر رنگ آب برم و محلول پرمنگنات پتاسیم نشان دهنده چیست؟
نتیجه:
(CH 3)-(CH2) 7 -CH=CH-(CH2) 7 –COOH +[O]+HON→(CH3)-(CH2) 7 -CH – CH-(CH2) 7 – UNS
دی هیدروکسی استئاریک اسید
آزمایش شماره 8 حل کردن صابون در آب.
یک تکه صابون (تقریباً 10 میلی گرم) را در یک لوله آزمایش قرار دهید، 5 قطره آب به آن اضافه کنید و محتویات لوله آزمایش را به مدت 1-2 دقیقه کاملاً تکان دهید. پس از این، محتویات لوله آزمایش در شعله مشعل گرم می شود. سدیم و سایر صابون های قلیایی (پتاسیم، آمونیوم) به خوبی در آب حل می شوند.
سوالات تستی مبحث کربوکسیلیک اسیدها:
1 تبدیل های زیر را انجام دهید: C 2 H 6 → C 2 H 5 Cl → C 2 H 5 OH → CH 3 COH → CH 3 COOH
2. برای تولید 6 لیتر هیدروژن چند گرم منیزیم و اسید استیک لازم است.
3-معادلات واکنش تولید اسید سوکسینیک از اسید مونوکلرواستیک را بنویسید؟
4- معادلات واکنش را بنویسید و ترکیبات تشکیل شده را نام ببرید:
الف) اسید لاکتیک + اتیل الکل
ب) اسید لاکتیک + هیدروکسید سدیم
ج) اسید لاکتیک + اسید استیک
5. فرمول ساختاری پالمیتودیستارین را بنویسید
کار آزمایشگاهی شماره 9 اسیدهای آمینه. سنجاب ها
پروتئین ها حاوی کربن، هیدروژن، اکسیژن، نیتروژن، گوگرد، فسفر و عناصر دیگر هستند. وزن مولکولی یک پروتئین می تواند به صدها هزار واحد کربن برسد. پروتئین ها ترکیبات ناپایداری هستند و به راحتی تحت تأثیر اسیدها، قلیاها یا آنزیم ها هیدرولیز می شوند. محصولات نهایی تجزیه پروتئین اسیدهای آمینه با ترکیبات مختلف هستند.
اسیدهای آمینه را می توان به عنوان مشتقاتی از اسیدهای کربوکسیلیک در نظر گرفت که در آنها اتم هیدروژن در رادیکال با یک گروه آمینه جایگزین می شود:
اسیدهای آمینه به طور همزمان دارای دو نوع گروه عاملی هستند: کربوکسیل که یک حامل است. خواص اسیدیو یک گروه آمینه - حامل خواص اساسی است. اسیدهای آمینه خاصیت آمفوتریک دارند، به عنوان مثال، خواص اسیدها و بازها، بنابراین پروتئین ها نیز خواص آمفوتریک را نشان می دهند، زیرا آنها از بقایای اسید آمینه ساخته شده اند.
پروتئین ها در حلال های مختلف حل می شوند. بسیاری از پروتئین ها در آب حل می شوند، برخی در محلول های نمک های خنثی، قلیاها یا اسیدها.
تحت شرایط خاصی، پروتئین ها می توانند رسوب کنند و رسوب می تواند برگشت پذیر یا غیر قابل برگشت باشد. توانایی رسوب پروتئین ها در شرایط مختلف برای شناسایی و جداسازی آنها استفاده می شود. از واکنش های رنگی به پروتئین ها نیز برای شناسایی پروتئین ها استفاده می شود. این واکنش ها شامل زانتوپروتئین، بیورت و واکنش های دیگر است.
معرف ها. محلول پروتئین؛ محلول اسید آمینه استیک؛ اسید سولفوریک(مجموع)؛ اسید نیتریک (conc.)؛ اسید هیدروکلریک (conc.)؛ هیدروکسید سدیم، محلول 20٪؛ استات سرب، محلول های 10 و 20 درصد؛ سولفات مس (محلول های اشباع و 1٪) CuSO 4 ; آمونیاک (conc.) NH 3; سدیم کلرید NaCl، محلول 10٪؛ سولفات آمونیوم، محلول اشباع (NH 4) 2 SO 4; فنل فتالئین؛ کاغذ تورنسل، متیل اورنج؛ قرمز تورنسل اسید آمینه استیک، 0.2N. راه حل؛ اکسید مس (II) CuO، پودر؛ سود سوزآور، 2 نیوتن. محلول NaOH
تجهیزات. لوله آزمایش خشک؛ میله شیشه ای، لوله آزمایش با لوله خروجی گاز.
تجربه شماره 1.تشکیل نمک آمینواستیک مساسیدها
معرف ها و مواد:
کمی پودر اکسید مس CuO و 4 قطره محلول اسید آمینه استیک را در یک لوله آزمایش قرار داده و در شعله مشعل حرارت داده و محتویات لوله آزمایش را تکان می دهند. لوله آزمایش برای مدتی روی پایه قرار می گیرد تا پودر اکسید مس سیاه اضافی ته نشین شود. 1 قطره محلول هیدروکسید سدیم را به محلول آبی ته نشین شده اضافه کنید. راه حل روشن باقی می ماند.
اسیدهای آمینه با تشکیل نمک های مس رنگی مشخص می شوند رنگ ابی.
اسیدهای آمینه α نمکهای پیچیده داخلی رنگی با مس می دهند که بسیار پایدار هستند:
تجربهشماره 2. تأثیر اسیدهای آمینه بر شاخص ها
0.5 میلی لیتر محلول آمینو استیک اسید را در سه لوله آزمایش بریزید و فنل فتالئین را به لوله اول، متیل اورانژ را به لوله دوم و تورنسل را به لوله سوم اضافه کنید. رنگ اندیکاتورها تغییر نمی کند چرا محلول های آبی مونو آمینو اسیدها نسبت به اندیکاتورها خنثی هستند؟
نتیجه:
تجربهشماره 3. انعقاد پروتئین هنگام گرم شدن
مقدار کمی از محلول پروتئین را در یک لوله آزمایش قرار داده و در شعله مشعل حرارت داده تا به جوش آید. رسوب پروتئین را به صورت پوسته پوسته یا ابری مشاهده کنید. چه چیزی این را توضیح می دهد؟ محلول را با آب رقیق کنید. آیا رسوب حل می شود؟ اگر نه، چرا که نه؟ محلول پروتئین را برای استفاده در آزمایش بعدی کمی خنک کنید.
نتیجه:
تجربه شماره4. نمک زدن پروتئین ها با سولفاتآمونیوم
1-1.5 میلی لیتر محلول پروتئین و سولفات آمونیوم را در لوله آزمایش بریزید و مخلوط را تکان دهید و در شعله مشعل حرارت دهید تا بجوشد. مایع کدر می شود و مقدار پروتئین منعقد شده به شدت افزایش می یابد. افزودن نمک های خنثی باعث تسهیل و تسریع انعقاد پروتئین ها در هنگام گرم شدن می شود. انعقاد پروتئین یک فرآیند رسوب برگشت ناپذیر است، زیرا مولکول های پروتئین ساختار خود را تغییر می دهند.
تجربهشماره 5. رسوب پروتئین ها با نمک های سنگینفلزات
2-1 میلی لیتر محلول پروتئین را در دو لوله آزمایش بریزید و به آرامی قطره قطره در حین تکان دادن محلول اشباع سولفات مس در یکی از آنها و محلول 20 درصد استات سرب را در دیگری بریزید. یک رسوب لخته یا کدورت تشکیل می شود. نمک های فلزات سنگین پروتئین ها را از محلول ها رسوب می دهند و ترکیبات نمک ساز نامحلول در آب را تشکیل می دهند؛ با نمک های مس - یک رسوب آبی؛ با نمک های سرب - یک رسوب سفید.
تجربهشماره 6. رسوب پروتئین ها توسط مواد معدنیاسیدها
1 میلی لیتر محلول پروتئین را در سه لوله آزمایش بریزید. اسید نیتریک غلیظ را با دقت به لوله آزمایش حاوی محلول پروتئین اضافه کنید تا اسید با پروتئین مخلوط نشود. حلقه ای از رسوبات پوسته پوسته سفید در جایی که این دو مایع در تماس هستند تشکیل می شود. این آزمایش را با اسیدهای سولفوریک و هیدروکلریک غلیظ تکرار کنید. پروتئین ها با اسیدهای غلیظ ترکیباتی شبیه نمک می سازند و در عین حال باعث انعقاد پروتئین می شوند. در بیشتر موارد، رسوب تشکیل شده در اسیدهای غلیظ اضافی (به جز اسید نیتریک) محلول است.
تجربهشماره 7. واکنش های رنگی به پروتئین ها
1 واکنش زانتوپروتئینواکنش زانتوپروتئین نشان دهنده وجود آمینو اسیدهای حاوی هسته های بنزن مانند تیروزین در پروتئین است. هنگامی که چنین اسیدهای آمینه با اسید نیتریک برهمکنش می کنند، ترکیبات نیترو به رنگ زرد تشکیل می شوند.
5-6 قطره اسید نیتریک غلیظ را به 1 میلی لیتر محلول پروتئین اضافه کنید تا زمانی که یک رسوب سفید یا کدر شدن از پروتئین منعقد شده ظاهر شود. مخلوط واکنش را حرارت دهید تا رسوب تبدیل شود رنگ زرد. در طی فرآیند هیدرولیز، رسوب حل می شود. مخلوط را خنک کرده و با دقت قطره قطره محلول غلیظ سدیم هیدروکسید NaOH را به آن اضافه کنید. رنگ نارنجی می شود که نشان دهنده تشکیل آنیون های با رنگ شدیدتر است.
2 واکنش بیورتبا استفاده از واکنش بیورت، وجود گروه های پپتیدی (-CO-NH-) در مولکول های پروتئین تشخیص داده می شود. پروتئین های دارای نمک مس به دلیل تشکیل ترکیبات پیچیده رنگ قرمز مایل به بنفش می دهند.
1-2 میلی لیتر محلول پروتئین، 20% هیدروکسید سدیم را در یک لوله آزمایش بریزید. سپس 3-4 قطره از محلول رقیق شده و تقریباً بی رنگ سولفات مس (CuSO*5H 2 O) را اضافه کنید و محتویات را کاملاً مخلوط کنید. مایع به رنگ بنفش در می آید.
سوالات تستی با موضوع "اسیدهای آمینه"
1. هر ساختار یک مولکول پروتئین را به اختصار توضیح دهید.
2.. نموداری بسازید که منعکس کننده تبدیل پروتئین های غذا در بدن انسان است.
3. موارد استفاده از پروتئین ها را به اختصار شرح دهید.
4. چه چیزی فعالیت بیولوژیکی خاص یک مولکول پروتئین را تعیین می کند؟ در چه مواردی می توان آن را از دست داد؟
5. چه نوع هیدرولیز پروتئین را می شناسید؟
کار آزمایشگاهی شماره 10.خواصمونوساکاریدها
با توجه به هیدرولیز، کربوهیدرات ها به دو دسته اصلی تقسیم می شوند: کربوهیدرات های ساده یا مونوساکاریدها (گلوکز، فروکتوز، گالاکتوز) و قندهای پیچیده یا پلی ساکاریدها. کربوهیدرات های پیچیده به نوبه خود به دو گروه اصلی تقسیم می شوند: کربوهیدرات های قند مانند (ساکارز، لاکتوز، مالتوز) و کربوهیدرات های غیر قند مانند (نشاسته، فیبر). از بین مونوساکاریدها، مهمترین آنها گلوکز و فروکتوز است که خواص شیمیایی آنها با ویژگی های ساختار آنها تعیین می شود. کربوهیدرات های پیچیده شبیه شکر طعم شیرینی دارند، در آب حل می شوند و در طول هیدرولیز به مونوساکاریدها تجزیه می شوند. کربوهیدراتهای پیچیده غیر قندی طعم شیرینی ندارند، پس از هیدرولیز به مونوساکاریدها نیز تجزیه میشوند.
معرف ها. گلوکز، محلول های 20٪ و 2٪؛ معرف سلیوانوف؛ ساکارز کریستالی و محلول 10٪ تازه تهیه شده؛ لاکتوز، محلول 10٪؛ مایع فهلینگ (I); اسید سولفوریک، محلول 10٪؛ محلول آمونیاک، 2.5٪ NH 3 * H 2 O. سدیم هیدروکسید NaOH، محلول 1٪؛ نیترات نقره، محلول AgNO3 1٪؛
تجهیزات.لیوان با ظرفیت 100 میلی لیتر؛ حمام آب؛ قیف کاغذ فیلتر؛ .
تجربه شماره 1. اکسیداسیونگلوکز با محلول آمونیاک اکسید نقره (واکنش آینه نقره)
1-2 میلی لیتر محلول آمونیاک را در یک لوله آزمایش بریزید و 1 میلی لیتر نیترات نقره AgNO 3 را اضافه کنید. ابتدا یک رسوب قهوه ای اکسید نقره رسوب می کند که سپس در محلول آمونیاک اضافی ([Ag(NH 3) 2]OH حل می شود. 2 میلی لیتر از محلول گلوکز 20 درصد و چند قطره هیدروکسید سدیم 2 درصد را به محلول آمونیاک آماده شده اکسید نقره اضافه کنید و مخلوط حاصل را با دقت حرارت دهید تا محلول شروع به سیاه شدن کند. علاوه بر این، واکنش بدون حرارت دادن ادامه می یابد و نقره فلزی به شکل یک پوشش آینه بر روی دیواره های لوله آزمایش آزاد می شود.

گلوکز گلوکونیک اسید
تجربه شماره 2. اکسیداسیون گلوکز با معرف Fehling
3 قطره محلول گلوکز و یک قطره معرف Fehling وارد لوله آزمایش می شود. لوله آزمایش را با زاویه نگه دارید، قسمت بالای محلول را با دقت گرم کنید. در این حالت، قسمت گرم شده محلول به دلیل تشکیل هیدروکسید مس (I) به رنگ نارنجی مایل به زرد در می آید که متعاقباً به یک رسوب قرمز اکسید مس (I) Cu 2 O تبدیل می شود.
اکسیداسیون با معرف Fehling به عنوان یک واکنش کیفی به گلوکز عمل می کند.
ورزش:معادله این واکنش را بنویسید و نتیجه بگیرید
آزمایش شماره 3 رزین کردن گلوکز با قلیایی
4 قطره محلول گلوکز را در یک لوله آزمایش بریزید و 2 قطره محلول هیدروکسید سدیم به آن اضافه کنید. مخلوط را به جوش آورده و به مدت 2 تا 3 دقیقه به آرامی بجوشانید. محلول زرد شده و سپس به رنگ قهوه ای تیره در می آید. وقتی با مواد قلیایی حرارت داده می شود، مونوساکاریدها رزینی می شوند و قهوه ای می شوند. فرآیند رزین سازی منجر به تشکیل مخلوط پیچیده ای از مواد می شود.
آزمایش شماره 4 واکنش سلیوانوف به کتوز
یک کریستال رزورسینول، 2 قطره اسید کلریدریک و 2 قطره محلول فروکتوز در یک لوله آزمایش قرار می گیرد. محتویات لوله آزمایش تا زمان جوشیدن حرارت داده می شود. مایع به تدریج قرمز می شود.
هنگامی که با اسیدهای معدنی غلیظ حرارت داده می شود، مولکول های هگزوز به تدریج تجزیه می شوند و مخلوطی از محصولات مختلف را تشکیل می دهند (هیدروکسی متیل فورفورال نیز یکی از محصولات است) که ترکیب رنگی با رزورسینول تشکیل می دهد. این واکنش به فرد اجازه می دهد تا به سرعت وجود کتوهگزوزها را در مخلوطی از قندها تشخیص دهد.
سوالات تستی با موضوع "خواص مونوساکاریدها و دی ساکاریدها"
به چه ترکیباتی مونوساکارید می گویند؟
بر اساس چه آزمایشاتی می توانیم در مورد ساختار گلوکز نتیجه گیری کنیم؟
در طی تخمیر الکلی گلوکز، 112 لیتر CO 2 آزاد شد. چه مقدار الکل اتیلیک دریافت کردید و چه مقدار گلوکز مصرف کرد؟
4. با استفاده از متن پاراگراف کتاب درسی، پاسخ کتبی سؤالات زیر را آماده کنید: الف) چیست؟ مشخصات فیزیکیگلوکز؟ ب) گلوکز در کجای طبیعت وجود دارد؟ ج) فرمول مولکولی گلوکز چیست؟
5- کدام مونوساکاریدها پنتوز و کدام هگزوز نامیده می شوند؟
6. کدام اشکال قندها را فورانوز و کدام را پیرانوز می نامند
7- مبنای تعیین ایزومرهای راست و چپ قندها با رشته شیمیایی آنها چیست؟
کار آزمایشگاه شماره 11 خواصپلی ساکاریدها
معرف هانشاسته، پودر و محلول؛ محلول ساکارز؛ سیب زمینی؛ نان چاودار؛ سیب زمینی؛ محلول ید؛ اسید سولفوریک، محلول 20٪ H 2 SO 4 I (conc.); کربنات سدیم Na 2 CO 3; کربنات کلسیم CaCO 3 ;; آمونیاک، محلول 1٪ NH 3 * H 2 O؛ مایع فهلینگ (I);
تجهیزات.لیوان با ظرفیت 100 میلی لیتر؛ قیف حمام آب؛ لیوان های چینی - 2 کامپیوتر. هاون و هاون؛ میله شیشه ای، کاغذ صافی؛ پشم پنبه
آزمایش شماره 1. برهمکنش نشاسته با ید. واکنش کیفی به نشاسته.
2 قطره خمیر نشاسته و 1 قطره محلول ید را در یک لوله آزمایش بریزید. محتویات لوله آزمایش آبی می شود. مایع آبی تیره به دست آمده حرارت داده می شود تا به جوش آید. رنگ ناپدید می شود، اما پس از سرد شدن دوباره ظاهر می شود.
نشاسته مخلوطی از دو پلی ساکارید - آمیلوز (20٪) و آمیلوپکتین (80٪) است. آمیلوز در آب گرم محلول است و با ید رنگ آبی می دهد. آمیلوز و آمیلوپکتین هر دو از واحدهای گلوکز تشکیل شدهاند که توسط پیوندهای آلفا گلیکوزیدی به هم متصل شدهاند، اما در شکل مولکولها متفاوت هستند. آمیلوز یک پلی ساکارید خطی است که از چندین پلی ساکارید تشکیل شده است

آمیلوپکتین در آب گرم نامحلول است و در آن متورم می شود و خمیر نشاسته ای تشکیل می دهد. آمیلوپکتین، بر خلاف آمیلوز، حاوی زنجیره های شاخه ای از باقی مانده های گلوکز است. آمیلوپکتین با ید رنگ بنفش مایل به قرمز می دهد.
به دست آوردن خمیر نشاسته.
12 گرم نشاسته را در 40 میلی لیتر آب سرد رقیق می کنیم تا شیر نشاسته به دست آید. 160 میلی لیتر آب را به جوش بیاورید و در حین هم زدن شیر نشاسته را داخل آن بریزید. خمیر نشاسته به دست آمده را به جوش آورده و تا دمای اتاق خنک کنید
آزمایش شماره 2. به روز رسانیافزودن نشاسته به نان و سیب زمینی
یک قطره ید را روی یک تکه نان سفید و یک برش سیب زمینی خام بریزید. رنگ چگونه تغییر خواهد کرد؟ نتیجه گیری کنید.
تجربه№3. شواهدی برای وجود گروه های هیدروکسیل در ساکارز
1 قطره محلول ساکارز، 5 قطره محلول قلیایی و 4-5 قطره آب را در یک لوله آزمایش بریزید. یک قطره محلول سولفات مس (II) اضافه کنید. این مخلوط به دلیل تشکیل ساکارات مس، رنگ مایل به آبی کمرنگی پیدا می کند.
راه حل برای آزمایش بعدی ذخیره می شود.
آزمایش شماره 4 عدم توانایی کاهش در ساکارز
محلول ساکارات مس با احتیاط روی شعله مشعل حرارت داده می شود و لوله آزمایش را نگه می دارد تا فقط قسمت بالایی محلول گرم شود. ساکارز در این شرایط اکسید نمی شود، که نشان دهنده عدم وجود یک گروه آلدهید آزاد در مولکول آن است.
تجربه شماره 5هیدرولیز اسیدی ساکارز
1 قطره محلول ساکارز را در یک لوله آزمایش، 1 قطره 2 نیوتن بریزید. اسید هیدروکلریک 3 قطره آب و با احتیاط روی شعله شعله به مدت 20-30 دقیقه حرارت دهید. نیمی از محلول را در لوله آزمایش دیگری ریخته و 4-5 قطره محلول قلیایی به آن اضافه می کنند (تا واکنش قلیایی به تورنسل) و 3-4 قطره آب. سپس 1 قطره محلول سولفات مس اضافه کنید و روی محلول آبی را حرارت دهید تا بجوشد. رنگ زرد نارنجی ظاهر می شود که نشان دهنده تشکیل گلوکز است. به باقی مانده محلول ساکارز هیدرولیز شده (اولین لوله آزمایش)، یک کریستال رزورسینول، 2 قطره اسید هیدروکلریک غلیظ اضافه کنید و حرارت دهید تا بجوشد. رنگ مایل به قرمز ظاهر می شود که نشان دهنده تشکیل فروکتوز است. مولکول ساکارز به راحتی در طول هیدرولیز به یک مولکول گلوکز و یک مولکول فروکتوز تقسیم می شود. هر دو مونوساکارید در ساکارز به شکل حلقوی وجود دارند. هر دو هیدروکسیل گلیکوزیدی در ایجاد پیوند بین آنها نقش دارند.
در ساکارز، باقیمانده فروکتوز به شکل یک حلقه پنج عضو شکننده - فورانوز است. چنین قندهای پیچیده ای به راحتی هیدرولیز می شوند.
نتیجه:

تجربه شماره 6. هیدرولیز اسیدی نشاسته
که در 7 3 قطره آب ید بسیار رقیق و تقریبا بی رنگ در هر لوله آزمایش ریخته می شود. 10 میلی لیتر خمیر نشاسته در یک فنجان چینی ریخته می شود، 5 میلی لیتر محلول اسید سولفوریک به آن اضافه می شود و محتویات آن با میله شیشه ای مخلوط می شود. فنجان را با محلول روی توری آزبست قرار دهید و آن را روی شعله کوچک گرم کنید. هر 30 ثانیه یک قطره از محلول را با پیپت با سوراخ مویین بردارید و با آب ید به لوله آزمایش دیگری منتقل کنید. نمونه های متوالی تغییر رنگ تدریجی را در واکنش با ید نشان می دهند. رنگ نمونه
اولین. . آبی
دومین. آبی-بنفش
سوم قرمز بنفش
چهارم ...... قرمز مایل به نارنجی
پنجم.........نارنجی
ششم نارنجی-زرد
زرد روشن هفتم (رنگ آب ید)
محلول خنک می شود، با یک محلول قلیایی با استفاده از کاغذ تورنسل قرمز به یک واکنش قلیایی قوی خنثی می شود، یک قطره از معرف Fehling اضافه می شود و گرم می شود. ظاهر یک رنگ نارنجی ثابت می کند که محصول نهایی هیدرولیز گلوکز است.
(با 6 ن 10 در باره 5 ) ایکس + xH 2 0 = xС 6 ن 12 0 6
گلوکز نشاسته
هنگام گرم شدن با اسیدهای معدنی رقیق و همچنین تحت تأثیر آنزیم ها، نشاسته تحت هیدرولیز قرار می گیرد. هیدرولیز نشاسته به تدریج با تشکیل کربوهیدرات های ساده به طور فزاینده اتفاق می افتد.
طرح هیدرولیز تدریجی نشاسته به شرح زیر است:
(با 6 ن 10 در باره 5 ) ایکس → (C 6 ن 10 در باره 5 )у →(با 6 ن 10 در باره 5 ) z → با 12 ن 22 0 11 → با 6 ن 12 در باره ب
نشاسته محلول دکسترین مالتوز گلوکز
اولین محصول هیدرولیز - نشاسته محلول - خمیر تشکیل نمی دهد، با ید رنگ آبی می دهد. پس از هیدرولیز بیشتر، آنها تشکیل می شوند دکسترین ها- پلی ساکاریدهای ساده تر که با ید رنگی از بنفش آبی به نارنجی می دهند. مالتوز و سپس گلوکز رنگ طبیعی ید را تغییر نمی دهند.
تجربه شماره 7. فیبر یا سلولز
فیبر اساس اندام های فردی همه گیاهان، اسکلت آنها است. آن را به همان روش نشاسته ساخته شده است - از مقدار زیادی از باقی مانده های گلوکز. واحدهای گلوکز مجزا در سلولز از طریق هیدروکسیل های بتا گلوکزیدیک به یکدیگر متصل می شوند.
تفاوت در چسبندگی متقابل مولکول های گلوکز در نشاسته و فیبر منجر به تفاوت شدید در برخی از خواص آنها می شود. فیبر در محلول آمونیاک هیدرات اکسید مس (معرف شوایتزر) حل می شود. در عین حال، مولکول های آن تا حدی به قطعات کوچکتر تقسیم می شوند. اگر چنین محلولی با اسید خنثی شود، فیبر دوباره به شکل یک توده لختهای ظاهر میشود، اما طول و ساختار مولکولها کمی تغییر کرده است.
پس از یک درمان کوتاه با اسید سولفوریک قوی، فیبر حل می شود و یک توده چسبنده - آمیلوئید تشکیل می دهد. آمیلوئید با ید آبی رنگ می شود. پس از درمان با اسید سولفوریک، کاغذ صافی قوی تر و شفاف تر می شود. این با این واقعیت توضیح داده می شود که آمیلوئید الیاف سلولز منفرد (پرگامنت گیاهی) را به هم می چسباند.
ب- تهیه پوست سبزی الف. نصف نوار کاغذ صافی را به مدت 30 تا 40 ثانیه در فنجانی با اسید سولفوریک 80 درصد فرو کنید. سپس کاغذ را در ظرفی با آب غوطه ور کنید و در نهایت آن را در محلول آمونیاک بشویید.بخش های تیمار نشده و اسیدی شده نوار کاغذ را با هم مقایسه کنید (شفافیت، استحکام). هنگام انجام این آزمایش مراقب باشید؛ هنگام انتقال کاغذ به آب، اسید سولفوریک نپاشید!
نتایج آزمایش را ثبت کنید.
سوالات تستی با موضوع "خواص پلی ساکاریدها"
1. به چه ترکیباتی پلی ساکارید می گویند
2- به چه ترکیباتی دی ساکارید می گویند؟
3.. با استفاده از متن پاراگراف کتاب درسی، پاسخ کتبی سوالات زیر را تهیه کنید:
الف) خواص فیزیکی سلولز چیست؟
ب) سلولز در کجای طبیعت وجود دارد؟ ج) فرمول واحد ابتدایی ماکرومولکول سلولز چیست؟
د) تفاوت اصلی بین نشاسته، گلیکوژن و فیبر چیست؟
4. نموداری که استفاده از نشاسته را نشان می دهد تهیه کنید.
5. خواص شیمیایی سلولز را فهرست کنید.
6. شکر معکوس به چه چیزی می گویند؟
کار آزمایشگاهی شماره 12ترکیبات هتروسیکلیک
معرف ها و مواد:فورفورال تازه آماده شده؛ نیترات نقره، 0.2 نیوتن. راه حل؛ آمونیاک، 2 N. راه حل؛ فوشینوس اسید؛ آنیلین؛ فلوروگلوسینول؛ اسید هیدروکلریک (^ = 1.19 گرم / سانتی متر مکعب)؛ اسید استیک یخبندان. اسید مخاطی؛ آمونیاک، محلول غلیظ؛ گلیسرول؛ اسید هیدروکلریک (ρ=1.19 گرم بر سانتی متر مکعب). نیل (پودر ریز آسیاب شده)؛ اسید سولفوریک (ρ = 1.84 گرم / سانتی متر 3). قلع (II) کلرید، 1 نیوتن. محلول در محیط اسید هیدروکلریک؛ سود سوزآور، 1 نیوتن. راه حل.
تجهیزات:خرده کاج، میله شیشه ای. پارچه سفید؛ کاغذ فیلتر؛ حمام آب؛ هاون و هاون.
تجربهشماره 1. واکنش های فورفورال
تجهیزات:شیشه ساعت؛ میله شیشه ای؛ کاغذ فیلتر.
2 قطره فورفورال و 8 قطره آب را داخل لوله آزمایش بریزید و تکان دهید تا فورفورال کاملا حل شود.
واکنش با اسید فوشینوس 4 قطره فوشینوس اسید و یک قطره محلول فورفورال را روی شیشه ساعت بریزید و با میله شیشه ای مخلوط کنید. پس از مدتی، رنگ صورتی کمی ظاهر می شود.
واکنش با آمونیاک نقرهیک قطره نیترات نقره و یک قطره محلول آمونیاک روی شیشه ساعت قرار می گیرد. رسوبی از هیدروکسید نقره رسوب می کند. یک قطره دیگر آمونیاک اضافه کنید و محلولی شفاف از نمک پیچیده نقره [Ag(]NНз) 2 ]ОН بدست آورید.
یک قطره محلول فورفورال به محلول آمونیاک نقره اضافه می شود. نقره آزاد به شکل لکه سیاه یا پوشش نقره ای روی شیشه ظاهر می شود.
3. واکنش با آنیلینیک قطره آنیلین را با یک قطره اسید استیک روی شیشه ساعت مخلوط کنید. نواری از کاغذ صافی با محلول به دست آمده مرطوب می شود و یک قطره فورفورال روی آن اعمال می شود. یک نقطه صورتی مایل به قرمز ظاهر می شود.
4. واکنش با فلوروگلوسینول 3 قطره محلول فورفورال، 1 قطره اسید کلریدریک و 2 کریستال فلوروگلوسینول در یک لوله آزمایش قرار می گیرد. هنگامی که گرم می شود، مخلوط به رنگ سبز تیره در می آید. فورفورال دارای خواص آلدئیدهای معطر است. به راحتی واکنش "آینه نقره ای" را ایجاد می کند، اسید فوشینوس را رنگ می کند و فنیل هیدرازون را تشکیل می دهد.
واکنش های رنگی فورفورال با آنیلین و فلوروگلوسینول بر اساس واکنش تراکم است. فورفورال در حضور اسید کلریدریک یا استیک محصولات تراکم رنگی با آنیلین، بنزیدین، رزورسینول، زایلیدین می دهد.
تجربهشماره 2. تهیه پیرول.واکنش کیفی به پیرول
(تجربهانجام دادنVاگزوزکمد لباس!)
چندین کریستال اسید موکوس و 2 قطره محلول آمونیاک را در یک لوله آزمایش قرار دهید و محتویات لوله آزمایش را با یک میله شیشه ای کاملاً مخلوط کنید. 2 قطره گلیسیرین اضافه کنید و دوباره مخلوط را مخلوط کنید. لوله آزمایش با دقت در شعله مشعل گرم می شود. یک خرده کاج را با 1 قطره اسید کلریدریک مرطوب می کنند و به قسمت بالایی لوله آزمایش اضافه می کنند و حرارت دادن آن را ادامه می دهند. بخار پیرول خرده های کاج را قرمز می کند.
هنگامی که آمونیاک اضافه می شود، نمک آمونیوم اسید موکوس به دست می آید که سپس تجزیه می شود. محصولات تجزیه شامل پیرول است. گلیسیرین بر روند واکنش تأثیر می گذارد و آن را یکنواخت تر می کند. پیرول به راحتی توسط اسیدها قیر می شود و قرمز می شود.
تجربهشماره 3. خواص نیل
1. حلالیت نیل در آب.پودر نیل را روی نوک یک ریز اسپاتول داخل لوله آزمایش بریزید و 5-6 قطره آب به آن اضافه کنید. محتویات لوله آزمایش با دقت است
در دمای اتاق تکان دهید و سپس در شعله شعله گرم کنید. یک قطره از مخلوط حاصل روی نوار کاغذ صافی اعمال می شود - یک نقطه بی رنگ تشکیل می شود که در مرکز آن پودر نیل آبی ته نشین می شود. نیل مانند اکثر حلال های رایج در آب حل نمی شود.
2 رنگرزی “Vubic”. 5 قطره از محلول کلرید قلع (II) را در یک لوله آزمایش بریزید و یک محلول هیدروکسید سدیم را قطره قطره به آن اضافه کنید تا رسوب تشکیل شده حل شود. در یک هاون کوچک، چندین کریستال نیل را با 5-6 قطره آب به دقت آسیاب کنید. با استفاده از یک پیپت، 2 قطره از سوسپانسیون به دست آمده را به یک لوله آزمایش با محلول استنیت سدیم منتقل کنید و لوله آزمایش را در حمام آب جوش حرارت دهید تا مخلوط واکنش شفاف شود.
نوار کوچکی از پارچه سفید که قبلاً شسته و ساییده شده است، در محلول قلیایی حاصل از نیل سفید قرار می گیرد. پارچه به طور کامل در محلول نیل کاهش یافته آغشته می شود، سپس صاف می شود و در هوا می ماند. پارچه ابتدا رنگ سبز و سپس آبی به خود می گیرد.
نیل آبی رنگی است که در محیط قلیایی وجود دارد و در یک محیط قلیایی، نیل آبی به نیل سفید تبدیل می شود که خاصیت فنلی دارد و در قلیاها محلول است. محلول قلیایی نیل سفید "مکعب" نامیده می شود. پارچه را در چنین محلولی غوطه ور می کنند، در محلول خیس می کنند و سپس در هوا می گذارند تا "رسیده شود". روی الیاف پارچه، نیل سفید توسط اکسیژن هوا اکسید می شود و به نیل آبی نامحلول تبدیل می شود.
 نیل آبی نیلی سفید
نیل آبی نیلی سفید
تجربه شماره 4اکسیداسیون نیل با یک عامل اکسید کننده قوی
هنگامی که نیل با یک عامل اکسید کننده قوی اکسید می شود، ایزاتین به دست می آید که در محلول ها رنگ زرد دارد (ایزاتین جامد قرمز است):
حدود 1 میلی لیتر محلول کارمین نیل و 5-10 قطره اسید نیتریک غلیظ را در لوله آزمایش بریزید چه مشاهده می شود؟ رنگ محلول چگونه تغییر کرد؟
نتیجه آزمایش را یادداشت کنید

نیل ایساتین
سوالات تستی با موضوع "ترکیبات هتروسیکلیک"
1. به چه ترکیباتی هتروسیکلیک می گویند
2. فرمول ها و نام های مهم ترین هتروسیکل های پنج عضوی را بنویسید
2. فرمول ها و نام های مهم ترین هتروسیکل های شش عضوی را بنویسید
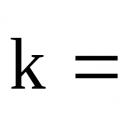 رهنمودهای ثابت سرعت واکنش برای کارهای آزمایشگاهی
رهنمودهای ثابت سرعت واکنش برای کارهای آزمایشگاهی آیا زندگی پس از مرگ وجود دارد؟
آیا زندگی پس از مرگ وجود دارد؟ دانشمندان: زمین یک "زندان فضایی" برای بشریت است دانشمندان: زمین یک زندان فضایی در جهان است
دانشمندان: زمین یک "زندان فضایی" برای بشریت است دانشمندان: زمین یک زندان فضایی در جهان است