Типы химических связей. Электроотрицательность
ОПРЕДЕЛЕНИЕ
Аммоний – положительно заряженный полиатомный ион.
Химическая формула NH 4 +
Ион аммония NH 4 + является правильным тетраэдром с в центре и атомами в вершинах тетраэдра.
В молекуле аммиака NH 3 три электронные пары образуют три связи N – H, четвертая, прина длежащая атому азота электронная пара является неподеленной. С помощью этой электронной пары образуется связь с ионом водорода, который имеет свободную орбиталь:

Таким образом, в ионе аммония три ковалентные связи образуются по обменному механизму, а одна – по донорно-акцепторному. Механизм образования не оказывает слияния на характеристики связи, все связи в катионе аммония равноценны.
Соединения аммония
Катион аммония может образовывать с различными противоионами аммонивые соединения, в которых положительно заряженный атом азота, ковалентно связан с ионами водорода и (или) с органическими радикалами, а ионно – с каким-либо анионом.
Неорганические соединения аммония
Гидрат аммиака (гидроксид аммония, аммиачная вода, едкий аммоний, едкий аммиак). Формула: NH 3 ·H 2 O
Образуется при взаимодействии аммиака с водой. Слабое основание, диссоциирует в воде с образованием катионов аммония и гидроксид-ионов:
Реакция обратима, поэтому водные растворы гидроксида аммония всегда имеют характерный резкий запах аммиака.
Соли аммония
Все соли аммония по своим свойствам похожи на соответствующие соли натрия. Хорошо растворяются в воде, полностью диссоциируют в водном растворе, при нагревании разлагаются:
В растворе гидролизуются по катиону:
Органические аммониевые соединения разделяют по количеству органических радикалов, связанных с атомом азота на первичные (R 1 NH 3) + X – , вторичные (R 1 R 2 NH 2) + X – , третичные (R 1 R 2 R 3 NH) + X – , и четвертичные (R 1 R 2 R 3 R 4 N) + X – .
Первичные, вторичные и третичные аммониевые соединения можно рассматривать как соли соответствующих аминов, их можно получить взаимодействием этих аминов с кислотами:
где R 1 ,R 2 , R 3 - органические радикалы или водород, X - анион кислотного остатка.
Качественная реакция на ионы аммония – взаимодействие со щелочами с выделением аммиака:
Примеры решения задач
ПРИМЕР 1
| Задание | Какое значение рН (больше или меньше 7) имеет водный раствор хлорида аммония? Запишите молекулярное и ионно-молекулярное уравнения гидролиза. |
| Решение | NH 4 Cl – соль слабого основания и сильной кислоты, поэтому гидролиз протекает по катиону.
Молекулярное уравнение: Полное ионное уравнение: Краткое ионное уравнение: В процессе гидролиза образовались водорода (H +), поэтому раствор имеет кислую среду (pH |
| Ответ | рН раствора хлорида аммония меньше 7. |
ПРИМЕР 2
| Задание | Какая масса соли образуется при взаимодействии 44,8 л аммиака и 33,6 литров хлороводорода (нормальные условия)? | ||||||
| Решение | Запишем уравнение реакции:
Молярные массы аммиака, хлороводорода и образующейся соли – хлорида аммония (NH 4 Cl) равны. 170133 0 Каждый атом обладает некоторым числом электронов. Вступая в химические реакции, атомы отдают, приобретают, либо обобществляют электроны, достигая наиболее устойчивой электронной конфигурации. Наиболее устойчивой оказывается конфигурация с наиболее низкой энергией (как в атомах благородных газов). Эта закономерность называется "правилом октета" (рис. 1). Рис. 1. Это правило применимо ко всем типам связей . Электронные связи между атомами позволяют им формировать устойчивые структуры, от простейших кристаллов до сложных биомолекул, образующих, в конечном счете, живые системы. Они отличаются от кристаллов непрерывным обменом веществ. При этом многие химические реакции протекают по механизмам электронного переноса , которые играют важнейшую роль в энергетических процессах в организме. Химическая связь - это сила, удерживающая вместе два или несколько атомов, ионов, молекул или любую их комбинацию . Природа химической связи универсальна: это электростатическая сила притяжения между отрицательно заряженными электронами и положительно заряженными ядрами, определяемая конфигурацией электронов внешней оболочки атомов. Способность атома образовывать химические связи называется валентностью , или степенью окисления . С валентностью связано понятие о валентных электронах - электронах, образующих химические связи, то есть находящихся на наиболее высокоэнергетических орбиталях. Соответственно, внешнюю оболочку атома, содержащую эти орбитали, называют валентной оболочкой . В настоящее время недостаточно указать наличие химической связи, а необходимо уточнить ее тип: ионная, ковалентная, диполь-дипольная, металлическая. Первый тип связи - ионная связь В соответствии с электронной теорией валентности Льюиса и Косселя, атомы могут достичь устойчивой электронной конфигурации двумя способами: во-первых, теряя электроны, превращаясь в катионы , во-вторых, приобретая их, превращаясь в анионы . В результате электронного переноса благодаря электростатической силе притяжения между ионами с зарядами противоположного знака образуется химическая связь, названная Косселем «электровалентной » (теперь ее называют ионной ). В этом случае анионы и катионы образуют устойчивую электронную конфигурацию с заполненной внешней электронной оболочкой. Типичные ионные связи образуются из катионов Т и II групп периодической системы и анионов неметаллических элементов VI и VII групп (16 и 17 подгрупп - соответственно, халькогенов и галогенов ). Связи у ионных соединений ненасыщенные и ненаправленные, поэтому возможность электростатического взаимодействия с другими ионами у них сохраняется. На рис. 2 и 3 показаны примеры ионных связей, соответствующих модели электронного переноса Косселя. Рис. 2. Рис. 3. Ионная связь в молекуле поваренной соли (NaCl) Здесь уместно напомнить о некоторых свойствах, объясняющих поведение веществ в природе, в частности, рассмотреть представление о кислотах и основаниях . Водные растворы всех этих веществ являются электролитами. Они по-разному изменяют окраску индикаторов . Механизм действия индикаторов был открыт Ф.В. Оствальдом. Он показал, что индикаторы представляют собой слабые кислоты или основания, окраска которых в недиссоциированном и диссоциированном состояниях различается. Основания способны нейтрализовать кислоты. Не все основания растворимы в воде (например, нерастворимы некоторые органические соединения, не содержащие ‑ ОН-групп, в частности, триэтиламин N(С 2 Н 5) 3) ; растворимые основания называют щелочами . Водные растворы кислот вступают в характерные реакции: а) с оксидами металлов - с образованием соли и воды; б) с металлами - с образованием соли и водорода; в) с карбонатами - с образованием соли, СO 2 и Н 2 O . Свойства кислот и оснований описывают несколько теорий. В соответствие с теорией С.А. Аррениуса, кислота представляет собой вещество, диссоциирующее с образованием ионов Н + , тогда как основание образует ионы ОН ‑ . Эта теория не учитывает существования органических оснований, не имеющих гидроксильных групп. В соответствие с протонной теорией Бренстеда и Лоури, кислота представляет собой вещество, содержащее молекулы или ионы, отдающие протоны (доноры протонов), а основание - вещество, состоящее из молекул или ионов, принимающие протоны (акцепторы протонов). Отметим, что в водных растворах ионы водорода существуют в гидратированной форме, то есть в виде ионов гидроксония H 3 O + . Эта теория описывает реакции не только с водой и гидроксидными ионами, но и осуществляющиеся в отсутствие растворителя или с неводным растворителем. Например, в реакции между аммиаком NH 3 (слабым основанием) и хлороводородом в газовой фазе образуется твердый хлорид аммония, причем в равновесной смеси двух веществ всегда присутствуют 4 частицы, две из которых - кислоты, а две другие - основания: Эта равновесная смесь состоит из двух сопряженных пар кислот и оснований: 1) NH 4 + и NH 3 2) HCl и Сl ‑ Здесь в каждой сопряженной паре кислота и основание различаются на один протон. Каждая кислота имеет сопряженное с ней основание. Сильной кислоте соответствует слабое сопряженное основание, а слабой кислоте - сильное сопряженное основание. Теория Бренстеда-Лоури позволяет объяснить уникальность роли воды для жизнедеятельности биосферы. Вода, в зависимости от взаимодействующего с ней вещества, может проявлять свойства или кислоты, или основания. Например, в реакциях с водными растворами уксусной кислоты вода является основанием, а с водными растворами аммиака - кислотой. 1) СН 3 СООН + Н 2 O ↔ Н 3 O + + СН 3 СОО ‑ . Здесь молекула уксусной кислоты донирует протон молекуле воды; 2) NH 3 + Н 2 O ↔ NH 4 + + ОН ‑ . Здесь молекула аммиака акцептирует протон от молекулы воды. Таким образом, вода может образовывать две сопряженные пары: 1) Н 2 O (кислота) и ОН ‑ (сопряженное основание) 2) Н 3 О + (кислота) и Н 2 O (сопряженное основание). В первом случае вода донирует протон, а во втором - акцептирует его. Такое свойство называется амфипротонностью . Вещества, способные вступать в реакции в качестве и кислот, и оснований, называются амфотерными . В живой природе такие вещества встречаются часто. Например, аминокислоты способны образовывать соли и с кислотами, и с основаниями. Поэтому пептиды легко образуют координационные соединения с присутствующими ионами металлов. Таким образом, характерное свойство ионной связи - полное перемещение нары связывающих электронов к одному из ядер. Это означает, что между ионами существует область, где электронная плотность почти нулевая. Второй тип связи - ковалентная связь Атомы могут образовывать устойчивые электронные конфигурации путем обобществления электронов. Такая связь образуется, когда пара электронов обобществляется по одному от каждого атома. В таком случае обобществленные электроны связи распределены между атомами поровну. Примерами ковалентной связи можно назвать гомоядерные двухатомные молекулы Н 2 , N 2 , F 2 . Этот же тип связи имеется у аллотропов O 2 и озона O 3 и у многоатомной молекулы S 8 , а также у гетероядерных молекул хлороводорода НСl , углекислого газа СO 2 , метана СH 4 , этанола С 2 Н 5 ОН , гексафторида серы SF 6 , ацетилена С 2 Н 2 . У всех этих молекул электроны одинаково общие, а их связи насыщенные и направлены одинаково (рис. 4). Для биологов важно, что у двойной и тройной связей ковалентные радиусы атомов по сравнению с одинарной связью уменьшены. Рис. 4. Ковалентная связь в молекуле Сl 2 . Ионный и ковалентный типы связей - это два предельных случая множества существующих типов химических связей, причем на практике большинство связей промежуточные. Соединения двух элементов, расположенных в противоположных концах одного или разных периодов системы Менделеева, преимущественно образуют ионные связи. По мере сближения элементов в пределах периода ионный характер их соединений уменьшается, а ковалентный - увеличивается. Например, галогениды и оксиды элементов левой части периодической таблицы образуют преимущественно ионные связи (NaCl, AgBr, BaSO 4 , CaCO 3 , KNO 3 , CaO, NaOH ), а такие же соединения элементов правой части таблицы - ковалентные (Н 2 O, СO 2 , NH 3 , NO 2 , СН 4 , фенол C 6 H 5 OH , глюкоза С 6 H 12 О 6 , этанол С 2 Н 5 ОН ). Ковалентная связь, в свою очередь, имеет еще одну модификацию. У многоатомных ионов и в сложных биологических молекулах оба электрона могут происходить только из одного атома. Он называется донором электронной пары. Атом, обобществляющий с донором эту пару электронов, называется акцептором электронной пары. Такая разновидность ковалентной связи названа координационной (донорно-акцепторной , или дативной ) связью (рис. 5). Этот тип связи наиболее важен для биологии и медицины, поскольку химия наиболее важных для метаболизма d-элементов в значительной степени описывается координационными связями. Pиc. 5. Как правило, в комплексном соединении атом металла выступает акцептором электронной пары; наоборот, при ионных и ковалентных связях атом металла является донором электрона. Суть ковалентной связи и ее разновидности - координационной связи - можно прояснить с помощью еще одной теории кислот и оснований, предложенной ГН. Льюисом. Он несколько расширил смысловое понятие терминов «кислота» и «основание» по теории Бренстеда-Лоури. Теория Льюиса объясняет природу образования комплексных ионов и участие веществ в реакциях нуклеофильного замещения, то есть в образовании КС. Согласно Льюису, кислота - это вещество, способное образовывать ковалентную связь путем акцептирования электронной пары от основания. Льюисовым основанием названо вещество, обладающее неподеленной электронной парой, которое, донируя электроны, образует ковалентную связь с Льюисовой кислотой. То есть теория Льюиса расширяет круг кислотно-основных реакций также на реакции, в которых протоны не участвуют вовсе. Причем сам протон, по этой теории, также является кислотой, поскольку способен акцептировать электронную пару. Следовательно, согласно этой теории, катионы являются Льюисовыми кислотами, а анионы - Льюисовыми основаниями. Примером могут служить следующие реакции: Выше отмечено, что подразделение веществ на ионные и ковалентные относительное, поскольку полного перехода электрона от атомов металла к акцепторным атомам в ковалентных молекулах не происходит. В соединениях с ионной связью каждый ион находится в электрическом поле ионов противоположного знака, поэтому они взаимно поляризуются, а их оболочки деформируются. Поляризуемость определяется электронной структурой, зарядом и размерами иона; у анионов она выше, чем у катионов. Наибольшая поляризуемость среди катионов - у катионов большего заряда и меньшего размера, например, у Hg 2+ , Cd 2+ , Pb 2+ , Аl 3+ , Тl 3+ . Сильным поляризующим действием обладает Н + . Поскольку влияние поляризации ионов двустороннее, она значительно изменяет свойства образуемых ими соединений. Третий тип связи - диполь-дипольная связь Кроме перечисленных типов связи, различают еще диполь-дипольные межмолекулярные взаимодействия, называемые также вандерваалъсовыми . Сила этих взаимодействий зависит от природы молекул. Выделяют взаимодействия трех типов: постоянный диполь - постоянный диполь (диполь-дипольное притяжение); постоянный диполь - индуцированный диполь (индукционное притяжение); мгновенный диполь - индуцированный диполь (дисперсионное притяжение, или лондоновские силы; рис. 6). Рис. 6. Диполь-дипольным моментом обладают только молекулы с полярными ковалентными связями (HCl, NH 3 , SO 2 , Н 2 O, C 6 H 5 Cl ), причем сила связи составляет 1-2 дебая (1Д = 3,338 × 10 ‑30 кулон-метра - Кл × м). В биохимии выделяют еще один тип связи - водородную связь, являющуюся предельным случаем диполь-дипольного притяжения. Эта связь образована притяжением между атомом водорода и электроотрицательным атомом небольшого размера, чаще всего - кислородом, фтором и азотом. С крупными атомами, обладающими аналогичной электроотрицательностью (например, с хлором и серой), водородная связь оказывается значительно более слабой. Атом водорода отличается одной существенной особенностью: при оттягивании связывающих электронов его ядро - протон - оголяется и перестает экранироваться электронами. Поэтому атом превращается в крупный диполь. Водородная связь, в отличие от вандерваальсовой, образуется не только при межмолекулярных взаимодействиях, но и внутри одной молекулы - внутримолекулярная водородная связь. Водородные связи играют в биохимии важную роль, например, для стабилизации структуры белков в виде а-спирали, или для образования двойной спирали ДНК (рис. 7). Рис.7. Водородная и вандерваальсовая связи значительно слабее, чем ионная, ковалентная и координационная. Энергия межмолекулярных связей указана в табл. 1. Таблица 1. Энергия межмолекулярных сил Примечание : Степень межмолекулярных взаимодействий отражают показатели энтальпии плавления и испарения (кипения). Ионным соединениям требуется для разделения ионов значительно больше энергии, чем для разделения молекул. Энтальпии плавления ионных соединений значительно выше, чем молекулярных соединений. Четвертый тип связи - металлическая связь Наконец, имеется еще один тип межмолекулярных связей - металлический : связь положительных ионов решетки металлов со свободными электронами. В биологических объектах этот тип связи не встречается. Из краткого обзора типов связей выясняется одна деталь: важным параметром атома или иона металла - донора электронов, а также атома - акцептоpa электронов является его размер . Не вдаваясь в детали, отметим, что ковалентные радиусы атомов, ионные радиусы металлов и вандерваальсовы радиусы взаимодействующих молекул увеличиваются по мере возрастания их порядкового номера в группах периодической системы. При этом значения радиусов ионов - наименьшие, а вандерваальсовых радиусов - наибольшие. Как правило, при движении вниз по группе радиусы всех элементов увеличиваются, причем как ковалентные, так и вандерваальсовы. Наибольшее значение для биологов и медиков имеют координационные
(донорно-акцепторные
) связи, рассматриваемые координационной химией. Медицинская бионеорганика. Г.К. Барашков Применение хлорида аммония в фармацииАммония хлорид оказывает диуретическое действие; вместе с тем как кислотообразующее средство аммония хлорид является эффективным средством для коррекции алкалоза. Как диуретическое средство аммония хлорид назначают иногда при отеках сердечного происхождения. Аммония хлорид оказывает также отхаркивающее действие и применяется при бронхите, пневмонии и т.п. Гравиметрический анализ Последовательность выполнения работы: 1. Осаждение: 1. В чистый химический стакан берут для анализа раствор FeCl3. 2. Подкисляют его 3-5 мл 2 н. раствора HNO3 и осторожно нагревают, не допуская кипения. 3... Железо в почвах. Методы определения железа Навеску воздушно-сухой почвы 5 г, просеянной через сито с отверстиями 1 мм, помещают в колбу и приливают 250 мл 0,2 Н раствора HCL, перемешивают и настаивают в течение суток. Суспензии фильтруют... Определение диацетила и ацетоина в алкогольных напитках Для стандартизации раствора хлорида железа (III) было проведено комплексонометрическое титрование. Аликвотную часть 1,00 приготовленного раствора хлорида железа (III) помещали в мерную колбу вместимостью 100,0... Комплексные (координационные) соединения чрезвычайно широко распространены в живой и неживой природе, применяются в промышленности, сельском хозяйстве, науке, медицине. Так, хлорофилл - это комплексное соединение магния с порфиринами... Получение тетрахлороцинката аммония и изучение его свойств тетрахлороцинкат аммоний химический приготовление Тетрахлороцинкат аммония применяются в гальваностегии и при пайке, входит в состав флюсов. Пайка -- технологическая операция... Получение тетрахлороцинката аммония и изучение его свойств Существуют несколько способов получения тетрахлороцинката аммония. 1. Первый метод основан на изначальном получении хлорида цинка и дальнейшем взаимодействии его с хлоридом аммония, до растворения осадка... Процесс алкилирования на примере получения этилбензола в присутствии катализатора хлорида алюминия Производительность стадии алкилирования по 100% этилбензолу составляет: или где 10000 - производительность в расчете на 100%-й этилбензол, т/год; 8000 - число рабочих часов; 4 - потери этилбензола на стадиях выделения, %; 106 - молярная масса этилбензола... Получение товарного хлорида кальция из дистиллерной жид-кости содового производства заключается в последовательном выпаривании дистиллерной жидкости от концентрации ~ 10% СаС12 до 67%, требуемой условиями ГОСТ на плавленый продукт... Свойства и получение хлорида кальция Получение плавленого хлорида кальция из маточного щелока хлоратного производства, содержащего в 4 - 5 раз больше СаС12, чем дистиллерная жидкость, является значительно более эконо-мичным. Здесь, однако... Свойства и получение хлорида кальция Гидрооксихлорид кальция образуется при смешении в стехиометрическом отношении хлорида кальция, молотой извести и воды. Его можно выделить из дистиллерной жидкости без выпарки ее или на определенной стадии ее выпари-вания... Свойства и получение хлорида кальция Получение хлорида кальция этим методом заключается в растворении известняка в соляной кислоте, в очистке образующегося «сырого» (неочищенного) раствора СаС12 от примесей и в обезвоживании его. Продукт получается более чистым... ОПРЕДЕЛЕНИЕ Хлорид аммония представляет собой малоустойчивый мелкокристаллический порошок белого цвета. Летуч. Он хорошо растворяется в воде (гидролизуется). Кристаллогидратов не образует. Рис. 1. Хлорид аммония. Внешний вид. Основные характеристики хлорида аммония приведены в таблице ниже: Получение хлорида аммонияПолучение хлорида аммония в промышленных масштабах заключается в упаривании маточного раствора, остающегося после отделения гидрокарбоната натрия, образующегося по следующей реакции: NaCl + H 2 O + CO 2 + NH 3 = NaHCO 3 ↓ + NH 4 Cl. В лабораторных условиях эту соль получают, используя такие реакции, как 8NH 3 + 3Cl 2 = 6NH 4 Cl + N 2 ; NH 3 + HCl = NH 4 Cl. Химические свойства хлорида аммонияХлорид аммония - это средняя соль, образованная слабым основанием - гидроксидом аммония (NH 4 OH) и сильной кислотой - соляной (хлороводородной) (HCl). В водном растворе гидролизуется. Гидролиз протекает по катиону. Наличие катионов Н + свидетельствует о кислом характере среды. NH 4 Cl ↔NH 4 + + Cl — ; NH 4 + + HOH ↔ NH 4 OH + H + ; NH 4 + + Cl — + HOH ↔ NH 4 OH + Cl — + H + ; NH 4 Cl + H 2 O ↔ NH 4 OH +HCl. При нагревании хлорид аммония как бы возгоняется - разлагается на аммиак и хлороводород, которые на холодных частях сосуда вновь соединяются в хлорид аммония: NH 4 Cl↔ NH 3 + HCl. Хлорид аммония разлагается концентрированной серной кислотой и щелочами: 2NH 4 Cl + H 2 SO 4 (conc) = (NH 4) 2 SO 4 + 2HCl; NH 4 Cl + NaOH = NaCl + NH 3 + H 2 O; 2NH 4 Cl + Ca(OH) 2 = 2NH 3 + CaCl 2 + 2H 2 O (t = 200 o C). Он реагирует с хлором (1), типичными металлами (2), оксидами (3) и нитритами металлов (4): NH 4 Cl + 3Cl 2 = Cl 3 N + 4HCl (t = 60 - 70 o C) (1); 2NH 4 Cl + Mg = MgCl 2 + H 2 + 2NH 3 (2); 2NH 4 Cl + 4CuO = N 2 + 4H 2 O + CuCl 2 + 3Cu (t = 300 o C) (3); NH 4 Cl + KNO 2 = N 2 + KCl + 2H 2 O (4). Применение хлорида аммонияХлорид аммония, или нашатырь, применяется в красильном деле, в ситцепечатании, при паянии и лужении, а также в гальванических элементах. Применение хлорида аммония при паянии основано на том, что он способствует удалению с поверхности металла оксидных пленок, благодаря чему припой хорошо пристает к металлу. При соприкосновении сильно нагретого металла с хлоридом аммония оксиды, находящиеся на поверхности металла, либо восстанавливаются, либо переходят в хлориды. Последние, будучи более летучи, чем оксиды, удаляются с поверхности металла. Для случая меди и железа основные происходящие при этом процессы можно выразить такими уравнениями: 4CuO + NH 4 Cl = 3Cu + CuCl 2 + N 2 + 4H 2 O; Fe 3 O 4 + 8NH 4 Cl = FeCl 2 + 2FeCl 3 + 8NH 3 + 4H 2 O. Примеры решения задачПРИМЕР 1
Химическая связь. Кристаллическая решетка Ответами к заданиям являются слово, словосочетание, число или последовательность слов, чисел. Запишите ответ без пробелов, запятых и других дополнительных символов. Начало формы 1 В хлориде аммония присутствуют химические связи: 1. ионные 2. ковалентные полярные 3. ковалентные неполярные 4. Водородные 5. металлические 2 Межмолекулярные водородные связи в жидком состоянии характерны для: 1. водорода 2. Воды 3. Аммиака 4. Ацетальдегида 5. изобутана 3 Ковалентные неполярные химические связи имеются в веществах: 1. белый фосфор 2. ортофосфорная кислота 3. аммиак 4. этиловый спирт 5. сера ромбическая 4 Из предложенного перечня выберите два соединения, в которых присутствует ионная химическая связь. 1. Ca(ClO 2 ) 2 2. HClO 3 3. NH 4 Cl 4. HClO 4 5. C l2 O 7 5 Из предложенного перечня выберите два соединения, в которых присутствует ковалентная неполярная химическая связь. 1. Са 2. Н 2 3. АlСl 3 4. HClO 4 5. Cl 2 6 В сульфате калия присутствуют химические связи: 1. ионные 2. ковалентные неполярные 3. ковалентные полярные 4. водородные 5. металлические 7 И ионные, и ковалентные химические связи имеются в веществе: 1. НСl 2. H 2 SO 4 3. NaOH 4. NH 4 Br 5. С 2 Н 5 ОН 8 Из предложенного перечня выберите два соединения, между молекулами которых образуется водородная связь. 1. фенол 2. диэтиловый эфир 3. Этилацетат 4. муравьиный альдегид 5. муравьиная кислота 9 Из предложенного перечня выберите два соединения, в которых присутствует ковалентная полярная химическая связь. 1. СаСl 2 2. НСl 3. ВаО 4. КСIO 4 5. Сl 2 10 Немолекулярное строение имеют: 1. гидроксид калия 2. Аммиак 3. уксусная кислота 4. азотная кислота 5. графит 11 Ионные связи реализуются в каждом из двух веществ: 1. А l 2 O 3 и FeCl 3 2. K 2 S и NaNO 3 3. KNO 2 и NO 2 4. HF и НСl 5. NaBr и NH 4 F 12 Атомную кристаллическую решётку в твёрдом состоянии имеют: 1. кислород 2. белый фосфор 3. красный фосфор 4. алмаз 5. хлорид натрия 13 Из предложенного перечня выберите два соединения, в которых химическая связь образована за счет общей пары электронов. 1. Ca 2. H 2 O 3. NaCl 4. CaO 5. Cl 2 14 Молекулярное строение имеют: 1. пропанол-2 2. ацетат калия 3. углекислый газ 4. метилат натрия 5. карбонат кальция 15 Все вещества с ионными кристаллическими решётками 1. твёрдые 2. Пластичные 3. относительно летучие 4. хорошо растворимы в воде 5. имеют высокие температуры плавления 16 Из предложенного перечня выберите два соединения, между молекулами которых образуется водородная связь. 1. метан 2. Силан 3. Аммиак 4. Фосфин 5. Вода Конец формы |
 Великая русская река Волга начинается еле
Великая русская река Волга начинается еле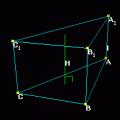 Что такое параллелепипед?
Что такое параллелепипед? Старый Свет - это что такое?
Старый Свет - это что такое?