Tellur atomunun quruluşu. Tellur atomunun strukturu Tellur: Dünya bazarında qiymət dəyişmələrinin dinamikası
TƏrif
Tellur- Dövri Cədvəlin əlli ikinci elementi. Təyinat - Latın "tellurium" dan Te. Beşinci dövrdə, VIA qrupunda yerləşir. Metaloidlər ailəsinə aiddir. Nüvə yükü 52-dir.
Tellur nadir elementlərdən biridir: onun tərkibi yer qabığı cəmi 0,000001% (ağırlıq) təşkil edir.
Sərbəst formada tellur altıbucaqlı qəfəsli gümüşü-ağ rəngli metal kimi kristal maddədir (şək. 1). Kövrək, asanlıqla toz halına salınır. Yarımkeçirici. Sıxlıq 6,25 q/sm3. Ərimə temperaturu 450 o C, qaynama temperaturu 990 o C.
Amorf vəziyyətdə mövcud olduğu bilinir.
düyü. 1. Tellur. Görünüş.
Tellurun atom və molekulyar kütləsi
Maddənin nisbi molekulyar kütləsi (M r) müəyyən bir molekulun kütləsinin karbon atomunun kütləsinin 1/12-dən neçə dəfə çox olduğunu və elementin nisbi atom kütləsinin (A r) neçə dəfə çox olduğunu göstərən rəqəmdir. kimyəvi elementin atomlarının orta kütləsi karbon atomunun 1/12 kütləsindən neçə dəfə böyükdür.
Tellurun sərbəst vəziyyətdə monatomik Te molekulları şəklində mövcud olduğu üçün onun atom və molekulyar kütlələrinin dəyərləri üst-üstə düşür. Onlar 127,60-a bərabərdir.
Tellurun izotopları
Məlumdur ki, tellur təbiətdə səkkiz sabit izotop şəklində tapıla bilər, onlardan ikisi radioaktivdir (128 Te və 130 Te): 120 Te, 122 Te, 123 Te, 124 Te, 125 Te və 126 Te. Onların kütlə nömrələri müvafiq olaraq 120, 122, 123, 124, 125, 126, 128 və 130-dur. Tellurium izotopunun bir atomunun nüvəsi 120 Te əlli iki proton və altmış səkkiz neytrondan ibarətdir və qalan izotoplar ondan yalnız neytronların sayına görə fərqlənir.
Kütləvi nömrələri 105-dən 142-yə qədər olan tellurun süni qeyri-sabit izotopları, həmçinin nüvələrin on səkkiz izomer vəziyyəti var.
Tellur ionları
Tellur atomunun xarici enerji səviyyəsində valentlik olan altı elektron var:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 5s 2 5p 4 .
Kimyəvi qarşılıqlı təsir nəticəsində tellur valentlik elektronlarından imtina edir, yəni. onların donorudur və müsbət yüklü iona çevrilir və ya başqa atomdan elektronları qəbul edir, yəni. onların qəbuledicisidir və mənfi yüklü iona çevrilir:
Te 0 -2e → Te + ;
Te 0 -4e → Te 4+ ;
Te 0 -6e → Te 6+ ;
Te 0 +2e → Te 2- .
Tellur molekulu və atomu
Sərbəst vəziyyətdə tellur monatomik Te molekulları şəklində mövcuddur. Tellur atomunu və molekulunu xarakterizə edən bəzi xüsusiyyətlər bunlardır:
Problemin həlli nümunələri
NÜMUNƏ 1
NÜMUNƏ 2
| Məşq edin | Tellur dioksidin molekulyar formulu TeO 2 olarsa, onu təşkil edən elementlərin kütlə paylarını hesablayın. |
| Həll | Hər hansı bir molekulun tərkibindəki elementin kütlə payı düsturla müəyyən edilir: ω (X) = n × Ar (X) / Cənab (HX) × 100%. |
Bundan əlavə, peşəkar sirk güləşçisi, məşhur metallurq və cərrahiyyə klinikasında məsləhətçi həkim olan dəniz kapitanı haqqında hekayəyə kimsə inanmayacaq. Kimyəvi elementlər dünyasında bu cür müxtəlif peşələr çox yaygın bir hadisədir və Kozma Prutkovun ifadəsi onlara aid deyil: "Mütəxəssis saqqız kimidir: onun tamlığı birtərəflidir." Gəlin xatırlayaq (hekayəmizin əsas obyektindən danışmazdan əvvəl) maşınlarda dəmir və qanda dəmir, dəmir konsentratdır maqnit sahəsi dəmir isə oxranın tərkib hissəsidir... Düzdür, elementlərin “peşəkar hazırlığı” bəzən orta ixtisaslı yoqinin hazırlanmasından xeyli çox vaxt aparırdı. Beləliklə, haqqında danışacağımız 52 nömrəli element uzun illər yalnız əslində nə olduğunu nümayiş etdirmək üçün istifadə edilmişdir, bu element planetimizin adını daşıyır: "tellurium" - latınca "Yer" mənasını verən tellusdan "
Bu element təxminən iki əsr əvvəl aşkar edilmişdir. 1782-ci ildə mədən müfəttişi Frans Cozef Müller (sonralar Baron fon Reyxenşteyn) o zamanlar Avstriya-Macarıstan olan Semigoryedə tapılan qızıl filizini tədqiq etdi. Filizin tərkibini deşifrə etmək o qədər çətin oldu ki, onu Aurum problematicum - "şübhəli qızıl" adlandırdılar. Məhz bu "qızıldan" Müller yeni bir metal təcrid etdi, lakin onun həqiqətən yeni olduğuna tam inam yox idi. (Sonradan məlum oldu ki, Müller başqa bir şeydə yanılır: onun kəşf etdiyi element yeni idi, lakin onu ancaq böyük ehtiyata malik metal kimi təsnif etmək olar.)
Şübhələri aradan qaldırmaq üçün Müller kömək üçün görkəmli mütəxəssis, isveçli mineralog və analitik kimyaçı Berqmana müraciət etdi.
Təəssüf ki, alim göndərilən maddənin analizini başa vurmadan öldü - o illərdə analitik üsullar artıq kifayət qədər dəqiq idi, lakin təhlil çox vaxt apardı.
Digər elm adamları da Müllerin kəşf etdiyi elementi tədqiq etməyə çalışdılar, lakin onun kəşfindən cəmi 16 il sonra o dövrün qabaqcıl kimyaçılarından olan Martin Heinrich Klaproth təkzibedilməz şəkildə bu elementin yeni olduğunu sübut etdi və "tellurium" adını təklif etdi. o.
Həmişə olduğu kimi, element aşkar edildikdən sonra onun tətbiqləri üçün axtarışlar başladı. Göründüyü kimi, atrokimya dövründən qalma köhnə prinsipə əsaslanaraq - dünya aptekdir, fransız Fournier bəzi ciddi xəstəlikləri tellurla, xüsusən də cüzamla müalicə etməyə çalışırdı. Ancaq uğur qazanmadı - yalnız uzun illər sonra tellur həkimlərə bəzi "xırda xidmətlər" göstərə bildi. Daha doğrusu, tellurun özü deyil, tədqiq olunan bakteriyalara müəyyən rəng verən boyalar kimi mikrobiologiyada istifadə olunmağa başlayan tellur turşusu K 2 Te0 3 və Na 2 Te0 3 duzlarıdır. Beləliklə, tellur birləşmələrinin köməyi ilə difteriya çöpü bakteriya kütləsindən etibarlı şəkildə təcrid olunur. Müalicədə deyilsə, heç olmasa diaqnozda 52 nömrəli element həkimlər üçün faydalı oldu.
Ancaq bəzən bu element və daha çox onun bəzi birləşmələri həkimlərə çətinlik yaradır. Tellur olduqca zəhərlidir. Ölkəmizdə havada tellurun icazə verilən maksimal konsentrasiyası 0,01 mq/m3 təşkil edir. Tellur birləşmələrindən ən təhlükəlisi hidrogen tellurid H 2 Te, xoşagəlməz qoxu olan rəngsiz zəhərli qazdır. Sonuncu olduqca təbiidir: tellur kükürdün analoqudur, yəni H 2 Te hidrogen sulfidlə oxşar olmalıdır. Bronxları qıcıqlandırır və sinir sisteminə zərərli təsir göstərir.
Bu xoşagəlməz xüsusiyyətlər tellurun texnologiyaya daxil olmasına və bir çox "peşə" qazanmasına mane olmadı.
Metallurqlar tellurla maraqlanırlar, çünki qurğuşun üçün kiçik əlavələr belə bu vacib metalın gücünü və kimyəvi müqavimətini xeyli artırır. Tellur ilə aşqarlanmış qurğuşun kabel və kimya sənayesi. Beləliklə, içərisi qurğuşun-tellur ərintisi ilə (0,5%-ə qədər Te) örtülmüş sulfat turşusu istehsal edən cihazların istismar müddəti, sadəcə olaraq qurğuşunla örtülmüş eyni qurğulara nisbətən iki dəfə uzundur. Mis və poladın tərkibinə tellurun əlavə edilməsi onların emalını asanlaşdırır.
Şüşə istehsalında tellur şüşəyə qəhvəyi rəng və daha yüksək sınma əmsalı vermək üçün istifadə olunur. Kauçuk sənayesində bəzən rezinlərin vulkanizasiyası üçün kükürdün analoqu kimi istifadə olunur.
Tellur - yarımkeçirici
Bununla belə, bu sənayelər qiymətlərin sıçrayışına və 52 nömrəli elementə tələbata cavabdeh deyildi. Bu sıçrayış əsrimizin 60-cı illərinin əvvəllərində baş verdi. Tellur tipik yarımkeçirici və texnoloji yarımkeçiricidir. Germanium və silikondan fərqli olaraq, nisbətən asanlıqla əriyir (ərimə nöqtəsi 449,8 ° C) və buxarlanır (bir az 1000 ° C-dən aşağı temperaturda qaynar). Nəticə etibarı ilə ondan müasir mikroelektronika üçün xüsusi maraq kəsb edən nazik yarımkeçirici plyonkalar əldə etmək asandır.
Bununla belə, yarımkeçirici kimi təmiz tellur məhdud dərəcədə - bəzi növ sahə effektli tranzistorların istehsalı üçün və qamma şüalanmanın intensivliyini ölçən cihazlarda istifadə olunur. Bundan əlavə, elektron tipli keçiricilik yaratmaq üçün qallium arsenidinə (silikon və germaniumdan sonra üçüncü ən vacib yarımkeçirici) bir tellur çirki qəsdən daxil edilir.
Bəzi telluridlərin - tellurun metallarla birləşmələrinin tətbiq dairəsi daha genişdir. Bismutun telluridləri Bi 2 Te 3 və sürmə Sb 2 Te 3 termoelektrik generatorlar üçün ən vacib materiallara çevrilmişdir. Bunun niyə baş verdiyini izah etmək üçün gəlin fizika və tarix sahəsinə qısaca nəzər salaq.
Əsr yarım əvvəl (1821-ci ildə) alman fiziki Seebek kəşf etdi ki, müxtəlif materiallardan ibarət olan, təmasları müxtəlif temperaturda olan qapalı elektrik dövrəsində elektrohərəkətçi qüvvə yaranır (buna termo-EMF deyilir). 12 il sonra İsveçrəli Peltier bu effekti kəşf etdi. əks təsir Seebeck: nə vaxt elektrik müxtəlif materiallardan ibarət bir dövrə vasitəsilə axır, təmas nöqtələrində adi Joule istiliyinə əlavə olaraq müəyyən miqdarda istilik ayrılır və ya udulur (cərəyin istiqamətindən asılı olaraq).
Təxminən 100 il ərzində bu kəşflər “özlüyündə şeylər”, maraqlı faktlar olaraq qaldı, başqa heç nə. Və bunu demək mübaliğə olmaz yeni həyat Bu təsirlərin hər ikisi akademik A.F.İoffe və onun həmkarları termoelementlərin istehsalı üçün yarımkeçirici materiallardan istifadə nəzəriyyəsini inkişaf etdirdikdən sonra başladı. Və tezliklə bu nəzəriyyə real termoelektrik generatorlarda və müxtəlif təyinatlı termoelektrik soyuducularda təcəssüm olundu.
Xüsusilə, vismut, qurğuşun və sürmənin telluridlərindən istifadə edən termoelektrik generatorlar Yerin süni peyklərini, naviqasiya və meteoroloji qurğuları, magistral boru kəmərləri üçün katod mühafizə vasitələrini enerji ilə təmin edir. Eyni materiallar bir çox elektron və mikroelektron cihazlarda istənilən temperaturu saxlamağa kömək edir.
IN son illər Daha bir şey böyük maraq doğurur kimyəvi birləşmə yarımkeçirici xüsusiyyətlərə malik tellur kadmium tellurid CdTe-dir. Bu material günəş batareyaları, lazerlər, fotorezistorlar və radioaktiv radiasiya sayğaclarının istehsalı üçün istifadə olunur. Kadmium tellurid həm də Han effektinin nəzərəçarpacaq dərəcədə təzahür etdiyi bir neçə yarımkeçiricidən biri olması ilə məşhurdur.
Sonuncunun mahiyyəti ondan ibarətdir ki, müvafiq yarımkeçiricinin kiçik bir boşqabının kifayət qədər güclü elektrik sahəsinə daxil edilməsi yüksək tezlikli radio emissiyasının yaranmasına səbəb olur. Hahn effekti artıq radar texnologiyasında tətbiq tapmışdır.
Sonda deyə bilərik ki, kəmiyyətcə tellurun əsas “peşəsi” qurğuşun və digər metalların ərintisidir. Keyfiyyət baxımından əsas şey, əlbəttə ki, tellur və telluridlərin yarımkeçiricilər kimi işləməsidir.
Faydalı qarışıq
Dövri cədvəldə tellur VI qrupun əsas alt qrupunda kükürd və selenin yanında yerləşir. Bu üç element kimyəvi xassələrə görə oxşardır və təbiətdə çox vaxt bir-birini müşayiət edir. Lakin yer qabığında kükürdün payı 0,03%, selenium cəmi 10-5%, tellur hətta daha az miqyasda - 10-6% təşkil edir. Təbii ki, tellur, selenium kimi, ən çox təbii kükürd birləşmələrində - çirk kimi olur. Bununla belə (tellurun kəşf edildiyi mineralı xatırlayın) qızıl, gümüş, mis və digər elementlərlə təmasda olur. Planetimizdə qırx tellur mineralının 110-dan çox yatağı aşkar edilmişdir. Amma həmişə ya selen, ya qızıl, ya da başqa metallarla birlikdə hasil edilir.
Rusiyada Peçenqa və Monçeqorskun mis-nikel tellur tərkibli filizləri, Altayın tellur tərkibli qurğuşun-sink filizləri və bir sıra başqa yataqlar məlumdur.
Tellurium mis filizindən blister misin elektroliz yolu ilə təmizlənməsi mərhələsində təcrid olunur. Çöküntü - çamur - elektrolizatorun dibinə düşür. Bu çox bahalı ara məhsuldur. Kanada zavodlarından birinin lil tərkibini göstərmək üçün: 49,8% mis, 1,976% qızıl, 10,52% gümüş, 28,42% selen və 3,83% tellur. Çamurun bütün bu qiymətli komponentləri ayrılmalıdır və bunun bir neçə yolu var. Onlardan biri budur.
Çamur sobada əridilir və hava ərimədən keçir. Qızıl və gümüşdən başqa metallar oksidləşərək şlaklara çevrilir. Selenium və tellur da oksidləşir, lakin uçucu oksidlərə çevrilir, onlar xüsusi cihazlarda (skrubberlər) tutulur, sonra həll edilir və turşulara - selenium H 2 SeO3 və tellur H 2 TeO3 -ə çevrilir. Kükürd dioksidi S0 2 bu məhluldan keçərsə, reaksiyalar baş verəcəkdir
H 2 Se0 3 + 2S0 2 + H 2 0 → Se ↓ + 2H 2 S0 4.
H2Te03 + 2S02 + H20 → Te ↓ + 2H 2 S0 4.
Tellur və selen eyni vaxtda düşür, bu çox arzuolunmazdır - onlara ayrıca ehtiyacımız var. Buna görə də, proses şəraiti elə seçilir ki, kimyəvi termodinamika qanunlarına uyğun olaraq ilk növbədə selenium azalsın. Bu, məhlula əlavə edilən xlorid turşusunun optimal konsentrasiyasını seçməklə kömək edir.
Tellurium daha sonra yatırılır. Nəticədə yaranan boz toz, təbii ki, müəyyən miqdarda selenium və əlavə olaraq kükürd, qurğuşun, mis, natrium, silisium, alüminium, dəmir, qalay, sürmə, vismut, gümüş, maqnezium, qızıl, arsen, xlor ehtiva edir. Tellur əvvəlcə kimyəvi üsullarla, sonra distillə və ya zona əriməsi ilə bütün bu elementlərdən təmizlənməlidir. Təbii ki, tellur müxtəlif filizlərdən müxtəlif üsullarla çıxarılır.
Tellur zərərlidir
Tellurdan getdikcə daha geniş istifadə olunur və buna görə də onunla işləyənlərin sayı artır. 52 nömrəli element haqqında hekayənin birinci hissəsində biz artıq tellurun və onun birləşmələrinin toksikliyini qeyd etdik. Gəlin bu barədə daha ətraflı danışaq - məhz ona görə ki, getdikcə daha çox insan tellurla işləməli olur. Tellurun sənaye zəhəri olması ilə bağlı dissertasiyadan bir sitat belədir: tellur aerozolunun yeridilmiş ağ siçovullar “narahatlıq nümayiş etdirir, asqırır, üzlərini ovuşdurur, letarji və yuxulu olurlar”. Tellurium insanlara oxşar təsir göstərir.
Və özüm tellur və onun əlaqələri müxtəlif “kalibrli” problemlər gətirə bilər. Onlar, məsələn, keçəlliyə səbəb olur, qan tərkibinə təsir edir və müxtəlif ferment sistemlərini bloklaya bilir. Elementar tellur ilə xroniki zəhərlənmənin simptomları ürəkbulanma, yuxululuq, arıqlamadır; çıxarılan hava alkil telluridlərin pis, sarımsaqlı qoxusunu alır.
Kəskin tellur zəhərlənməsi zamanı qlükoza ilə serum venadaxili yeridilir., və bəzən hətta morfin. Askorbin turşusu profilaktik olaraq istifadə olunur. Lakin əsas qarşısının alınması cihazların etibarlı möhürlənməsi, tellur və onun birləşmələrinin iştirak etdiyi proseslərin avtomatlaşdırılmasıdır.

52 nömrəli element bir çox fayda gətirir və buna görə də diqqətə layiqdir. Ancaq onunla işləmək ehtiyatlılıq, aydınlıq və yenə də cəmlənmiş diqqət tələb edir.
TELLURIN GÖRÜNÜŞÜ. Kristal tellur ən çox antimona bənzəyir. Rəngi gümüşü-ağdır. Kristallar altıbucaqlıdır, onların içindəki atomlar spiral zəncirlər əmələ gətirir və bir-birinə bağlıdır kovalent bağlarən yaxın qonşularla. Buna görə də elementar tellur qeyri-üzvi polimer hesab edilə bilər. Kristal tellur metal parıltı ilə xarakterizə olunur, baxmayaraq ki, kimyəvi xassələri kompleksinə görə onu qeyri-metal kimi təsnif etmək olar. Tellur kövrəkdir və toz halına gətirmək olduqca asandır. Tellurun amorf modifikasiyasının mövcudluğu məsələsi aydın şəkildə həll edilməmişdir. Tellur və ya tellur turşusundan tellur reduksiya edildikdə, bir çöküntü əmələ gəlir, lakin bu hissəciklərin həqiqətən amorf və ya sadəcə çox kiçik kristallar olduğu hələ də aydın deyil.
İKİ RƏNGLİ ANHİDRİD. Kükürdün analoquna uyğun olaraq, tellur 2-, 4+ və 6+ və daha az 2+ valentlik nümayiş etdirir. Tellur monoksid TeO yalnız qaz halında ola bilər və asanlıqla Te0 2-ə qədər oksidləşir. Bu, 733 ° C-də parçalanmadan əriyən ağ, higroskopik olmayan, tamamilə sabit kristal maddədir; polimer quruluşa malikdir.
Tellurium dioksidi suda demək olar ki, həll olunmur - suyun 1,5 milyon hissəsinə Te0 2-nin yalnız bir hissəsi məhlula keçir və cüzi konsentrasiyalı zəif tellur turşusunun H 2 Te0 3 məhlulu əmələ gəlir. Həm də zəif ifadə olunur turşu xüsusiyyətləri və tellur turşusu
H 6 TeO 6 . Bu düstur (və ona H 2 TeO 4 deyil, suda yaxşı həll olan Ag 6 Te0 6 və Hg 3 Te0 6 tərkibli duzlar alındıqdan sonra təyin edilmişdir. Tellur turşusu əmələ gətirən TeO3 anhidridi suda praktiki olaraq həll olunmur. .Bu maddə iki modifikasiyada mövcuddur-sarı və boz:α-TeO3 və β-TeO3.Boz tellur anhidridi çox dayanıqlıdır:qızdırdıqda belə turşuların və qatılaşdırılmış qələvilərin təsirinə məruz qalmır.Sarı sortdan qaynadıb təmizlənir. qatılaşdırılmış kaustik kaliumda qarışıq.
İKİNCİ İSTİSNA. Mendeleyev dövri cədvəli yaratarkən tellur və onun qonşusu yodu (eləcə də arqon və kalium) VI və VII qruplara onlara uyğun deyil, əksinə yerləşdirdi. atom çəkiləri. Həqiqətən də tellurun atom kütləsi 127,61, yodunki isə 126,91-dir.Bu o deməkdir ki, yod tellurun arxasında yox, onun qarşısında olmalıdır. Mendeleyev isə haqlı olduğuna şübhə etmirdi
mülahizələrinin düzgünlüyü, çünki bu elementlərin atom çəkilərinin kifayət qədər dəqiq müəyyən edilmədiyinə inanırdı. Mendeleyevin yaxın dostu, çex kimyaçısı Boquslav Brauner tellur və yodun atom çəkilərini diqqətlə yoxladı, lakin onun məlumatları əvvəlkilərlə üst-üstə düşdü. Qaydanı təsdiq edən istisnaların etibarlılığı yalnız əsas olduqda müəyyən edilmişdir Dövri Cədvəl Hər iki elementin izotop tərkibi məlum olanda atom çəkiləri deyil, nüvə yükləri əmələ gəlirdi. Tellur, yoddan fərqli olaraq, ağır izotoplarla üstünlük təşkil edir.
Yeri gəlmişkən, izotonlar haqqında. Hal-hazırda 52 nömrəli elementin 22 izotopu məlumdur. Onlardan səkkizi - kütlə nömrələri 120, 122, 123, 124, 125, 126, 128 və 130 - sabitdir. Son iki izotop ən çox yayılmışdır: müvafiq olaraq 31,79 və 34,48%.
TELLUR FAYDALLARI. Tellurun Yer üzündə seleniumdan əhəmiyyətli dərəcədə az olmasına baxmayaraq, 52 nömrəli elementin həmkarından daha çox mineral məlumdur. Tellur mineralları iki növdür: ya telluridlər, ya da yer qabığında telluridlərin oksidləşməsinin məhsulları. Birincilər arasında bir neçə təbii qızıl birləşmələri arasında olan kalaverit AuTe 2 və krennerit (Au, Ag) Te2 var. Bizmut, qurğuşun və civənin təbii telluridləri də məlumdur. Doğma tellur təbiətdə çox nadir hallarda olur. Bu elementin kəşfindən əvvəl də bəzən sulfid filizlərində tapılırdı, lakin düzgün müəyyən edilə bilməzdi. Tellur minerallarının praktik əhəmiyyəti yoxdur - bütün sənaye tellurları digər metalların filizlərinin emalının əlavə məhsuludur.
| Tellur | |
|---|---|
| Atom nömrəsi | 52 |
| Sadə bir maddənin görünüşü | |
| Atomun xassələri | |
| Atom kütləsi (molar kütlə) |
127.6 a. e.m (q/mol) |
| Atom radiusu | axşam 160 |
| İonlaşma enerjisi (ilk elektron) |
869,0 (9,01) kJ/mol (eV) |
| Elektron konfiqurasiya | 4d 10 5s 2 5p 4 |
| Kimyəvi xassələri | |
| Kovalent radius | axşam 136 |
| İon radiusu | (+6e) 56,211 (-2e) pm |
| Elektromənfilik (Paulinqə görə) |
2,1 |
| Elektrod potensialı | 0 |
| Oksidləşmə halları | +6, +4, +2 |
| Sadə maddənin termodinamik xassələri | |
| Sıxlıq | 6,24 /sm³ |
| Molar istilik tutumu | 25,8 J/(mol) |
| İstilikkeçirmə | 14,3 Vt/(·) |
| Ərimə temperaturu | 722,7 |
| Ərimə istiliyi | 17,91 kJ/mol |
| Qaynama temperaturu | 1 263 |
| Buxarlanma istiliyi | 49,8 kJ/mol |
| Molar həcm | 20,5 sm³/mol |
| Sadə maddənin kristal qəfəsi | |
| Şəbəkə quruluşu | altıbucaqlı |
| Şəbəkə parametrləri | 4,450 |
| c/a nisbəti | 1,330 |
| Debay temperaturu | yox |
Tellur— dövri cədvəldə atom nömrəsi 52 və atom kütləsi 127,60 olan kimyəvi element; Te (Tellurium) simvolu ilə işarələnmiş metaloid ailəsinə aiddir.
Hekayə
İlk dəfə 1782-ci ildə Transilvaniyanın qızıl filizlərində mədən müfəttişi Franz Cozef Müller (sonralar Baron von Reyxenşteyn) tərəfindən Avstriya-Macarıstan ərazisində aşkar edilmişdir. 1798-ci ildə Martin Heinrich Klaproth telluru təcrid etdi və onun ən vacib xüsusiyyətlərini təyin etdi.
adının mənşəyi
Latın dilindən tellus, Genitive telluris, Yer.
Təbiətdə olmaq
Doğma tellur da selen və kükürdlə birlikdə baş verir (Yapon tellur kükürdünün tərkibində 0,17% Te və 0,06% Se var).
Tellurun mühüm mənbəyi mis və qurğuşun filizləridir.
Qəbz
Əsas mənbə mis və qurğuşunun elektrolitik emalı nəticəsində yaranan çamurdur. Çamur yandırılır, tellur xlorid turşusu ilə yuyulan şlakda qalır. Tellurium kükürd dioksidi SO 2-ni keçirərək yaranan xlorid turşusu məhlulundan təcrid olunur.
Selen və telluru ayırmaq üçün əlavə edin sulfat turşusu. Bu halda tellur dioksidi TeO 2 düşür, H 2 SeO 3 isə məhlulda qalır.
Tellur TeO2 oksidindən kömürlə reduksiya olunur.
Telluru kükürddən və selendən təmizləmək üçün onun qələvi mühitdə bir azaldıcı agentin (Al) təsiri altında həll olunan disodium ditellurid Na 2 Te 2-yə çevrilmə qabiliyyəti istifadə olunur:
6Te + 2Al + 8NaOH = 3Na 2 Te 2 + 2Na.
Teluru çökdürmək üçün məhluldan hava və ya oksigen keçir:
2Na 2 Te 2 + 2H 2 O + O 2 = 4Te + 4NaOH.
Xüsusi saflıqda tellur əldə etmək üçün onu xlorlayırlar
Te + 2Cl 2 = TeCl 4.
Yaranan tetraklorid distillə və ya rektifikasiya yolu ilə təmizlənir. Sonra tetraklorid su ilə hidrolizə olunur:
TeCl 4 + 2H 2 O = TeO 2 + 4HCl,
və nəticədə TeO 2 hidrogenlə azaldılır:
TeO 2 + 4H 2 = Te + 2H 2 O.
Qiymətlər
Tellur nadir elementdir və kiçik istehsal həcmi ilə əhəmiyyətli tələbat onun yüksək qiymətini müəyyən edir (təmizliyindən asılı olaraq hər kq üçün təxminən 200-300 dollar), lakin buna baxmayaraq, onun tətbiqi sahələri daim genişlənir.
Fiziki-kimyəvi xüsusiyyətləri
Tellur metal parıltısı olan kövrək, gümüşü-ağ maddədir. İncə təbəqələrdə işığa məruz qaldıqda qırmızı-qəhvəyi, cütlükdə qızılı-sarı olur.
Kimyəvi cəhətdən tellur kükürddən daha az aktivdir. Qələvilərdə həll olunur, azot və sulfat turşularının təsirinə həssasdır, lakin seyreltilmiş vəziyyətdədir. xlorid turşusu azca həll edir. Tellur metalı 100°C-də su ilə reaksiyaya girməyə başlayır və toz halında otaq temperaturunda belə havada oksidləşərək Te0 2 oksidi əmələ gətirir.
Havada qızdırıldıqda tellur yanır və Te0 2 əmələ gətirir. Bu güclü birləşmə tellurun özündən daha az uçucudur. Buna görə də telluru oksidlərdən təmizləmək üçün 500-600 ° C-də axan hidrogenlə reduksiya edilir.
Ərinmiş vəziyyətdə tellur kifayət qədər təsirsizdir, ona görə də əridərkən konteyner materialları kimi qrafit və kvars istifadə olunur.
Ərizə
Ərintilər
Tellurium artan çeviklik və möhkəmliyə malik qurğuşun ərintilərinin istehsalında istifadə olunur (məsələn, kabellərin istehsalında istifadə olunur). 0,05% tellurun tətbiqi ilə sulfat turşusunun təsiri altında əriməsi nəticəsində qurğuşun itkisi 10 dəfə azalır və bundan qurğuşun-turşu akkumulyatorlarının istehsalında istifadə olunur. Tellurla qatlanmış qurğuşunun plastik deformasiya ilə emal edildikdə yumşalmaması da vacibdir və bu, soyuq kəsmə üsulundan istifadə edərək akkumulyator plitələrinin cərəyan kollektorlarının istehsalı texnologiyasından istifadə etməyə və batareyanın xidmət müddətini və spesifik xüsusiyyətlərini əhəmiyyətli dərəcədə artırmağa imkan verir. .
Termoelektrik materiallar
Vismut tellurid monokristal
Yarımkeçirici materialların və xüsusilə qurğuşun, vismut, sürmə və sezium telluridlərinin istehsalında da onun rolu böyükdür. Yaxın illərdə lantanid-telluridlərin, onların ərintilərinin və metal selenidlərlə ərintilərinin istehsalı çox yüksək (72-78%-ə qədər) səmərəliliyə malik olan termoelektrik generatorların istehsalı üçün çox mühüm əhəmiyyət kəsb edəcəkdir ki, bu da onlardan sənayedə istifadə etməyə imkan verəcəkdir. enerji sektorunda və avtomobil sənayesində.
Məsələn, bu yaxınlarda manqan telluridində (500 μV/K) və onun vismut, sürmə və lantanidlərin selenidləri ilə birləşməsində çox yüksək istilik emf aşkar edilmişdir ki, bu da termogeneratorlarda nəinki çox yüksək effektivliyə nail olmağa, həm də yarımkeçirici soyuducu bir mərhələdə artıq həyata kriogen (maye azot temperatur səviyyəsi) temperatur aşağı soyutma və daha aşağı. Son illərdə yarımkeçirici soyuducuların istehsalı üçün tellur əsaslı ən yaxşı material tellur ərintisi olmuşdur.
Bundan əlavə, peşəkar sirk güləşçisi, məşhur metallurq və cərrahiyyə klinikasında məsləhətçi həkim olan dəniz kapitanı haqqında hekayəyə kimsə inanmayacaq. Kimyəvi elementlər dünyasında bu cür müxtəlif peşələr çox yaygın bir hadisədir və Kozma Prutkovun ifadəsi onlara aid deyil: "Mütəxəssis saqqız kimidir: onun tamlığı birtərəflidir." Gəlin xatırlayaq ki, (hekayəmizin əsas obyektindən danışmamışdan əvvəl) maşınlarda dəmir, qanda dəmir, dəmir maqnit sahəsinin konsentratoru, dəmir isə oxranın tərkib hissəsidir... Düzdür, elementlərin “peşəkar hazırlığı” bəzən aralıq yoga hazırlamaqdan daha çox vaxt apardı. Beləliklə, haqqında danışacağımız 52 nömrəli element uzun illər yalnız əslində nə olduğunu nümayiş etdirmək üçün istifadə edilmişdir, bu element planetimizin adını daşıyır: "tellurium" - latınca "Yer" mənasını verən tellusdan.
Bu element təxminən iki əsr əvvəl aşkar edilmişdir. 1782-ci ildə mədən müfəttişi Frans Cozef Müller (sonralar Baron fon Reyxenşteyn) o zamanlar Avstriya-Macarıstan olan Semigoryedə tapılan qızıl filizini tədqiq etdi. Filizin tərkibini deşifrə etmək o qədər çətin oldu ki, onu Aurum problematicum - "şübhəli qızıl" adlandırdılar. Məhz bu "qızıldan" Müller yeni bir metal təcrid etdi, lakin onun həqiqətən yeni olduğuna tam inam yox idi. (Sonradan məlum oldu ki, Müller başqa bir şeydə yanılır: onun kəşf etdiyi element yeni idi, lakin onu ancaq böyük ehtiyata malik metal kimi təsnif etmək olar.)
Şübhələri aradan qaldırmaq üçün Müller kömək üçün görkəmli mütəxəssis, isveçli mineralog və analitik kimyaçı Berqmana müraciət etdi.
Təəssüf ki, alim göndərilən maddənin analizini başa vurmadan öldü - o illərdə analitik üsullar artıq kifayət qədər dəqiq idi, lakin təhlil çox vaxt apardı.
Digər elm adamları da Müllerin kəşf etdiyi elementi tədqiq etməyə çalışdılar, lakin onun kəşfindən cəmi 16 il sonra o dövrün qabaqcıl kimyaçılarından olan Martin Heinrich Klaproth bu elementin əslində yeni olduğunu təkzibolunmaz sübut etdi və ona “tellurium” adını təklif etdi. .
Həmişə olduğu kimi, element aşkar edildikdən sonra onun tətbiqləri üçün axtarışlar başladı. Göründüyü kimi, atrokimya dövründən qalma köhnə prinsipə əsaslanaraq - dünya aptekdir, fransız Fournier bəzi ciddi xəstəlikləri tellurla, xüsusən də cüzamla müalicə etməyə çalışırdı. Ancaq uğur qazanmadı - yalnız uzun illər sonra tellur həkimlərə bəzi "xırda xidmətlər" göstərə bildi. Daha doğrusu, tellurun özü deyil, tədqiq olunan bakteriyalara müəyyən rəng verən boyalar kimi mikrobiologiyada istifadə olunmağa başlayan tellur turşusu K 2 TeO 3 və Na 2 TeO 3 duzları. Beləliklə, tellur birləşmələrinin köməyi ilə difteriya çöpü bakteriya kütləsindən etibarlı şəkildə təcrid olunur. Müalicədə deyilsə, heç olmasa diaqnozda 52 nömrəli element həkimlər üçün faydalı oldu.
Ancaq bəzən bu element və daha çox onun bəzi birləşmələri həkimlərə çətinlik yaradır. Tellur olduqca zəhərlidir. Ölkəmizdə havada tellurun icazə verilən maksimal konsentrasiyası 0,01 mq/m3 hesab olunur. Tellur birləşmələrindən ən təhlükəlisi hidrogen tellurid H 2 Te, xoşagəlməz qoxu olan rəngsiz zəhərli qazdır. Sonuncu olduqca təbiidir: tellur kükürdün analoqudur, yəni H 2 Te hidrogen sulfidlə oxşar olmalıdır. Bronxları qıcıqlandırır və sinir sisteminə zərərli təsir göstərir.
Bu xoşagəlməz xüsusiyyətlər tellurun texnologiyaya daxil olmasına və bir çox "peşə" qazanmasına mane olmadı.
Metallurqlar tellurla maraqlanırlar, çünki qurğuşun üçün kiçik əlavələr belə bu vacib metalın gücünü və kimyəvi müqavimətini xeyli artırır. Tellurla aşqarlanmış qurğuşun kabel və kimya sənayesində istifadə olunur. Beləliklə, içərisi qurğuşun-tellur ərintisi ilə (0,5%-ə qədər Te) örtülmüş sulfat turşusu istehsal edən cihazların istismar müddəti, sadəcə olaraq qurğuşunla örtülmüş eyni qurğulara nisbətən iki dəfə uzundur. Mis və poladın tərkibinə tellurun əlavə edilməsi onların emalını asanlaşdırır.
Şüşə istehsalında tellur şüşəyə qəhvəyi rəng və daha yüksək sınma əmsalı vermək üçün istifadə olunur. Kauçuk sənayesində bəzən rezinlərin vulkanizasiyası üçün kükürdün analoqu kimi istifadə olunur.
Tellur yarımkeçiricidir
Bununla belə, bu sənayelər qiymətlərin sıçrayışına və 52 nömrəli elementə tələbata cavabdeh deyildilər. Bu sıçrayış əsrimizin 60-cı illərinin əvvəllərində baş verdi. Tellur tipik yarımkeçirici və texnoloji yarımkeçiricidir. Germanium və silisiumdan fərqli olaraq, nisbətən asanlıqla əriyir (ərimə nöqtəsi 449,8 ° C) və buxarlanır (bir az 1000 ° C-də qaynar). Nəticə etibarı ilə ondan müasir mikroelektronika üçün xüsusi maraq kəsb edən nazik yarımkeçirici plyonkalar əldə etmək asandır.
Bununla belə, yarımkeçirici kimi təmiz tellur məhdud dərəcədə - bəzi növ sahə effektli tranzistorların istehsalı üçün və qamma şüalanmanın intensivliyini ölçən cihazlarda istifadə olunur. Bundan əlavə, elektron tipli keçiricilik yaratmaq üçün qallium arsenidinə (silikon və germaniumdan sonra üçüncü ən vacib yarımkeçirici) qəsdən tellur çirki daxil edilir.
* Yarımkeçiricilərə xas olan iki keçiricilik növü "Germanium" məqaləsində ətraflı təsvir edilmişdir.
Bəzi telluridlərin - tellurun metallarla birləşmələrinin tətbiq dairəsi daha genişdir. Bismutun telluridləri Bi 2 Te 3 və sürmə Sb 2 Te 3 termoelektrik generatorlar üçün ən vacib materiallara çevrilmişdir. Bunun niyə baş verdiyini izah etmək üçün gəlin fizika və tarix sahəsinə qısaca nəzər salaq.
Əsr yarım əvvəl (1821-ci ildə) alman fiziki Seebek kəşf etdi ki, müxtəlif materiallardan ibarət olan, təmasları müxtəlif temperaturda olan qapalı elektrik dövrəsində elektrohərəkətçi qüvvə yaranır (buna termo-EMF deyilir). 12 ildən sonra isveçrəli Peltier Seebeck effektinə əks effekt kəşf etdi: elektrik cərəyanı müxtəlif materiallardan ibarət dövrədən keçdikdə, təmas nöqtələrində adi Joule istiliyinə əlavə olaraq müəyyən miqdarda istilik ayrılır və ya udulmuş (cərəyin istiqamətindən asılı olaraq).
Təxminən 100 il ərzində bu kəşflər “özlüyündə şeylər”, maraqlı faktlar olaraq qaldı, başqa heç nə. Və bu təsirlərin hər ikisi üçün yeni həyat Sosialist Əməyi Qəhrəmanı, akademik A.F. İoffe və onun həmkarları termoelementlərin istehsalı üçün yarımkeçirici materiallardan istifadə nəzəriyyəsini inkişaf etdirdilər. Və tezliklə bu nəzəriyyə real termoelektrik generatorlarda və müxtəlif təyinatlı termoelektrik soyuducularda təcəssüm olundu.
Xüsusilə, vismut, qurğuşun və sürmənin telluridlərindən istifadə edən termoelektrik generatorlar Yerin süni peyklərini, naviqasiya və meteoroloji qurğuları, magistral boru kəmərləri üçün katod mühafizə vasitələrini enerji ilə təmin edir. Eyni materiallar bir çox elektron və mikroelektron cihazlarda istənilən temperaturu saxlamağa kömək edir.
Son illərdə yarımkeçirici xassələrə malik başqa bir tellur kimyəvi birləşməsi, kadmium tellurid CdTe böyük marağa səbəb olmuşdur. Bu material günəş batareyaları, lazerlər, fotorezistorlar və radiasiya sayğaclarının istehsalı üçün istifadə olunur. Kadmium tellurid həm də Han effektinin nəzərəçarpacaq dərəcədə təzahür etdiyi bir neçə yarımkeçiricidən biri olması ilə məşhurdur.
Sonuncunun mahiyyəti ondan ibarətdir ki, müvafiq yarımkeçiricinin kiçik bir boşqabının kifayət qədər güclü elektrik sahəsinə daxil edilməsi yüksək tezlikli radio emissiyasının yaranmasına səbəb olur. Hahn effekti artıq radar texnologiyasında tətbiq tapmışdır.
Sonda deyə bilərik ki, kəmiyyətcə tellurun əsas “peşəsi” qurğuşun və digər metalların ərintisidir. Keyfiyyət baxımından əsas şey, əlbəttə ki, tellur və telluridlərin yarımkeçiricilər kimi işləməsidir.
Faydalı qarışıq
Dövri cədvəldə tellur VI qrupun əsas alt qrupunda kükürd və selenin yanında yerləşir. Bu üç element kimyəvi xassələrə görə oxşardır və təbiətdə çox vaxt bir-birini müşayiət edir. Lakin yer qabığında kükürdün payı 0,03%, selenium cəmi 10-5%, tellur isə daha az miqyasdadır - 10-6%. Təbii ki, tellur, selenium kimi, ən çox təbii kükürd birləşmələrində - çirk kimi olur. Bununla belə (tellurun kəşf edildiyi mineralı xatırlayın) qızıl, gümüş, mis və digər elementlərlə təmasda olur. Planetimizdə qırx tellur mineralının 110-dan çox yatağı aşkar edilmişdir. Amma həmişə ya selen, ya qızıl, ya da başqa metallarla birlikdə hasil edilir.
SSRİ-də mis-nikel tellur tərkibli Peçenqa və Monçeqorsk filizləri, Altayın tellur tərkibli qurğuşun-sink filizləri və bir sıra başqa yataqlar məlumdur.
Tellurium mis filizindən blister misin elektroliz yolu ilə təmizlənməsi mərhələsində təcrid olunur. Çöküntü - çamur - elektrolizatorun dibinə düşür. Bu çox bahalı ara məhsuldur. Kanada zavodlarından birinin lil tərkibini göstərmək üçün: 49,8% mis, 1,976% qızıl, 10,52% gümüş, 28,42% selen və 3,83% tellur. Çamurun bütün bu qiymətli komponentləri ayrılmalıdır və bunun bir neçə yolu var. Onlardan biri budur.
Çamur sobada əridilir və hava ərimədən keçir. Qızıl və gümüşdən başqa metallar oksidləşərək şlaklara çevrilir. Selenium və tellur da oksidləşir, lakin uçucu oksidlərə çevrilir, onlar xüsusi cihazlarda (skrubberlər) tutulur, sonra həll edilir və turşulara - selenium H 2 SeO 3 və tellur H 2 TeO 3 -ə çevrilir. Kükürd dioksidi SO2 bu məhluldan keçərsə, aşağıdakı reaksiyalar baş verəcək:
H 2 SeO 3 + 2SO 2 + H 2 O → Se ↓ + 2H 2 SO 4,
H 2 TeO 3 + 2SO 2 + H 2 O → Te ↓ + 2H 2 SO 4.
Tellur və selen eyni vaxtda düşür, bu çox arzuolunmazdır - onlara ayrıca ehtiyacımız var. Buna görə də, proses şəraiti elə seçilir ki, kimyəvi termodinamika qanunlarına uyğun olaraq ilk növbədə selenium azalsın. Bu, məhlula əlavə edilən xlorid turşusunun optimal konsentrasiyasını seçməklə kömək edir.
Tellurium daha sonra yatırılır. Nəticədə yaranan boz toz, təbii ki, müəyyən miqdarda selenium və əlavə olaraq kükürd, qurğuşun, mis, natrium, silisium, alüminium, dəmir, qalay, sürmə, vismut, gümüş, maqnezium, qızıl, arsen, xlor ehtiva edir. Tellur əvvəlcə kimyəvi üsullarla, sonra distillə və ya zona əriməsi ilə bütün bu elementlərdən təmizlənməlidir. Təbii ki, tellur müxtəlif filizlərdən müxtəlif üsullarla çıxarılır.
Tellur zərərlidir
Tellurdan getdikcə daha geniş istifadə olunur və buna görə də onunla işləyənlərin sayı artır. 52 nömrəli element haqqında hekayənin birinci hissəsində biz artıq tellurun və onun birləşmələrinin toksikliyini qeyd etdik. Gəlin bu barədə daha ətraflı danışaq, çünki getdikcə daha çox insan tellurla işləməli olur. Tellurun sənaye zəhəri olması ilə bağlı dissertasiyadan bir sitat belədir: tellur aerozolunun yeridilmiş ağ siçovullar “narahatlıq nümayiş etdirir, asqırır, üzlərini ovuşdurur, letarji və yuxulu olurlar”. Tellurium insanlara oxşar təsir göstərir.
Tellurun özü və onun birləşmələri müxtəlif "kalibrli" problemlər yarada bilər. Onlar, məsələn, keçəlliyə səbəb olur, qan tərkibinə təsir edir və müxtəlif ferment sistemlərini bloklaya bilir. Elementar tellur ilə xroniki zəhərlənmənin simptomları ürəkbulanma, yuxululuq, arıqlamadır; çıxarılan hava alkil telluridlərin pis, sarımsaqlı qoxusunu alır.
Kəskin tellur zəhərlənməsi zamanı qlükoza ilə serum, bəzən hətta morfin venadaxili yeridilir. Askorbin turşusu profilaktik olaraq istifadə olunur. Lakin əsas qarşısının alınması cihazların qutularının bağlanması, tellurun və onun birləşmələrinin iştirak etdiyi proseslərin avtomatlaşdırılmasıdır.
52 nömrəli element bir çox fayda gətirir və buna görə də diqqətə layiqdir. Ancaq onunla işləmək ehtiyatlılıq, aydınlıq və yenə də cəmlənmiş diqqət tələb edir.
Tellurun görünüşü
Kristal tellur ən çox antimona bənzəyir. Rəngi gümüşü-ağdır. Kristallar altıbucaqlıdır, onların tərkibindəki atomlar spiral zəncirlər əmələ gətirir və ən yaxın qonşuları ilə kovalent bağlarla bağlanır. Buna görə də elementar tellur qeyri-üzvi polimer hesab edilə bilər. Kristal tellur metal parıltı ilə xarakterizə olunur, baxmayaraq ki, kimyəvi xassələri kompleksinə görə onu qeyri-metal kimi təsnif etmək olar. Tellur kövrəkdir və toz halına gətirmək olduqca asandır. Tellurun amorf modifikasiyasının mövcudluğu məsələsi aydın şəkildə həll edilməmişdir. Tellur və ya tellur turşusundan tellur reduksiya edildikdə, bir çöküntü əmələ gəlir, lakin bu hissəciklərin həqiqətən amorf və ya sadəcə çox kiçik kristallar olduğu hələ də aydın deyil.
İki rəngli anhidrid
Kükürd analoquna uyğun olaraq tellur 2–, 4+ və 6+, daha az hallarda isə 2+ valentlik nümayiş etdirir. Tellur monoksid TeO yalnız qaz halında ola bilər və asanlıqla TeO 2-ə oksidləşir. Bu, 733°C-də parçalanmadan əriyən ağ rəngli, hiqroskopik olmayan, tamamilə dayanıqlı kristal maddədir; molekulları belə qurulmuş bir polimer quruluşa malikdir:
Tellurium dioksidi suda demək olar ki, həll olunmur - 1,5 milyon su hissəsinə TeO 2-nin yalnız bir hissəsi məhlula keçir və cüzi konsentrasiyalı zəif tellur turşusu H 2 TeO 3 məhlulu əmələ gəlir. Tellur turşusu H 6 TeO 6-nın turşu xüsusiyyətləri də zəif ifadə edilir. Bu düstur (H 2 TeO 4 deyil) ona suda çox həll olunan Ag 6 TeO 6 və Hg 3 TeO 6 tərkibli duzlar alındıqdan sonra təyin edilmişdir. Tellur turşusunu əmələ gətirən anhidrid TeO 3 suda praktiki olaraq həll olunmur. Bu maddə iki modifikasiyada mövcuddur - sarı və boz: α-TeO 3 və β-TeO 3. Boz tellur anhidridi çox dayanıqlıdır: qızdırıldıqda belə, turşuların və konsentratlı qələvilərin təsirinə məruz qalmır. Qatılaşdırılmış kaustik kaliumda qarışığı qaynadaraq sarı çeşiddən təmizlənir.
İkinci istisna
Mendeleyev dövri cədvəli yaratarkən telluru və ona qonşu olan yodu (eləcə də arqon və kalium) VI və VII qruplara atom çəkilərinə uyğun deyil, əksinə yerləşdirdi. Həqiqətən, tellurun atom kütləsi 127,61, yodun isə 126,91-dir. Bu o deməkdir ki, yod tellurun arxasında deyil, onun qarşısında olmalıdır. Mendeleyev isə öz mülahizəsinin düzgünlüyünə şübhə etmirdi, çünki o, bu elementlərin atom çəkilərinin kifayət qədər dəqiq müəyyən edilmədiyinə inanırdı. Mendeleyevin yaxın dostu, çex kimyaçısı Boquslav Brauner tellur və yodun atom çəkilərini diqqətlə yoxladı, lakin onun məlumatları əvvəlkilərlə üst-üstə düşdü. Qaydanı təsdiq edən istisnaların etibarlılığı yalnız dövri sistem atom çəkilərinə deyil, nüvə yüklərinə əsaslandıqda, hər iki elementin izotop tərkibi məlum olduqda müəyyən edildi. Tellur, yoddan fərqli olaraq, ağır izotoplarla üstünlük təşkil edir.
Yeri gəlmişkən, izotoplar haqqında. Hal-hazırda 52 nömrəli elementin 22 izotopu məlumdur. Onlardan səkkizi - kütlə nömrələri 120, 122, 123, 124, 125, 126, 128 və 130 - sabitdir. Son iki izotop ən çox yayılmışdır: müvafiq olaraq 31,79 və 34,48%.
Tellur mineralları
Tellurun Yer üzündə seleniumdan əhəmiyyətli dərəcədə az olmasına baxmayaraq, 52-ci elementin həmkarından daha çox mineral məlumdur. Tellur mineralları iki növdür: ya telluridlər, ya da yer qabığında telluridlərin oksidləşməsinin məhsulları. Birincilər arasında bir neçə təbii qızıl birləşmələri arasında olan kalaverit AuTe 2 və krennerit (Au, Ag) Te 2 var. Bizmut, qurğuşun və civənin təbii telluridləri də məlumdur. Doğma tellur təbiətdə çox nadir hallarda olur. Bu elementin kəşfindən əvvəl də bəzən sulfid filizlərində tapılırdı, lakin düzgün müəyyən edilə bilməzdi. Tellur minerallarının praktik əhəmiyyəti yoxdur - bütün sənaye tellurları digər metalların filizlərinin emalının əlavə məhsuludur.
1782-ci ildə F.Müller tərəfindən kəşf edilmişdir.Elementin adı latınca tellus,genitive telluris,Yer (bu adı elementi sadə maddə kimi təcrid edən və onun ən mühüm xassələrini təyin edən M.Q.Klaproth tərəfindən təklif edilmişdir) sözlərindən gəlir.
Qəbz:
Təbiətdə 8 sabit izotopun (120, 122-126, 128, 130) qarışığı şəklində mövcuddur. Yer qabığındakı məzmun 10 -7% təşkil edir. Əsas minerallar altayit (PbTe), tellurobismutit (Bi 2 Te 3), tetradimit (Bi 2 Te 2 S), bir çox sulfid filizlərində tapılır.
Mis hasilatı şlamından Na 2 TeO 3 şəklində NaOH məhlulu ilə yuyulma yolu ilə alınır, ondan tellur elektrolitik yolla ayrılır. Əlavə təmizləmə sublimasiya və zona əriməsi ilə həyata keçirilir.
Fiziki xüsusiyyətlər:
Yığcam tellur altıbucaqlı kristal qəfəsə malik, metal parıltılı gümüşü-boz maddədir (sıxlığı 6,24 q/sm 3, ərimə temperaturu - 450°C, qaynama temperaturu - 990°C). Məhlullardan qəhvəyi toz şəklində çökür, buxarda Te 2 molekullarından ibarətdir.
Kimyəvi xassələri:
Tellur otaq temperaturunda havada sabitdir, qızdırıldıqda oksigenlə reaksiya verir. Halojenlərlə qarşılıqlı təsirə girir və qızdırıldıqda bir çox metallarla reaksiya verir.
Qızdırıldıqda tellur su buxarı ilə oksidləşərək tellur (II) oksidini əmələ gətirir və konsentratlaşdırılmış sulfat və azot turşuları ilə reaksiya verir. Qələvilərin sulu məhlullarında qaynadıqda kükürdlə eyni nisbətdə olur:
8 Te + 6NaOH = Na 2 TeO 3 + 2Na 2 Te + 3H 2 O
Birləşmələrdə -2, +4, +6, daha az +2 oksidləşmə vəziyyətini nümayiş etdirir.
Ən vacib əlaqələr:
Tellur (IV) oksidi Tellurium dioksid, TeO 2, suda zəif həll olunur, turşu oksidi, qələvilərlə reaksiyaya girərək tellur turşusu duzlarını əmələ gətirir. Optik eynəklərin tərkib hissəsi olan lazer texnologiyasında istifadə olunur.
Tellur (VI) oksidi, tellur trioksid, TeO 3, sarı və ya boz maddə, suda praktiki olaraq həll olunmur, qızdırıldıqda dioksid əmələ gətirmək üçün parçalanır, qələvilərlə reaksiya verir. Tellur turşusunun parçalanması ilə əldə edilir.
Tellur turşusu, H 2 TeO 3, az həll olunur, polimerləşməyə meyllidir, buna görə də o, adətən dəyişkən sulu TeO 2 *nH 2 O olan çöküntüləri təmsil edir. Duzlar - telluritlər(M 2 TeO 3) və adətən karbonatların TeO 2 ilə sinterlənməsi nəticəsində əldə edilən politelluritlər (M 2 Te 2 O 5 və s.) optik şüşələrin komponentləri kimi istifadə olunur.
Tellur turşusu, H 6 TeO 6, ağ kristallar, isti suda yaxşı həll olunur. Çox zəif bir turşudur, məhlulda MH 5 TeO 6 və M 2 H 4 TeO 6 tərkibinin duzlarını əmələ gətirir. Möhürlənmiş bir ampulada qızdırıldıqda, məhlulda tədricən tellur turşusuna çevrilən metatellurik turşusu H 2 TeO 4 də əldə edildi. duzlar - deyirlər. O, həmçinin oksidləşdirici maddələrin iştirakı ilə tellur (IV) oksidini qələvilərlə əritməklə və ya tellur turşusunu karbonat və ya metal oksidlə əritməklə əldə edilir. Tellurates qələvi metallar həll olunur. Onlar ferroelektriklər, ion dəyişdiricilər və luminescent kompozisiyaların komponentləri kimi istifadə olunur.
Hidrogen telluridi, H 2 Te, alüminium telluridin hidrolizi nəticəsində əldə edilən, xoşagəlməz iyli zəhərli qazdır. Güclü reduksiyaedicidir, məhlulda oksigenlə tez oksidləşərək tellura çevrilir. Sulu məhlulda turşu kükürd və hidrogen seleniddən daha güclüdür. duzlar - telluridlər, adətən qarşılıqlı təsir yolu ilə əldə edilir sadə maddələr, qələvi metal telluridlər həll olunur. Bir çox p və d elementli telluridlər yarımkeçiricilərdir.
Halidlər. Tellurium (II) halogenidləri, məsələn, TeCl 2, duza bənzəyir və qızdırıldıqda və məhlulda Te və Te (IV) birləşmələrinə qeyri-mütənasib olur. Tellur tetrahalidləri - bərk maddələr, məhlulda hidroliz edərək tellur turşusu əmələ gətirir, asanlıqla mürəkkəb halidlər əmələ gətirir (məsələn, K 2). TeF 6 heksafluorid, rəngsiz qaz, kükürd heksafloridindən fərqli olaraq, asanlıqla hidroliz olunur və tellur turşusunu əmələ gətirir.
Ərizə:
Yarımkeçirici materialların komponenti; çuqun, polad, qurğuşun ərintiləri üçün alaşımlı aşqar.
Dünya istehsalı (SSRİ-siz) təxminən 216 ton/ildir (1976).
Tellur və onun birləşmələri zəhərlidir. MPC təxminən 0,01 mq/m3 təşkil edir.
Həmçinin bax: Tellurium // Vikipediya. (giriş tarixi: 23.12.2019).
“Elementlərin kəşfi və onların adlarının mənşəyi”.
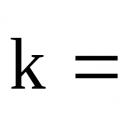 Reaksiya tezliyi sabiti Laboratoriya işi üçün göstərişlər
Reaksiya tezliyi sabiti Laboratoriya işi üçün göstərişlər Ölümdən sonra həyat varmı?
Ölümdən sonra həyat varmı? Alimlər: Yer bəşəriyyət alimləri üçün “kosmik həbsxanadır”: Yer kainatda kosmik həbsxanadır
Alimlər: Yer bəşəriyyət alimləri üçün “kosmik həbsxanadır”: Yer kainatda kosmik həbsxanadır